Hymenoptera venom allergy is a potentially life-threatening allergic reaction following a honeybee, vespid or ant sting. Allergic sting reactions can be mild and restricted to the skin or moderate to severe, with a risk of life-threatening anaphylaxis. Patients should carry an emergency kit containing an adrenaline autoinjector, H1-antihistamines and corticosteroids, depending on the severity of their previous sting reaction(s). The only treatment to prevent further systemic sting reactions is venom immunotherapy.
Alergia la veninul de himenoptere
Hymenoptera venom allergy
First published: 06 mai 2022
Editorial Group: MEDICHUB MEDIA
DOI: 10.26416/Aler.6.2.2022.6607
Abstract
Rezumat
Alergia la veninul de himenoptere este o reacţie alergică ce poate pune viaţa în pericol în urma unei înţepături de albine, viespe sau furnică. Reacţiile alergice pot fi uşoare şi limitate la piele sau moderate până la severe, cu risc de anafilaxie. Pacienţii trebuie să aibă asupra lor o trusă de urgenţă care să conţină un autoinjector de adrenalină, antihistaminice H1 şi corticosteroizi, în funcţie de severitatea reacţiilor lor anterioare. Singurul tratament pentru a preveni alte reacţii sistemice la înţepături este imunoterapia specifică cu venin.
Introducere
Alergia la veninul de himenoptere poate implica o reacţie alergică ce poate pune viaţa în pericol, în urma unei înţepături de albine, viespe sau furnică(1). Aproximativ 9,2% până la 28,7% din populaţia adultă prezintă o sensibilizare la venin de himenoptere, iar prevalenţa reacţiilor sistemice la înţepături în rândul adulţilor variază între 0,3% şi 7,5%(2).
Albinele sunt insecte zburătoare din ordinul Hymenoptera, cu aproximativ 20 000 de specii cunoscute, strâns înrudite cu viespi şi furnici. Speciile de albină sunt Apis mellifera (albină europeană, occidentală sau comună), Apis cerana şi bondarii (Bombus spp.), rudele apropiate ale albinelor, folosiţi pentru polenizarea în sere. Familia Vespidae este împărţită în subfamiliile Vespinae şi Polistinae. Vespula, Dolichovespula şi Vespa alcătuiesc trei genuri de Vespinae. Vespula (denumită „viespe“ în Europa sau „jachete galbene“ în SUA) este cea mai importantă specie în Europa. Speciile Polistes dominula şi Polistes gallicus sunt viespi europene de hârtie.
Tabelul 1 prezintă alergenii moleculari ai veninului de albină, bondar şi viespe, iar alergenii majori, la care mai mult de 50% dintre pacienţi prezintă reactivitate la IgE, sunt marcaţi cu bold. De asemenea, alergenii disponibili pentru diagnosticarea de rutină sunt marcaţi cu un asterisc, iar alergenii cross-reactivi sunt marcaţi cu x(2,3).
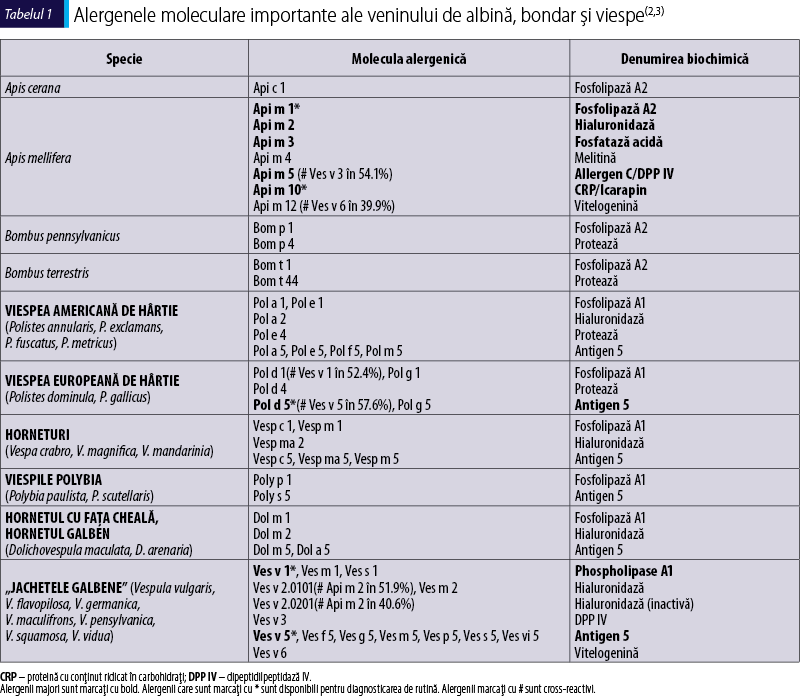
Cantitatea de venin care este injectată în timpul unei înţepături este specifică speciei. Albinele injectează până la 140 mcg de venin, cu un conţinut de proteine de aproximativ 59 mcg, în comparaţie cu viespile, care injectează venin cu un conţinut de proteine cuprins între 1,7 şi 3,1 mcg („yellow jacket“), până la 17 mcg (specia Polistes)(4).
Aspecte clinice
Reacţiile la înţepăturile de himenoptere sunt împărţite, în general, în reacţii locale şi sistemice(5).
Reacţii locale
O reacţie locală este definită ca orice reacţie în care semnele şi simptomele sunt limitate la ţesuturile învecinate cu locul înţepăturii. Cel mai frecvent apar doar reacţii locale minore (durere, edem, prurit trecător), care nu sunt considerate o formă de reacţie alergică, ci simptomele apar din cauza componentelor iritative şi toxice ale veninului.
Mai rar, pacienţii pot dezvolta reacţii locale mari care constau în edem şi eritem dureros limitat la piele şi la ţesuturile subcutanate contigue cu locul înţepăturii. Zona afectată este de obicei mai mare de 10 centimetri, iar reacţia atinge de obicei un vârf la 48 de ore şi poate dura 3 până la 10 zile. Dintre aceşti pacienţi, foarte puţini dezvoltă reacţii mai severe când sunt reînţepaţi cu aceeaşi insectă,l iaro reacţie locală extinsă nu este un predictor al severităţii alergiei(3).
Reacţii sistemice
Reacţiile sistemice – sau generalizate – ori anafilaxia includ urticarie, angioedem, prurit, eritem, nefropatie neobişnuită, sindrom neurologic central şi periferic, purpură trombocitopenică idiopatică, rabdomioliză, simptome vasculare sau respiratorii, bradicardie, aritmie, angină, infarct miocardic, crampe abdominale, contracţii ale musculaturii netede uterine sau ale tractului gastrointestinal. Simptomele încep de obicei la 10-30 de minute după înţepătură, dar pot apărea şi mai rapid (de exemplu, la pacienţii cu boli mastocitare) sau mai lent în 1‑4 ore(6). Reacţiile anafilactice la înţepăturile de himenoptere sunt severe şi pot provoca rapid un deces, timpul mediu al unui stop cardiorespirator putând fi observat în aproximativ 15 minute de la înţepătură. În tabelul 2 sunt descrise gradele anafilaxiei la veninul de himenoptere după Mueller(3,5,6,7,8,9,10).
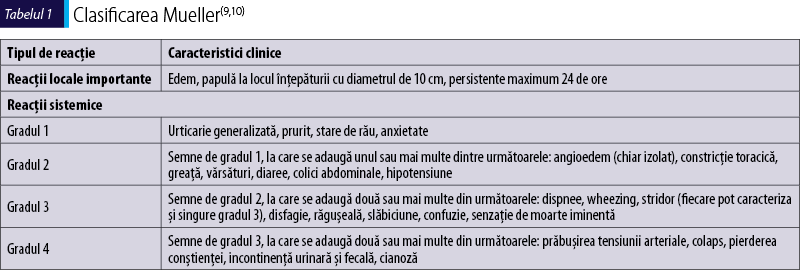
Anafilaxia bifazică este o anafilaxie recurentă, o reapariţie a simptomelor după ameliorarea completă a anafilaxiei, fără reexpunere la factorii declanşatori. Aceasta poate să apară între una şi 78 de ore de la debutul reacţiei anafilactice iniţiale şi trebuie diferenţiată clinic de o reacţie care nu răspunde pe deplin la tratamentul iniţial şi persistă sau revine rapid. Aproximativ jumătate din reacţiile bifazice apar în primele 6-12 ore după reacţia anafilactică iniţială. Incidenţa raportată a reacţiilor bifazice variază de la 3% la 20% dintre pacienţii care se prezintă în serviciul de urgenţă. Factorii de risc pentru o anafilaxie bifazică includ anafilaxia severă şi necesarul de mai mult de o doză de adrenalină pentru a trata anafilaxia. Factorii de risc suplimentari includ tahicardia, trigger necunoscut al anafilaxiei, semnele şi simptomele cutanate şi triggerul medicamentos la copii. Observaţia medicală este recomandată timp de o oră pentru cei fără risc de anafilaxie bifazică, iar pentru cei aflaţi la risc, 6 ore sau mai mult, până la remiterea completă a simptomatologiei(8,11,12).
Principalii factori de risc pentru reacţiile alergice severe la veninurile de insecte sunt concentraţia crescută a triptazei serice (independent de bolile mastocitare), mastocitoza, vârsta înaintată, sexul masculin, medicaţia pentru hipertensiune arterială (IECA, betablocante), alergia diagnosticată la viespe şi reacţiile sistemice la înţepăturile anterioare. De remarcat că nu există o diferenţă semnificativă, privind frecvenţa alergiei la veninul de himenoptere, la populaţia atopică şi cea nonatopică(3).
Diagnostic
Scopul diagnosticului în alergia la himenoptere este de a clasifica tipul de reacţie şi de a identifica insecta incriminată. În prezent, diagnosticul se bazează pe istoricul clinic, pe testele cutanate şi/sau pe detectarea anticorpilor IgE specifici faţă de venin(2).
Istoricul pacientului
Acesta trebuie să cuprindă informaţii precum numărul şi data reacţiilor la înţepătură, tipul şi severitatea simptomelor, intervalul de timp de la înţepătură şi până la apariţia simptomelor, tratamentul de urgenţă, locul înţepăturii, acul reţinut sau îndepărtat, mediul şi activităţile înainte de înţepătură, factorii de risc ai unei reacţii deosebit de severe, factori de risc pentru înţepături repetate, înţepături tolerate după primele reacţii sistemice şi alte alergii(13).
Testele cutanate
Testele cutanate se efectuează sub formă de test prick sau test intradermic cu extract de venin la cel puţin două săptămâni după ce a avut loc reacţia la înţepătură, pentru a evita eventuale rezultate falsnegative. Sensibilitatea testului cutanat prick este mai mică decât cea a testului intradermic (până la 1 mcg/ml), care trebuie utilizat pentru a confirma rezultatul negativ la testul prick. Nu există o corelaţie între severitatea reacţiilor la înţepătură şi reactivitatea testelor cutanate la extractele întregi de venin(2).
IgE totale
Determinarea IgE totale poate fi utilă pentru interpretarea adecvată a IgE specifice faţă de alergen, în special în cazul unui nivel foarte scăzut de IgE specifice. La persoanele asimptomatice cu IgE totale crescute, sunt observaţi frecvent anticorpi specifici la veninurile de himenoptere şi se corelează cu starea de atopie(14).
IgE specifice faţă de alergen
IgE specifice veninului pot fi detectate imediat după înţepătură, dar momentul optim va fi mai târziu de 1‑4 săptămâni, când va avea loc o creştere a producţiei de IgE.
Nu există o corelaţie între severitatea reacţiilor la înţepătură şi concentraţia de IgE specifice la extractele întregi de venin, iar unii pacienţi cu nivel minim sau absent de anticorpi IgE specifici veninului pot dezvolta anafilaxie severă(5,13,15). Nivelul de sensibilizare (cutanată sau IgE serică) este corelat cu frecvenţa, dar nu şi cu severitatea reacţiei. Indivizii sensibilizaţi cu niveluri scăzute de IgE totale (<50 kU/L) au avut un risc mai mare de reacţii severe(5,17).
Determinările IgE specifice faţă de extractele de venin de albină sau viespe ar putea arăta rezultate fals pozitive din cauza:
-
sensibilizării la mai multe veninuri sau a
-
interferenţei anticorpilor IgE îndreptaţi împotriva determinanţilor carbohidraţi cu reactivitate încrucişată (CCD) sau
-
din cauza prezenţei alergenilor omologi din diferite veninuri.
În sens contrar, rezultatele ar putea fi fals negative din cauza subreprezentării anumitor alergeni din extract. Acest lucru se poate evita prin utilizarea diagnosticului molecular cu alergene recombinate(2).
Triptaza serică bazală
Se recomandă determinarea concentraţiei de triptază la toţi pacienţii cu antecedente de reacţie severă după o înţepătură de himenopter. Pacienţii adulţi cu mastocitoză şi/sau valori iniţiale crescute ale triptazei serice sunt expuşi riscului de reacţii mai severe în urma înţepăturilor(2).
Testul de activare a bazofilelor (BAT)
Acesta este un test util şi poate fi folosit ca instrument de diagnostic în unele cazuri specifice. BAT permite identificarea a aproximativ două treimi dintre pacienţii cu reacţii sistemice la înţepătură, dar cu IgE specifice veninului şi cu rezultate negative ale testelor cutanate. BAT este, de asemenea, recomandat la pacienţii cu rezultate neconcludente dublu pozitive (şi albină, şi viespe) la testele cutanate sau cu alergene recombinate, mai ales dacă pacientul a avut o reacţie anafilactică la o singură insectă, facilitând astfel decizia selecţiei speciei de venin pentru imunoterapie specifică la pacienţii cu dublă pozitivitate(18). Deoarece rezultatele BAT sunt influenţate de prezenţa CCD-urilor din veninuri, BAT împreună cu un diagnostic bazat pe componente moleculare pot fi utile pentru o mai bună abordare de diagnostic al alergiei la veninul de himenoptere(16,18).
Testul de provocare cu insecta
O provocare cu înţepătura unei insecte vii nu este recomandată ca instrument de diagnostic la pacienţii netrataţi cu imunoterapie şi ar trebui să servească doar drept control al succesului imunoterapiei cu venin(5).
Testul de inhibiţie a IgE
Testul de inhibiţie a IgE este util pentru a face distincţia între reactivitate încrucişată şi dublă sensibilizare. Cu toate acestea, este un test costisitor, iar rezultatele sunt uneori dificil de interpretat(5,13).
Tratament
Prevenţia expunerii la insecte se face prin evitarea parfumurilor, a îmbrăcămintei florale sau colorate, consumul cu grijă al alimentelor în aerul liber, purtarea încălţămintei afară, evitarea lovirii insectelor, ţinerea închisă a geamurilor autovehiculului şi păstrarea distanţei faţă de stupi(2,5).
Farmacoterapia (trusa de urgenţă)
Dat fiind riscul de reacţii severe, pacienţii alergici la venin trebuie să aibă asupra lor o brăţară de atenţionare şi o trusă de urgenţă, mai ales:
-
în timpul sezonului insectelor
-
în special persoanele expuse la risc, cum sunt apicultorii, grădinarii, lucrătorii din managementul deşeurilor, pacienţii cu boală mastocitară sau cu triptază serică iniţială crescută ori cu alte comorbidităţi
-
anafilaxie severă în antecedente
-
în alergia la albină
-
sexul masculin, cu vârsta >45 de ani(2,5).
Trusa de urgenţă trebuie să cuprindă două autoinjectoare cu adrenalină, antihistaminic şi corticosteroid. Adrenalina este medicamentul de elecţie pentru tratamentul anafilaxiei. Doza recomandată este de 0,01 mg/kg corp, până la 0,3 mg la copii şi 0,3-0,5 mg la adulţi, în funcţie de severitatea reacţiei. Injectarea intramusculară în coapsa anterolaterală va obţine o concentraţie plasmatică mai rapidă şi mai mare decât injecţia subcutanată sau intramusculară în braţ(5,7,8).
Imunoterapia specifică la veninul de himenoptere (VIT)
VIT constă în administrarea repetată de alergen la intervale regulate, pentru a modula răspunsul imun, astfel încât să se reducă simptomele şi nevoia de medicaţie(1). Mecanismele detaliate de inducere a toleranţei imunologice în timpul VIT nu sunt complet înţelese. Se crede că Lf Treg specifice veninului şi Lf Th1 sunt induse în timpul VIT şi sunt capabile să suprime Lf Th2 proalergice. Mai mult, suprimarea Lf Th2 duce la reducerea nivelurilor de citokine, cum ar fi IL-4, IL-5, IL-9 şi IL-13, rezultând o desensibilizare a mastocitelor şi a bazofilelor, stimulând astfel trecerea la un fenotip tolerogen(19).
Recomandări în VIT(1):
-
este recomandată la copii şi adulţi în urma unei reacţii alergice sistemice cu o sensibilizare documentată la venin fie prin test cutanat prick şi/sau cu teste specifice IgE serice şi/sau cu testul de activare a bazofilelor (BAT)(20);
-
este recomandată la adulţii cu simptome cutanate, dar cu risc ridicat de reexpunere şi/sau afectare a calităţii vieţii;
-
este recomandată la pacienţii cu reacţii locale extinse recurente şi supărătoare, pentru a reduce durata şi dimensiunea reacţiilor locale extinse viitoare(21);
-
nu este recomandată persoanelor la care se descoperă accidental sensibilizarea la venin de insecte şi care nu au simptome clinice;
-
nu este recomandată la pacienţii cu reacţii neobişnuite care nu reprezintă reacţii sistemice de tip imediat;
-
bolile cardiovasculare nu sunt o contraindicaţie pentru VIT – pe baza profilului risc/beneficiu(22);
-
pe baza profilului risc/beneficiu, tratamentul cu betablocante nu este o contraindicaţie pentru VIT(22);
-
în tratamentul cu inhibitori ai enzimei de conversie a angiotensinei (IECA) – terapia poate fi continuată în timpul VIT, dar pacientul trebuie informat despre posibilele riscuri(22);
-
precauţie în tratamentul cu inhibitori ai monoaminooxidazei (IMAO) – ele previn descompunerea medicamentelor simpatomimetice, ceea ce ar putea duce la hipertensiune în eventualitatea unei reacţii adverse(22);
-
în bolile neoplazice maligne – VIT poate fi recomandată la pacienţii alergici la venin cu risc ridicat, când boala malignă este stabilă sau în remisiune(22);
-
în bolile autoimune – VIT poate fi recomandată pacienţilor internaţi cu afecţiuni autoimune specifice organului când boala de bază este stabilizată(22);
-
VIT la copiii cu vârsta sub 5 ani ar trebui luată în considerare numai în cazul unor reacţii severe la înţepături şi când copilul este capabil de a coopera(23);
-
în sarcină nu este recomandată iniţierea VIT, dar este permisă continuarea administrării dozei de întreţinere a VIT, tolerată înainte de sarcină(22,24);
-
precauţie în mastocitoză – reprezintă un factor de risc atât pentru dezvoltarea alergiei la veninul de himenoptere, cât şi pentru reacţii sistemice mai severe(22);
-
preparatele purificate cu venin pot fi recomandate deoarece au o frecvenţă mai mică a evenimentelor adverse locale şi sistemice decât preparatele apoase nepurificate;
-
la pacienţii cu antecedente de reacţii sistemice la înţepături sau cu reacţii iniţiale severe şi teste clar dublu pozitive, se recomandă VIT cu două veninuri (adică Apis mellifera şi Vespula sau Vespula şi Polistes);
-
se recomandă premedicaţie cu antihistaminice H1 deoarece se reduc reacţiile locale mari şi, într-o oarecare măsură, de asemenea, evenimentele adverse sistemice;
-
se recomandă administrarea unei doze standard de întreţinere de 100 mcg de venin;
-
dacă pacienţii reacţionează în continuare la înţepăturile de venin, se recomandă o creştere a dozei la 200 mcg de venin;
-
se recomandă administrarea injecţiilor la fiecare 4 săptămâni în primul an de tratament, la fiecare 6 săptămâni în al doilea an şi, în cazul unui tratament de 5 ani, la fiecare 8 săptămâni în anii 3-5;
-
în cazul terapiei pe tot parcursul vieţii, intervalele de 12 săptămâni pot fi încă sigure şi eficiente;
-
se recomandă efectuarea VIT cel puţin 3 ani; la pacienţii cu reacţii iniţiale severe, se recomandă un tratament de cel puţin 5 ani;
-
VIT pe tot parcursul vieţii poate fi recomandată la pacienţii cu alergie la venin de albină care sunt foarte expuşi, la pacienţii cu reacţii iniţiale la înţepătură foarte severe (gradul IV Muller sau gradul III-IV conform Ring & Messmer), la pacienţii cu efecte secundare sistemice în timpul VIT, deoarece sunt factori de risc majori pentru recidivă;
-
în timpul şi după VIT, autoinjectorul cu adrenalină nu este necesar a fi recomandat la pacienţii cu reacţii iniţiale uşoare până la moderate, fără factori de risc pentru recidivă;
-
în timpul şi după VIT, autoinjectorul cu adrenalină poate fi recomandat la pacienţii cu risc de înţepături multiple sau cu factori de risc pentru recidivă;
-
se recomandă ca pacienţii trataţi cu venin de albine şi cei cu protocoale de desensibilizare rapidă să fie monitorizaţi cu atenţie pentru efectele secundare, deoarece aceştia au un risc mai mare de a prezenta evenimente adverse;
-
în cazul evenimentelor adverse sistemice legate de VIT în timpul fazei de iniţiere, se recomandată reducerea temporară a dozei de venin (de exemplu, trecerea cu una sau două trepte înapoi în protocol), iar în cazul evenimentelor adverse sistemice repetate în timpul reluării dozei, se poate recomanda o premedicaţie cu omalizumab;
-
în cazul reacţiilor locale extinse legate de VIT, se recomandă împărţirea dozei în două injecţii sau schimbarea locului de injectare, şi nu neapărat a se reduce doza de venin;
-
se recomandă evitarea înţepăturilor de insecte în timpul fazei de iniţiere, prin respectarea măsurilor de prevenţie (de exemplu, oprirea apiculturii) până la atingerea dozei de întreţinere(1).
Imunoterapia specifică la veninul de himenoptere s-a dovedit a fi foarte eficientă în îmbunătăţirea calităţii vieţii pacienţilor alergici la venin şi reduce semnificativ riscul de reacţii sistemice la înţepătura de insectă în timpul şi după finalizarea imunoterapiei.
Bibliografie
-
Sturm GJ, et al. EAACI guidelines on allergen immunotherapy: Hymenoptera venom allergy. Allergy. 2018 Apr;73(4):744-764.
-
Matricardi PM, et al. EAACI Molecular Allergology User's Guide. Pediatr Allergy Immunol. 2016 May;27 Suppl 23:1-250.
-
Schiener M, Graessel A, Ollert M, Schmidt-Weber CB, Blank S. Allergen-specific immunotherapy of Hymenoptera venom allergy – also a matter of diagnosis. Hum Vaccin Immunother. 2017 Oct 3;13(10):2467-2481.
-
Schumacher M, Tveten M, Egen N. Rate and quantity of delivery of venom from honeybee stings. J Allergy Clin Immunol. 1994; 93:831- 5.
-
Golden DB. Stinging insect hypersensitivity: A practice parameter update 2016. Ann Allergy Asthma Immunol. 2017;118(1):28.
-
Golden DB. Anaphylaxis to insect stings. Immunol Allergy Clin North Am 2015; 35:287-302.
-
Muraro A, et al. European Academy of Allergy and Clinical Immunology, Food Allergy, Anaphylaxis Guidelines Group. EAACI guidelines: Anaphylaxis (2021 update). Allergy. 2022 Feb;77(2):357-37.
-
Cardona V, et al. World allergy organization anaphylaxis guidance 2020. World Allergy Organ J. 2020 Oct 30;13(10):100472.
-
Mueller UR. Clinical presentation and pathogenesis. In: Mueller UR, editor. Insect sting allergy. Stuttggart: Gustav Fischer; 1990. p. 33-65.
-
Mueller HL. Diagnosis and treatment of insect sensitivity. J Asthma Res 1966; 3:331-333.
-
Lee S, Bellolio MF, Hess EP, Erwin P, Murad MH, Campbell RL. Time of onset and predictors of biphasic anaphylactic reactions: a systematic review and meta-analysis. J Allergy Clin Immunol Pract. 2014;3:408–416.e2.
-
Shaker MS, Wallace DV, Golden DBK, et al. Anaphylaxis—a 2020 practice parameter update, systematic review, and Volume 13, No. 10, October 2020 23 Grading of Recommendations, Assessment, Development and Evaluation (GRADE) analysis. J Allergy Clin Immunol. 2020;145:1082–1123.
-
Biló BM, Rueff F, Mosbech H, Bonifazi F, Oude-Elberink JN; EAACI Interest Group on Insect Venom Hypersensitivity. Diagnosis of Hymenoptera venom allergy. Allergy. 2005 Nov;60(11):1339-49.
-
Sturm GJ, et al. EAACI guidelines on allergen immunotherapy: Hymenoptera venom allergy. Allergy. 2018 Apr;73(4):744-764.
-
Matricardi PM, et al. EAACI Molecular Allergology User's Guide. Pediatr Allergy Immunol. 2016 May;27 Suppl 23:1-250.
-
Schiener M, Graessel A, Ollert M, Schmidt-Weber CB, Blank S. Allergen-specific immunotherapy of Hymenoptera venom allergy – also a matter of diagnosis. Hum Vaccin Immunother. 2017 Oct 3;13(10):2467-2481.
-
Schumacher M, Tveten M, Egen N. Rate and quantity of delivery of venom from honeybee stings. J Allergy Clin Immunol. 1994; 93:831- 5.
-
Golden DB, Stinging insect hypersensitivity: A practice parameter update 2016. Ann Allergy Asthma Immunol. 2017;118(1):28.
-
Golden DB. Anaphylaxis to insect stings. Immunol Allergy Clin North Am. 2015; 35:287-302.
-
Muraro A, et al; European Academy of Allergy and Clinical Immunology, Food Allergy, Anaphylaxis Guidelines Group. EAACI guidelines: Anaphylaxis (2021 update). Allergy. 2022 Feb;77(2):357-37.
-
Cardona V,et al. World allergy organization anaphylaxis guidance 2020. World Allergy Organ J. 2020 Oct 30;13(10):100472.
-
Mueller UR. Clinical presentation and pathogenesis. In: Mueller UR, editor. Insect sting allergy. Stuttggart: Gustav Fischer; 1990. p. 33-65.
-
Mueller HL. Diagnosis and treatment of insect sensitivity. J Asthma Res 1966; 3:331-333.
-
Lee S, Bellolio MF, Hess EP, Erwin P, Murad MH, Campbell RL. Time of onset and predictors of biphasic anaphylactic reactions: a systematic review and meta-analysis. J Allergy Clin Immunol Pract. 2014;3:408–416.e2.
-
Shaker MS, Wallace DV, Golden DBK, et al. Anaphylaxis—a 2020 practice parameter update, systematic review, and Volume 13, No. 10, October 2020 23 Grading of Recommendations, Assessment, Development and Evaluation (GRADE) analysis. J Allergy Clin Immunol. 2020;145:1082–1123.
-
Biló BM, Rueff F, Mosbech H, Bonifazi F, Oude-Elberink JN; EAACI Interest Group on Insect Venom Hypersensitivity. Diagnosis of Hymenoptera venom allergy. Allergy. 2005 Nov;60(11):1339-49
Articole din ediţiile anterioare
Noi direcţii în imunoterapia alergenică
Este cunoscut faptul că imunoterapia alergenică (AIT) este singurul tratament care poate modifica evoluţia bolii alergice şi poate conferi toleranţ...
Antiinflamatoarele nesteroidiene – cofactor în reacţiile alergice la alimente
Antiinflamatoarele nesteroidiene (AINS) sunt utilizate frecvent pentru proprietăţile lor analgezice, antipiretice şi antiinflamatoare, la toate gru...
Forme gastrointestinale ale alergiilor alimentare non-IgE-mediate
Reacţiile de hipersensibilitate la alimente au impact negativ major asupra calităţii vieţii pacientului, dar nu numai asupra lui, ci şi asupra fami...
Sensibilizarea la acarienii din praful de casă – o interpretare moleculară
Acarienii din praful de casă reprezintă principala cauză de alergie respiratorie, iar reactivitatea atopică la produsele lor este una dintre cele m...