Omalizumab is the first monoclonal antibody approved for use in patients with chronic spontaneous urticaria who remain symptomatic despite H1 antihistamine treatment. Recent data on the dosage of this drug in urticaria and practical aspects of subcutaneous administration of prefilled syringes with omalizumab during the COVID-19 vaccination campaign are presented. In our opinion, doses of omalizumab before and after COVID-19 vaccination should be injected subcutaneously in the thigh or abdomen, avoiding the same arm as the site of intramuscular injection of the vaccine. The recommendations for the time intervals between COVID-19 vaccinations and biological treatments are presented in accordance with the Position Paper of the German Society of Allergology and Clinical Immunology (DGAKI) and the German Society of Applied Allergology (AeDA). COVID-19 vaccination should be given between two administrations of omalizumab, preferably with a time lag of at least one week after the previous biological treatment and at least one week before the next planned biological treatment.
Aspecte practice ale tratamentului cu omalizumab în urticaria spontană cronică în perioada campaniei de vaccinare împotriva COVID-19
Practical aspects of treatment with omalizumab in chronic spontaneous urticaria during COVID-19 vaccination campaign
First published: 27 aprilie 2021
Editorial Group: MEDICHUB MEDIA
DOI: 10.26416/Aler.5.2.2021.4909
Abstract
Rezumat
Omalizumab este primul anticorp monoclonal aprobat pentru utilizare la pacienţii cu urticarie cronică spontană care rămân simptomatici în ciuda tratamentului antihistaminic H1. Sunt prezentate date recente privind posologia acestui medicament în urticarie şi aspecte practice referitoare la administrarea subcutanată din seringi preumplute cu omalizumab în perioada campaniei de vaccinare împotriva COVID-19. În opinia noastră, dozele de omalizumab înainte şi după vaccinarea împotriva COVID-19 trebuie injectate subcutanat în coapsă sau în abdomen, evitând acelaşi braţ ca loc de injectare intramusculară a vaccinului. Recomandările pentru intervalele de timp dintre vaccinările împotriva COVID-19 şi tratamentele biologice sunt prezentate în conformitate cu Documentul de poziţie al Societăţii Germane de Alergologie şi Imunologie Clinică (DGAKI) şi al Societăţii Germane de Alergologie Aplicată (AeDA). Vaccinarea împotriva COVID-19 trebuie efectuată în intervalul dintre două administrări de omalizumab, preferabil cu un decalaj de cel puţin o săptămână după tratamentul biologic anterior şi cel puţin o săptămână înainte de următorul tratament biologic planificat.
Urticaria spontană cronică este o afecţiune relativ frecventă, cu prevalenţă de aproximativ 1%, caracterizată prin papule urticariene şi prurit, asociate sau nu cu angioedem, care afectează calitatea vieţii pacienţilor, familiilor şi prietenilor acestora, cu costuri semnificative atât pentru aceştia, cât şi pentru sistemul de sănătate(1-4).
Ghidul internaţional pentru urticarie EAACI/GA2LEN/EDF/WAO (European Academy of Allergy and Clinical Immunology/Global Allergy and Asthma European Network/European Dermatology Forum/World Allergy Organization) recomandă utilizarea unui antihistaminic H1 de a doua generaţie în doze standard ca terapie de primă linie(2). Cu toate acestea, tratamentul antihistaminic H1 controlează manifestările clinice la mai puţin de jumătate dintre pacienţi. Doze de antihistaminice H1 de a doua generaţie mai mari decât cele convenţionale (până la de patru ori) sunt recomandate pentru urticarie ca farmacoterapie de linia a doua, putând îmbunătăţi răspunsul terapeutic. Cu toate acestea, multe cazuri nu răspund la antihistaminice H1 orale de generaţie nouă şi necesită o abordare terapeutică mai eficientă(5,6).
Anticorpul monoclonal anti-IgE omalizumab este primul medicament biologic aprobat pentru tratamentul pacienţilor cu urticarie spontană cronică care rămân simptomatici în ciuda tratamentului antihistaminic H1. Agenţia Europeană de Medicamentului (EMA, European Medicine Agency) recomandă omalizumab ca tratament adjuvant al urticariei cronice spontane cu răspuns neadecvat la tratamentul cu antihistaminice H1, la adulţi şi adolescenţi (12 ani şi peste această vârstă) în doză de 300 mg s.c. la fiecare 4 săptămâni. De asemenea, Administraţia pentru Alimente şi Medicamente din Statele Unite ale Americii (FDA; Food and Drug Administration) recomandă omalizumab pentru tratamentul urticariei cronice, în doze de 150 sau 300 mg s.c. la fiecare 4 săptămâni, la adulţi şi adolescenţi care rămân simptomatici în ciuda tratamentului antihistaminic H1(1).
O revizuire sistematică recentă a EAACI relevă faptul că omalizumab 300 mg s.c. ca tratament suplimentar reduce semnificativ semnele şi simptomele urticariei, precum şi impactul urticariei cronice, cu o certitudine moderată a dovezilor. Pentru doza de 150 mg s.c., diferenţa minimă importantă nu este atinsă pentru niciunul dintre punctele finale observate. Pentru ambele doze există o probabilitate crescută de a obţine un răspuns complet şi un risc mai scăzut de a experimenta un scor de activitate urticariană UAS7 de agravare după oprirea tratamentului. În general, omalizumab îmbunătăţeşte calitatea vieţii, dar numai doza de 300 mg s.c. atinge semnificaţia clinică (peste diferenţa minimă importantă) cu o certitudine ridicată a dovezilor. Implicaţiile pentru practica alergologică includ faptul că doar doza de 300 mg s.c. de omalizumab a prezentat o îmbunătăţire a rezultatelor critice legate de urticaria spontană cronică, cu certitudine moderată şi o îmbunătăţire semnificativă a calităţii vieţii, cu o mare certitudine a dovezilor. Datele de siguranţă pe termen scurt sunt favorabile(1).
Experienţa din studiile clinice privind tratamentul cu durata de peste 6 luni pentru această indicaţie este limitată(7). Un studiu recent sugerează că tratamentul fără întrerupere timp de mai mult de un an poate reduce riscul de recidivă la pacienţii care răspund optim la terapia cu acest anticorp monoclonal(8). Mai mult, exacerbarea urticariei spontane cronice, posibilă în cazul COVID-19 produsă de noul tip de coronavirus SARS‑CoV-2, răspunde rapid şi excelent la omalizumab(9).
Omalizumab trebuie administrat doar subcutanat (s.c.), nu pe cale intravenoasă sau intramusculară. Dozele de peste 150 mg trebuie administrate în două sau mai multe locuri de injectare. Omalizumab se comercializează fie ca pulbere şi solvent pentru soluţie injectabilă, fie sub formă de soluţie injectabilă în seringi preumplute pentru administrare subcutanată, toate formele farmaceutice conţinând polisorbat 20 ca excipient(7).
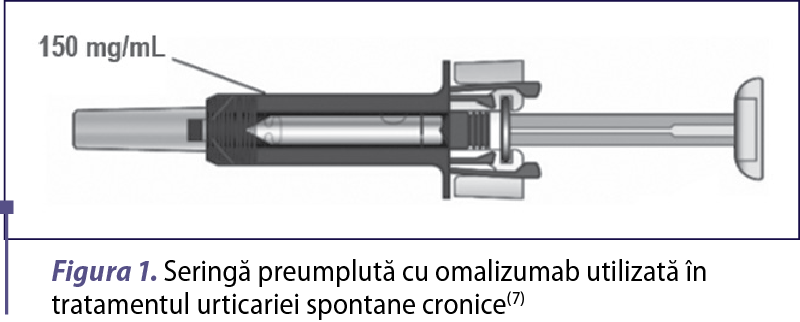
Pentru pacienţii cu urticarie, seringile preumplute cu 1 mL de soluţie conţin 150 mg de omalizumab (figura 1). Din motive practice, seringile preumplute cu 0,5 mL de soluţie care conţin 75 mg de omalizumab nu sunt preferate la pacienţii cu urticarie cronică.
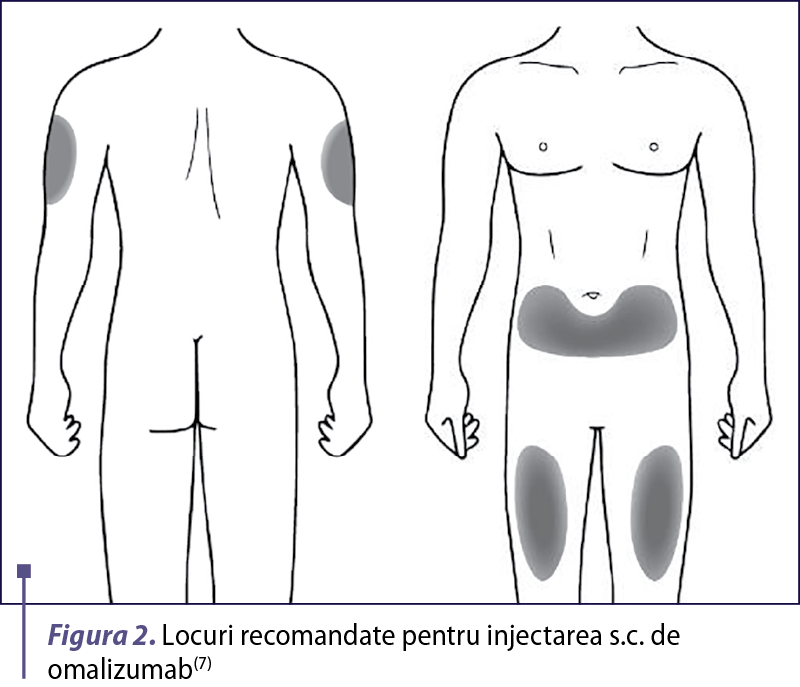
Locurile de injectare s.c. recomandate pentru administrarea de omalizumab sunt la nivelul părţii superioare a braţelor, părţii anterioare a coapselor sau în partea inferioară a abdomenului (nu periombilica, pe o rază de 5 cm) (figura 2). În urticaria cronică, pentru a atinge doza recomandată de 300 mg s.c., se utilizează două injecţii cu seringi preumplute de 150 mg omalizumab. Se alege un loc diferit la fiecare injectare s.c. la o distanţă de cel puţin 2,5 cm unul de celălalt. Omalizumab nu se injectează în nevi, cicatrice, echimoze, vergeturi, eroziuni sau ulceraţii(7).
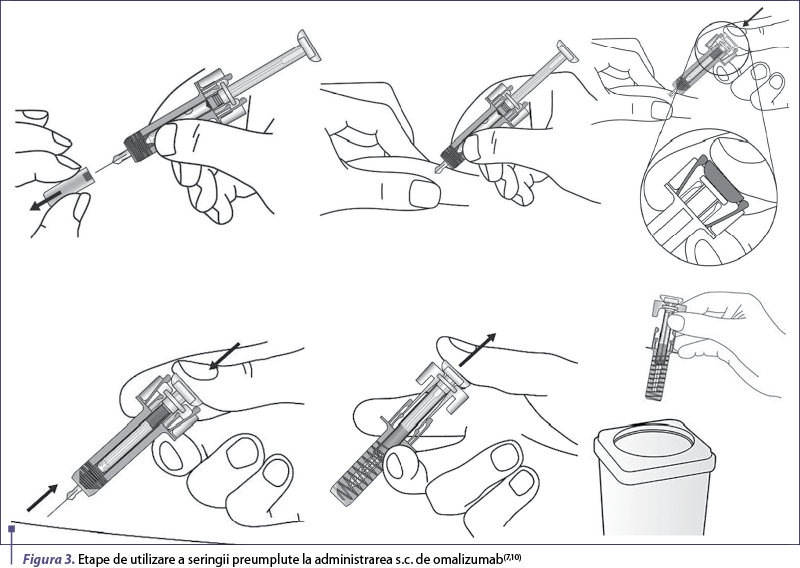
Etapele de utilizare a seringilor preumplute pentru administrarea s.c. de omalizumab sunt detaliate în figura 3. Profesioniştii din domeniul sănătăţii, pacienţii sau aparţinătorii trebuie instruiţi să administreze s.c. omalizumab în conformitate cu instrucţiunile furnizate în prospect(7).
Din cauza posibilelor reacţii adverse de hipersensibilitate de tip imediat, primele trei doze de omalizumab trebuie administrate fie de către un profesionist din domeniul sănătăţii, fie sub supravegherea acestuia(7). Reacţiile anafilactice pot apărea rareori, la aproximativ 0,09% dintre pacienţii trataţi cu omalizumab. S-a constatat că peste 60% dintre acestea au apărut în primele două ore postadministrare şi după primele trei injecţii(11).
În fenotipul distinct de urticarie spontană cronică rezistentă, asocierea omalizumabului cu un agent imunosupresor, cum ar fi ciclosporina A, s-a dovedit a fi eficace şi sigură în experienţa din viaţa reală, dar sunt necesare studii mai aprofundate pentru a verifica aceste date publicate recent(12).
Este important de subliniat că urticaria cronică persistă de obicei câţiva ani (peste 12 luni la 25-75% dintre pacienţi) şi durează adesea mai mult de un an înainte ca un management eficient al bolii să fie implementat. Deoarece peste 25% dintre cazurile de urticarie cronică sunt rezistente la antihistaminice H1 chiar şi la doze mari(13), tratamentul cu omalizumab este important de luat în considerare.
Aşa cum am menţionat anterior, doza recomandată de omalizumab în urticaria spontană cronică este de 300 mg s.c. la fiecare patru săptămâni, iar aspectele practice referitoare la administrarea s.c. din seringi preumplute sunt importante atât pentru eficienţă, cât şi pentru siguranţă. Se recomandă ca medicii prescriptori să reevalueze periodic necesitatea continuării terapiei(7). Un răspuns terapeutic rapid la omalizumab apare la majoritatea pacienţilor cu forme severe de boală, dar în unele cazuri răspunsul la omalizumab poate deveni clinic evident după mai mult de 3 luni de la iniţierea tratamentului. Din păcate, până în prezent, nu se poate anticipa viteza de răspuns, pacienţii neresponsivi şi/sau cei care răspund întârziat prezentând foarte multe asemănări clinice şi serologice cu pacienţii responsivi(14).
O provocare practică importantă în tratamentul regulat cu omalizumab la pacienţii cu urticarie spontană cronică este reprezentată de pandemia actuală cu SARS‑CoV-2 care produce COVID-19(15). Pandemia în curs de desfăşurare a afectat sănătatea a zeci de milioane de oameni din întreaga lume, iar vaccinurile împotriva COVID-19 sunt considerate cea mai importantă strategie de combatere a ei(16).
În prezent, două vaccinuri pe bază de ARN mesager (de la BioNTech-Pfizer şi de la Moderna), care conţin polietilen glicol (PEG 2000) în nanoparticulele lipidice, şi două vaccinuri pe bază de vector adenoviral (de la AstraZeneca şi de la Janssen – Johnson & Johnson), care conţin polisorbat 80 ca excipient, au fost aprobate de EMA în Europa. Conform rezumatului caracteristicilor produsului (RCP) al acestor patru vaccinuri împotriva COVID-19, terapiile imunomodulatoare cu agenţi biologici nu sunt contraindicate în timpul campaniei de vaccinare(17-20).
Campania de vaccinare împotriva COVID-19 a demarat în România la sfârşitul lui decembrie 2020(21). Este foarte important să se ofere informaţii cu privire la posibilele interacţiuni imunologice şi riscuri potenţiale ale agenţilor imunomodulatori reprezentaţi de anticorpi monoclonali în timpul imunizării concomitente cu vaccinurile aprobate. Pacienţii cu urticarie spontană cronică nu prezintă risc crescut de reacţii alergice la vaccinarea împotriva COVID-19. Cu toate acestea, vaccinarea poate duce la exacerbare tranzitorie din cauza stimulării imunitare. Antihistaminicele H1 orale nu afectează eficienţa vaccinării. Pacienţii trataţi cu corticosteroizi sistemici şi/sau ciclosporină pot fi de asemenea vaccinaţi, dar efectul vaccinării poate fi redus în perioada de imunosupresie sistemică. Pacienţii trataţi cu omalizumab, în schimb, pot fi vaccinaţi oricând. Ca şi în cazul altor agenţi biologici, se recomandă ca vaccinarea să fie administrată între injecţiile cu omalizumab, cu posibile modificări discrete ale intervalelor de administrare a tratamentului biologic(22).
Recomandările pentru intervalele de timp dintre vaccinările împotriva COVID-19 şi tratamentele biologice sunt prezentate în conformitate cu Documentul de poziţie al Societăţii Germane de Alergologie şi Imunologie Clinică (DGAKI) şi al Societăţii Germane de Alergologie Aplicată (AeDA). Cu un interval de patru săptămâni între administrări pentru omalizumab, vaccinurile de tip ARN mesager, cu intervale de 3 săptămâni şi respectiv 4 săptămâni între cele două doze, pot fi programate astfel încât schemele de tratament planificate pentru administrarea regulată de omalizumab să nu fie modificate major. Atât în cazul vaccinului cu vector adenoviral de cimpanzeu, la care a doua doză trebuie să fie administrată după un interval de timp cuprins între 4 şi 12 săptămâni, cât şi în cazul celui cu vector adenoviral uman cu doză unică, schemele de vaccinare şi administrare a omalizumabului sunt mai uşor de planificat(22).
Omalizumab nu trebuie întrerupt temporar din cauza vaccinării planificate împotriva COVID-19, deoarece nu este contraindicat în cazul acestor vaccinuri. Cu toate acestea, vaccinarea împotriva COVID-19 trebuie administrată în intervalul dintre două administrări de omalizumab, cu un decalaj de timp de cel puţin o săptămână după tratamentul biologic anterior sau cel puţin o săptămână înainte de următorul tratament biologic planificat(22).
În opinia noastră, dozele de omalizumab înainte şi după vaccinarea împotriva COVID-19 trebuie injectate subcutanat în coapsă sau în abdomen, evitând acelaşi braţ ca loc de injectare intramusculară a vaccinului.
Dacă este posibil, administrarea în clinică a agenţilor biologici poate fi înlocuită cu administrarea la domiciliu, cu o monitorizare atentă şi furnizarea suficientă de medicamente în perioada pandemiei(23). Pacienţii fără antecedente cunoscute de anafilaxie îşi pot autoadministra omalizumab sau medicamentul poate fi administrat de către un aparţinător, începând cu doza a patra, dacă un medic stabileşte că acest lucru este adecvat(7).
Injecţiile de omalizumab ca agent biologic pentru urticarie şi vaccinurile împotriva COVID-19 trebuie efectuate la date diferite, astfel încât, dacă apare o reacţie adversă la vaccinare(24,25), agentul cauzal să fie mai uşor de identificat.
În concluzie, aspectele practice referitoare la administrarea subcutanată din seringi preumplute cu omalizumab pentru urticaria spontană cronică sunt importante în perioada campaniei de vaccinare împotriva COVID-19 din actuala pandemie cu SARS-CoV-2.
Bibliografie
- Agache I, Rocha C, Pereira A, et al. Efficacy and safety of treatment with omalizumab for chronic spontaneous urticaria – a systematic review for the EAACI Biologicals Guidelines. Allergy. 2020; 10.1111/all.14547. doi:10.1111/all.14547
- Zuberbier T, Aberer W, Asero R, et al. The EAACI/GA2LEN/EDF/WAO guideline for the definition, classification, diagnosis and management of urticaria. Allergy. 2018; 73(7):1393-1414.
- Eyerich S, Metz M, Bossios A, Eyerich K. New biological treatments for asthma and skin allergies. Allergy. 2020; 75(3):546-560.
- Maurer M, Abuzakouk M, Berard F, et al. The burden of chronic spontaneous urticaria is substantial: real-world evidence from ASSURE-CSU. Allergy 2017; 72: 2005-2016.
- Maurer M, Raap U, Staubach P, et al. Antihistamine-resistant chronic spontaneous urticaria: 1-year data from the AWARE study. Clin Exp Allergy. 2019: 49; 655-662.
- Shahar E, Bergman R, Guttman-Yassky E, Pollack S. Treatment of severe chronic idiopathic urticaria with oral mycophenolate mofetil in patients not responding to antihistamines and/or corticosteroids. Int J Dermatol. 2006; 45(10): 1224-1227.
- Rezumatul Caracteristicilor Produsului. Data ultimei reînnoiri a autorizaţiei de punere pe piaţă: 22 iunie 2015, www.ema.europa.eu/en/documents/product-information/xolair-epar-product-information_ro.pdf. Accesare la data: 23.04.2021
- Su O, Bahali AG, Onsun N. The Effect of At Least 1-year Use of Omalizumab without Interruption on Relapse in Patients with Chronic Spontaneous Urticaria [published online ahead of print, 2020 Aug 13]. Dermatol Ther. 2020; e14192. doi:10.1111/dth.14192
- Criado PR, Criado RFJ, Pincelli TP, et al. Chronic spontaneous urticaria exacerbation in a patient with COVID-19: rapid and excellent response to omalizumab [published online ahead of print, 2020 Aug 17]. Int J Dermatol. 2020;10.1111/ijd.15134. doi:10.1111/ijd.15134
- Highlights of prescribing information. www.gene.com/download/pdf/xolair_prescribing.pdf. Accesare la data: 23.04.2021
- Cox L, Lieberman P, Wallace D, et al. American Academy of Allergy, Asthma & Immunology/American College of Allergy, Asthma & Immunology Omalizumab-Associated Anaphylaxis Joint Task Force follow-up report. J Allergy Clin Immunol. 2011; 128(1): 210-212.
- Maoz-Segal R, Levy T, Haj-Yahia S, et al. Combination therapy with omalizumab and an immune-suppressive agent for resistant chronic spontaneous urticaria – A real-life experience. World Allergy Organ J. 2020; 13(8): 100448.
- Gonçalo M, Gimenéz-Arnau A, Al-Ahmad M, et al. The global burden of chronic urticaria for the patient and society. Br J Dermatol. 2020 Sep 21. doi: 10.1111/bjd.19561.
- Asero R. Omalizumab in severe chronic urticaria: are slow and non-responders different? Eur Ann Allergy Clin Immunol. 2020 Sep 11. doi: 10.23822/EurAnnACI.1764-1489.167.
- www.who.int/emergencies/diseases/novel-coronavirus-2019/situation-reports. Accesare la data: 23.04.2021
- Wagner R, Meißner J, Grabski E, Sun Y, Vieths S, Hildt E. Regulatory concepts to guide and promote the accelerated but safe clinical development and licensure of COVID-19 vaccines in Europe. Allergy. 2021 Apr 22. doi: 10.1111/all.14868.
- www.ema.europa.eu/en/documents/product-information/comirnaty-epar-product-information_en.pdf. Accesare la data: 23.04.2021
- www.ema.europa.eu/en/documents/product-information/covid-19-vaccine-moderna-epar-product-information_en.pdf. Accesare la data: 23.04.2021
- www.ema.europa.eu/en/documents/product-information/vaxzevria-previously-covid-19-vaccine-astrazeneca-epar-product-information_en.pdf. Accesare la data: 23.04.2021
- www.ema.europa.eu/en/documents/product-information/covid-19-vaccine-janssen-epar-product-information_en.pdf. Accesare la data: 23.04.2021
- Guvernul României. Strategie de vaccinare împotriva COVID-19 în România. Aprobată prin Hotărârea nr. 1031 din 27 noiembrie 2020, publicată în Monitorul Oficial, Partea I, nr. 1171 din 3 decembrie 2020. http://legislatie.just.ro/Public/DetaliiDocumentAfis/234095. Accesare la data: 23.04.2021
- Pfaar O, Klimek L, Hamelmann E, Kleine-Tebbe J, Taube C, Wagenmann M, Werfel T, Brehler R, Novak N, Mülleneisen N, Becker S, Worm M. COVID-19 vaccination of patients with allergies and type-2 inflammation with concurrent antibody therapy (biologicals) – A Position Paper of the German Society of Allergology and Clinical Immunology (DGAKI) and the German Society for Applied Allergology (AeDA). Allergol Select. 2021; 5: 140-147. doi: 10.5414/ALX02241E.
- Pfaar O, Klimek L, Jutel M, et al. COVID-19 pandemic: Practical considerations on the organization of an allergy clinic-An EAACI/ARIA Position Paper. Allergy. 2021;76(3):648-676. doi:10.1111/all.14453.
- Klimek L, Jutel M, Akdis CA, Bousquet J, Akdis M, Torres-Jaen M, Agache I, Canonica GW, Del Giacco S, O’Mahony L, Shamji MH, Pawankar R, Untersmayr E, Ring J, Bedbrook A, Worm M, Zuberbier T. ARIA-EAACI statement on severe allergic reactions to COVID-19 vaccines – an EAACI-ARIA position paper. Allergy. 2020 Dec 30. doi: 10.1111/all.14726. Epub ahead of print. PMID: 33378789.
- Sokolowska M, Eiwegger T, Ollert M, Torres MJ, Barber D, Del Giacco S, Jutel M, Nadeau KC, Palomares O, Rabin RL, Riggioni C, Vieths S, Agache I, Shamji MH. EAACI statement on the diagnosis, management and prevention of severe allergic reactions to COVID-19 vaccines. Allergy. 2021 Jan 16:10.1111/all.14739. doi: 10.1111/all.14739.
Articole din ediţiile anterioare
Urticaria cronică spontană în practica clinică
Urticaria cronică spontană (UCS) este o patologie care afectează 1-2% din populaţie. Infecţia cronică subiacentă şi stresul mental şi emoţional pot...
Omalizumab în alergiile alimentare – perspectivă terapeutică
Imunoglobulina E (IgE) joacă un rol central în patogeneza bolilor alergice, inclusiv în astm şi alergii alimentare(1). Terapia cu anticorpi monoclo...
Actualităţi privind potenţiali markeri de răspuns la tratamentul cu omalizumab în urticaria cronică spontană
Urticaria este definită de apariţia papulelor urticariene, a angioedemului sau a ambelor timp de mai mult de şase săptămâni în urticaria cronică sa...
Urticaria cronică spontană – utilitatea instrumentelor de evaluare în practica clinică conform ghidului EAACI/GA²LEN/EuroGuiDerm/APAAACI 2021
Urticaria cronică spontană (UCS) este o boală cutanată frecventă şi debilitantă, care afectează calitatea vieţii şi performanţa la locul de muncă ş...