Acetaminophen (paracetamol) is the most commonly used analgesic and antipyretic during pregnancy. Research suggests that acetaminophen use in pregnancy is associated with abnormal fetal neurodevelopment (an increased risk for neurodevelopmental impairment − ADHD, autism and hyperactivity symptoms). Paracetamol causes language delay (less than 50 words at 30 months of age). Other recent studies describe the association of urogenital male malformations after prenatal paracetamol exposure.
Paracetamolul în sarcină: cât este de sigur?
Paracetamol during pregnancy: how safe is it?
First published: 20 mai 2018
Editorial Group: MEDICHUB MEDIA
DOI: 10.26416/Gine.20.2.2018.1711
Abstract
Rezumat
Acetaminofenul (paracetamolul) este cel mai utilizat analgezic şi antitermic în cursul sarcinii. Cercetările sugerează că utilizarea acetaminofenului în sarcină este asociată cu neurodezvoltare anormală (risc crescut de ADHD, autism şi hiperactivitate). Paracetamolul determină întârzierea vorbirii (mai puţin de 50 de cuvinte rostite la 30 de luni). Alte cercetări recente descriu asocierea cu malformaţiile urogenitale la descendenţii de sex masculin după expunerea intrauterină la paracetamol.
Paracetamolul (acetaminofenul) reprezintă cel mai utilizat medicament analgezic şi antipiretic în timpul sarcinii(1-3) şi este considerat de către Food and Drug Administration ca fiind de categoria B în ceea ce priveşte siguranţa administrării lui în sarcină(4). Paracetamolul este un derivat de para-aminofenol din clasa anilidelor, cu acţiune analgezică şi antipiretică. Acţiunea sa antiinflamatoare este foarte redusă, însă poate fi utilizat împotriva durerilor cauzate de inflamaţii(5).
În ultimii ani, expunerea la acetaminofen în timpul sarcinii a fost intens studiată, devenind, totodată, un subiect extrem de controversat. Diferite studii au raportat o serie de efecte nocive în copilăria timpurie, chiar şi după expunerea intrauterină la doze terapeutice. O metaanaliză recent publicată (2018) a inclus printre efectele nocive fetale(1): predispoziţie la astm(2,6), toxicitate testiculară cu risc crescut de criptorhidism(7-9), anomalii morfologice perineale masculine, cu scăderea distanţei anogenitale, care poate influenţa potenţialul reproductiv(2), tulburări ale neurodezvoltării(10-16) (figura 1).
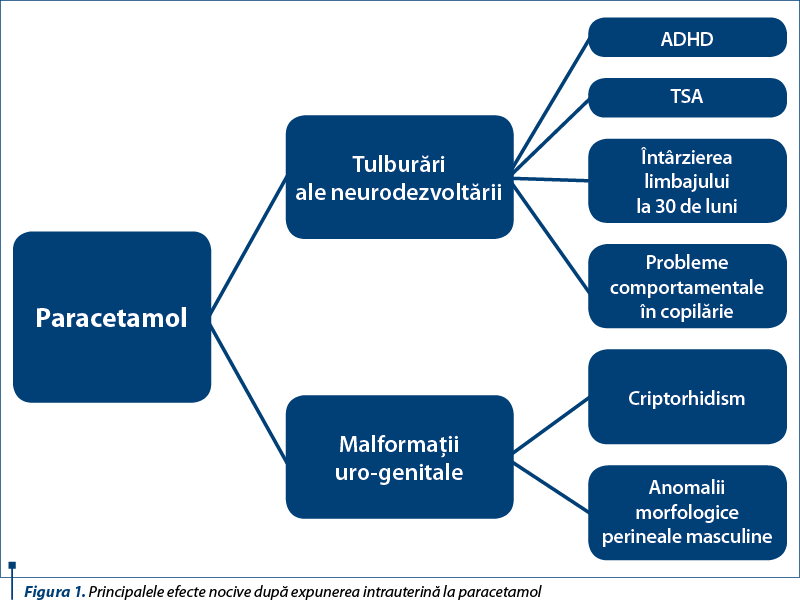
Printre efectele adverse ale paracetamolului asupra neurodezvoltării se numără: tulburarea hiperkinetică cu deficit de atenţie – ADHD(1,2), tulburările din spectrul autist (TSA)(10,12,15,17,18), afectarea dezvoltării neurologice(14,15), probleme comportamentale în copilărie(2). Studiile(1) au arătat că chiar şi doze mici de acetaminofen pot afecta neurodezvoltarea şi că efectele pot deveni vizibile după o perioadă variabilă faţă de momentul expunerii.
Corelaţia între creşterea explozivă a incidenţei cazurilor de ADHD şi TSA în copilărie şi utilizarea uzuală pe scară largă a acetaminofenului în timpul sarcinii au condus la ipoteza asocierii celor două condiţii(3,14). Rezultatele raportate privind această asociere sunt însă insuficiente, cu putere statistică variabilă, adesea scăzută, unele studii neidentificând nicio relaţie de cauzalitate(1,14,19). Integrarea lor însă în cadrul unei metaanalize a demonstrat o legătură semnificativă între administrarea de acetaminofen în sarcină şi anomaliile în neurodezvoltare(1,2). Studiile au fost efectuate prin chestionar ante- şi postnatal şi au demonstrat că acetaminofenul a fost administrat între 18 şi 32 de săptămâni, cu o medie de 5 comprimate la un episod febril, cefalee, viroză respiratorie, gripă cu o durată medie a expunerii de 4-7 zile (maximum 28 de zile)(1,11).
Analiza dovezilor disponibile indică faptul că administrarea de paracetamol în timpul sarcinii este asociată cu un risc crescut cu 20-30% pentru tulburări ale neurodezvoltării(1). S-a sugerat că tulburările de neurodezvoltare observate ca urmare a expunerii in utero la paracetamol sunt consecinţa distrucţiilor neuronale. Studiile pe şoareci sugerează că utilizarea acetaminofenului în timpul sarcinii poate avea consecinţe asupra dezvoltării creierului neonatal, cu afectarea funcţiei cognitive, prin scăderea nivelurilor de BDNF (brain-derived neurotrophic factor) în creier(14,20). La om, acetaminofenul poate interfera cu eliberarea hormonilor materni tiroidieni şi sexuali şi cu mecanismele de acţiune ale acestora la fătul în curs de dezvoltare(1,8,21), efectele fiind dependente de doză(1) şi de vârsta gestaţională. O altă teorie este aceea că acetaminofenul perturbă dezvoltarea creierului prin stresul oxidativ(14). Studiile efectuate la adulţi sugerează că utilizarea pe termen lung a acetaminofenului reduce antioxidanţii serici şi distruge echilibrul oxidant-antioxidant(22). La făt, cantităţi crescute de oxidanţi pot conduce la distrucţie neuronală în momentele critice din timpul neurodezvoltării(23).
În ceea ce priveşte riscul de ADHD, cel mai recent studiu efectuat de Ystrom şi colab. demonstrează că utilizarea acetaminofenului în timpul sarcinii pe o durată mai mică de 8 zile nu a fost asociată cu un risc crescut, iar expunerea pentru 22-28 de zile creşte riscul(24). Observaţii similare a adus şi Stergiakouli în metaanaliza sa din 2016, demonstrând că utilizarea acetaminofenului în timpul trimestrelor II şi III de sarcină este asociată cu un risc mai mare de tulburări hiperkinetice şi hiperactivitate asociată cu deficit de atenţie(11,14). Acest lucru a fost raportat după studiul unui eşantion foarte mare de copii, alături de mamele lor, recrutaţi din registrul naţional de naştere danez(11,14). Utilizarea preconcepţională maternă nu a fost asociată cu ADHD. Utilizarea preconcepţională paternă însă poate conduce la ADHD la descendenţi printr-un mecanism încă neclar, supoziţiile fiind de afectare germinală epigenetică, prin disfuncţie endocrină testiculară(14,25,26).
Expunerea la acetaminofen prenatal la 32 de săptămâni de amenoree a fost asociată, de asemenea, cu apariţia problemelor de ordin emoţional la descendenţi(14).
Rezultatele trebuie însă interpretate cu prudenţă, deoarece studiile analizate sunt heterogene şi au design observaţional, cu posibile rezultate eronate în ceea ce priveşte includerea pacienţilor în studiu (probabilitate crescută de a fi implicaţi şi alţi cofactori ai tulburărilor în neurodezvoltare – genetici, de mediu). Administrarea concomitentă de acetaminofen cu alte substanţe într-un episod febril/infecţios din sarcină, evident, poate spori tulburările în neurodezvoltare, crescând riscul prin dubla expunere. De asemenea, infecţia maternă şi febra pot avea efecte negative asupra neurodezvoltării, ceea ce creează confuzii la includerea subiecţilor în lotul de studiu. Studiile sugerează inclusiv o legătură între hipertermia maternă şi tulburările de comportament/TSA din copilărie(27).
Studiul efectuat de Garcia în 2016 pe 2644 de subiecţi (pereche mamă-copil), cu status socioeconomic variat, recrutaţi în timpul sarcinii, efectuat prin chestionarea antenatală şi postnatală a mamei şi cu evaluarea clinică a copiilor între 1 şi 5 ani, a subliniat faptul că expunerea la acetaminofen în cursul sarcinii poate creşte simptomele tulburărilor din spectrul autist la copiii de sex masculin(12). De asemenea, poate afecta funcţia de atenţie şi poate fi asociată cu un risc mai mare de hiperactivitate/impulsivitate la descendenţi. Nu s-a constatat afectarea funcţiei cognitive, motorii sau a dezvoltării sociale (copiii sunt apţi să acumuleze cunoştinţe, să îşi dezvolte competenţe/aptitudini care să le permită să relaţioneze eficient cu ceilalţi în familie, şcoală şi în comunitate).
Trialul multinaţional efectuat pe un lot de 754 de gravide (2017), care a urmărit dezvoltarea limbajului după expunerea intrauterină în primul trimestru la paracetamol, a obiectivat întârzierea limbajului în 8,5% din cazuri (pronunţarea a mai puţin de 50 de cuvinte la vârsta de 30 de luni şi a fost mai frecventă la băieţi decât la fete)(28), fără a fi precizată doza cu potenţial efect nociv.
În ceea ce priveşte teratogenitatea paracetamolului, cercetările au demonstrat că expunerea intrauterină poate provoca tulburări endocrine în testiculul fetal. Zece studii analizate în cadrul unui trial publicat în 2017(9) au observat o asociere semnificativă între utilizarea paracetamolului în timpul celui de-al doilea trimestru şi dezvoltarea ulterioară a criptorhidismului la descendenţii de sex masculin(9,25,29). Factorii de risc pentru criptorhidism rămân neclari, dar pot fi legaţi de perturbări ale funcţiei endocrine normale în timpul celor două faze de coborâre testiculară (8-15 săptămâni şi respectiv 25-35 de săptămâni de amenoree)(30).
În concluzie, ultimele constatări privind teratogenitatea acetaminofenului sunt alarmante şi justifică investigaţii suplimentare, cu dezvoltarea şi utilizarea unor instrumente valide de evaluare a rezultatelor în urma expunerii la acest medicament. Ţinând cont de numărul mare de femei gravide care utilizează acest medicament (>50% în Statele Unite ale Americii, 50-60% în Uniunea Europeană), chiar şi o mică creştere a riscului de apariţie a unor efecte adverse la copii poate avea implicaţii importante asupra sănătăţii publice(14,31,32).
Pe de altă parte, abţinerea de la a recomanda administrarea de acetaminofen în caz de durere şi febră poate avea, de asemenea, efecte nocive asupra fătului în curs de dezvoltare(33), astfel că paracetamolul rămâne totuşi în prezent medicamentul de primă alegere în aceste situaţii(1,34).
U.S. Food and Drug Administration (FDA) este conştientă şi înţelege preocupările ce decurg din rapoartele recente, care pun sub semnul întrebării siguranţa paracetamolului în sarcină, însă, după evaluarea studiilor publicate în literatura medicală, consideră că ponderea probelor este neconcludentă în ceea ce priveşte o posibilă legătură între utilizarea acetaminofenului în timpul sarcinii şi ADHD la copii(35). Totuşi, din cauza acestei incertitudini, recomandă utilizarea paracetamolului cu prudenţă şi doar la indicaţia medicului specialist.
Prin urmare, în calitate de clinicieni, suntem obligaţi în prezent să le oferim femeilor gravide cele mai recente informaţii privind siguranţa paracetamolului în timpul sarcinii.
Conflict of interests: The authors declare no conflict of interests.
Bibliografie
- Masarwa R, Levine H, Gorelik E, Reif S, Perlman A, Matok I. Prenatal exposure to acetaminophen and risk for attention deficit hyperactivity disorder and autistic spectrum disorder: a systematic review, meta-analysis, and meta-regression analysis of cohort studies. Am J Epidemiol. 2018;kwy086, https://doi.org/10.1093/aje/kwy086
- Toda K. Is acetaminophen safe in pregnancy? Scandinav J Pain. 2017;17(1):445-6. doi:10.1016/j.sjpain.2017.09.007.
- Daw JR, Hanley GE, Greyson DL, et al. Prescription drug use during pregnancy in developed countries: A systematic review. Pharmacoepidemiology and Drug Safety. 2011;20:895-902.
- Babb M, Koren G, Einarson A. Treating pain during pregnancy. Canadian Family Physician. 2010;56:25-7.
- Paracetamol. Wikipedia, encyclopedialiberă. //ro.wikipedia.org/w/index.php?title=Paracetamol&oldid=11467711. 2017.
- Amberbir A, Medhin G, Alem A, et al. The role of acetaminophen and geohelminth infection on the incidence of wheeze and eczema. A longitudinal birth-cohort study. Am J Respir Crit Care Med. 2011;183(2):165-70.
- Kristensen DM, Lesné L, Le Fol V, et al. Paracetamol (acetaminophen), aspirin (acetylsalicylic acid) and indomethacin are anti-androgenic in the rat foetal testis. Int J Androl. 2012;35(3):377-84.
- Kristensen DM, Hass U, Lesn L, et al. Intrauterine exposure to mild analgesics is a risk factor for development of male reproductive disorders in human and rat. Hum Reprod. 2011;26(1):235-44.
- Gurney J, Richiardi L, McGlynn KA, et al. Analgesia use during pregnancy and risk of cryptorchidism: a systematic review and meta-analysis. Hum Reprod. 2017;34(5):1-12.
- Ghanizadeh A. Acetaminophen may mediate oxidative stress and neurotoxicity in autism. Med Hypotheses. 2012;78(2):351.
- Liew Z, Ritz B, Rebordosa C, et al. Acetaminophen use during pregnancy, behavioral problems, and hyperkinetic disorders. JAMA Pediatr. 2014;168(4):313-20.
- Avella-Garcia CB, Julvez J, Fortuny J, et al. Acetaminophen use in pregnancy and neurodevelopment: attention function and autism spectrum symptoms. Int J Epidemiol. 2016;45(6):1987-96.
- Thompson JMD, Waldie KE, Wall CR, et al. Associations between acetaminophen use during pregnancy and ADHD symptoms measured at ages 7 and 11 years. PLoS One. 2014;9(9):e108210.
- Stergiakouli E, Thapar A, Davey Smith G. Association of acetaminophen use during pregnancy with behavioral problems in childhood: evidence against confounding. JAMA Pediatr [Internet]. 2016;170(10):964-70.
- Liew Z, Ritz B, Virk J, et al. Maternal use of acetaminophen during pregnancy and risk of autism spectrum disorders in childhood: A Danish national birth cohort study. Autism Res. 2015;9(9):951-8.
- Schultz KGB and ST. Similarities in features of autism and asthma and a possible link to acetaminophen use. Med Hypotheses. 2012;74(1):7-11.
- Brandlistuen RE, Ystrom E, Nulman I, et al. Prenatal paracetamol exposure and child neurodevelopment: A sibling-controlled cohort study. Int J Epidemiol. 2013;42(6):1702-13.
- Boţ M, Ichim M, Tecuci A, Zvâncă M, Mehedinţu C, Vlădăreanu S. Pre-and perinatal risk factors involved in the development of autistic spectrum disorders in children. Ginecologia.ro. 2017;5(17):29-31.
- Hoover RM, Hayes VAG, Erramouspe J. Association between prenatal acetaminophen exposure and future risk of attention deficit/hyperactivity disorder in children. Annals of Pharmacotherapy. 2015;49:1357-61.
- Viberg H, Eriksson P, Gordh T, Fredriksson A. Paracetamol (acetaminophen) administration during neonatal brain development affects cognitive function and alters its analgesic and anxiolytic response in adult male mice. Toxicol Sci. 2014;138(1):139-47.
- Colborn T. Neurodevelopment and endocrine disruption. Environmental health perspectives. 2004;112:944-9.
- Nuttall SL, Khan JN, Thorpe GH, Langford N, Kendall MJ. The impact of therapeutic doses of paracetamol on serum total antioxidant capacity. J Clin Pharm Ther. 2003;28(4):289-94.
- Posadas I, Santos P, Blanco A, Muñoz-Fernández M, Ceña V. Acetaminophen induces apoptosis in rat cortical neurons. PLoS One. 2010;5(12):e15360.
- Ystrom E, Gustavson K, Brandlistuen RE, et al. Prenatal exposure to acetaminophen and risk of ADHD. Pediatrics. 2017;140(5):e20163840.
- Albert O, Desdoits-Lethimonier C, Lesné L, et al. Paracetamol, aspirin and indomethacin display endocrine disrupting properties in the adult human testis in vitro. Hum Reprod. 2013;28(7):1890-8.
- Mazaud-Guittot S, Nicolas Nicolaz C, Desdoits-Lethimonier C, et al. Paracetamol, aspirin, and indomethacin induce endocrine disturbances in the human fetal testis capable of interfering with testicular descent. J Clin Endocrinol Metab. 2013;98(11):E1757-E1767.
- Hornig M, Bresnahan MA, Che X, et al. Prenatal fever and autism risk. Mol Psychiatry. 2017;23:759-66.
- Bornehag C-G, et al. Prenatal exposure to acetaminophen and children’s language development at 30 months. Eur Psychiatry. 2017; doi:10.1016/j.eurpsy.2017.10.007.
- Snijder CA, Kortenkamp A, Steegers EA, Jaddoe VW, Hofman A, Hass U, Burdorf A. Intrauterine exposure to mild analgesics during pregnancy and the occurrence of cryptorchidism and hypospadia in the offspring: the Generation R Study. Hum Reprod. 2012;27(4):1191-201.
- Hutson JM, Thorup JM, Beasley SW. Descent of the Testis, 2nd ed Switzerland, Springer, 2016.
- CDC. Prevalence of autism spectrum disorders - Autism and developmental disabilities monitoring network, 14 sites, United States, 2008. MMWR Surveill Summ. 2012;61(3):1-19.
- Lupattelli A, Spigset O, Twigg MJ, et al. Medication use in pregnancy: a cross-sectional, multinational web-based study. BMJ Open. 2014;4(2):e004365.
- Dreier JW, Andersen A-MN, Berg-Beckhoff G. Systematic review and meta- analyses: fever in pregnancy and health impacts in the offspring. Pediatrics. 2014;133(3):e674-688.
- Daw JR, Mintzes B, Law MR, et al. Prescription drug use in pregnancy: a retrospective, population-based study in British Columbia, Canada (2001-2006). Clin Ther. 2012;34(1):239-249.e2.
- https://www.fda.gov/Drugs/DrugSafety/ucm429117.htm