The infections of the cutaneous lesions caused by burns represent one of the most frequent causes of mortality and morbidity in burned patients, being an important public health issue. The thermal destruction of the cutaneous barrier and the local and systemic immune depression of the host are essential factors that contribute to the onset of infection in severely burned patients. Depending on the extent of the burned lesions, on the concentration of the pathogenic organisms that colonize the wound and on their penetration over and in the depth of the viable subcutaneous tissue (not burnt), we can define different types of infections, from the wound colonization to the noninvasive and the invasive infections (cellulitis, necrotizing fasciitis). When the microorganisms invade the bloodstream, they can cause septicaemia, which is an important mortality factor. The burn wounds are contaminated most often by bacteria and fungi, among which the most frequent species are Staphylococcus aureus, Pseudomonas aeruginosa and, lately, Acinetobacter baumannii and Klebsiella pneumoniae; the fungal infections represent a mortality predictor in patients with burns on more than 30-60% of the body’s surface area. The pathogenic agents may originate from the host’s normal flora (gastrointestinal and of the upper respiratory tract) and/or from the hospital environment. The emergence of the antimicrobial resistance, especially to nosocomial bacterial isolates, is an important obstacle in the treatment of these infections. Therefore, it is vital to know the microorganisms most frequently involved in the infections of the burn wounds, and their susceptibility to antibiotics.
Infecţii ale leziunilor cutanate cauzate de arsură
Infection of cutaneous lesions caused by burns
First published: 16 octombrie 2020
Editorial Group: MEDICHUB MEDIA
DOI: 10.26416/Med.137.5.2020.3868
Abstract
Rezumat
Infecţiile leziunilor cutanate din pricina arsurii reprezintă una dintre cele mai frecvente cauze de mortalitate şi morbiditate la pacienţii arşi, fiind o importantă problemă de sănătate publică. Distrugerea termică a barierei cutanate şi depresia răspunsului imun local şi sistemic al gazdei sunt factori esenţiali ce contribuie la apariţia infecţiilor în cazul pacienţilor cu arsuri severe. În funcţie de întinderea leziunii arse, de concentraţia de microorganisme patogene care colonizează plaga şi de penetrarea acestora în întinderea şi în profunzimea ţesutului subcutanat viabil (nears), putem defini mai multe tipuri ale infecţiilor, de la colonizarea plăgii la infecţia neinvazivă şi infecţia invazivă (celulita, fasciita necrozantă). Atunci când microorganismele invadează fluxul sanguin, pot provoca septicemie – un factor important de mortalitate. Bacteriile şi fungii contaminează cel mai frecvent rănile arse, cele mai frecvente specii fiind Staphylococcus aureus, Pseudomonas aeruginosa, iar în ultima perioadă şi Acinetobacter baumannii şi Klebsiella pneumoniae; infecţiile fungice constituie un predictor al mortalităţii la pacienţii cu o suprafaţă arsă a corpului de 30-60%. Agenţii patogeni pot proveni din flora normală a gazdei (gastrointestinală şi a tractului respirator superior) şi/sau din mediul spitalicesc. Emergenţa rezistenţei antimicrobiene, mai ales la izolatele bacteriene nozocomiale, este o problemă importantă în tratarea acestor infecţii. De aceea, este vital să cunoaştem microorganismele cel mai des implicate în infecţiile plăgilor arse şi susceptibilitatea acestora la antibiotice.
Introducere
Infecţiile leziunilor cutanate din pricina arsurii reprezintă una dintre cele mai frecvente cauze de mortalitate şi morbiditate la pacienţii arşi şi o importantă problemă de sănătate publică pe plan mondial(1,2).
Arsurile sunt deteriorări ale pielii cauzate de variate surse nemecanice, precum: căldură, substanţe chimice, electricitate, lumina soarelui sau radiaţii nucleare(3). Severitatea arsurilor este determinată pe baza gradului de deteriorare a ţesutului şi a dimensiunii zonei afectate. Pacienţii cu arsuri grave necesită îngrijire specializată imediată pentru a reduce la minimum morbiditatea şi mortalitatea. Aproximativ 180.000 de decese apar anual din cauza arsurilor, iar majoritatea acestora au loc în ţările în curs de dezvoltare, cu venituri mici sau medii, unde incidenţa leziunilor arse este mare, dar infrastructura şi finanţarea pentru gestionarea şi prevenirea arsurilor sunt limitate(4,5). În afara decesului, leziunile provocate de arsuri au condus la un procent mare de morbiditate, cu spitalizare prelungită, desfigurare şi dizabilităţi. În spitalele din SUA sunt tratate în fiecare an aproximativ 500.000 de arsuri; 40.000 au necesitat spitalizare prelungită(6). În 2004, aproape 11 milioane de oameni din întreaga lume au fost arşi suficient de grav pentru a necesita asistenţă medicală(4). Impactul economic cauzat de îngrijirea persoanelor cu arsuri este destul de ridicat. Astfel, în anul 2000, costurile directe pentru îngrijirea copiilor cu arsuri în SUA au depăşit 211 milioane USD. În Norvegia, costurile pentru gestionarea arsurilor în spitale în 2007 au depăşit 10,5 milioane de euro(4). Spre deosebire de alte tipuri de leziuni, rănile provocate de arsuri induc modificări metabolice şi inflamatorii care predispun pacientul la diverse complicaţii. Infecţia este cea mai frecventă cauză de morbiditate şi mortalitate la această populaţie, aproape 61% din decese fiind cauzate de infecţie(7). Pe lângă amploarea leziunii arse care favorizează infecţiile, tipul şi concentraţia de microorganisme care colonizează rana arsă par să influenţeze riscul de infecţie invazivă a plăgii. Agenţii patogeni care infectează rana sunt în primul rând bacterii Gram-pozitive, cum ar fi Staphylococcus aureus rezistent la meticilină (MRSA)(8), şi bacterii Gram-negative, cum ar fi Pseudomonas aeruginosa, Acinetobacter baumannii şi Klebsiella pneumoniae. Toţi aceşti patogeni se remarcă prin rezistenţa lor crescândă la o gamă largă de agenţi antimicrobieni(9,10).
Fiziopatologia arsurii
Plaga arsă are, de obicei, trei zone caracteristice importante: i) zona de coagulare, situată în locul în care pielea a intrat în contact cu sursa de arsură, în centrul plăgii; aici ţesutul cutanat este mort şi formează escara (crusta); ii) zona de stază înconjoară zona de coagulare; ţesutul din această zonă este viu, dar cu un risc ridicat de infecţie şi necroză din cauza irigaţiei scăzute, rezultat al circulaţiei sanguine slabe; iii) zona hiperemică înconjoară zona de stază şi conţine ţesut cutanat relativ sănătos, cu flux sanguin crescut şi vasodilataţie ca răspuns la leziunea celulară, care în această zonă este minimă(11).
În funcţie de gradul de afectare a ţesuturilor, arsurile sunt clasificate în trei categorii(11): arsurile de gradul I, care implică deteriorarea stratului superior al pielii, epidermul; arsurile de gradul II, cu deteriorarea epidermului, precum şi a dermului; arsurile de gradul III, care se referă la deteriorarea sau distrugerea tuturor celor trei straturi ale pielii (epiderm, derm şi hipoderm), precum şi a ţesuturilor care se află sub ea (figura 1).
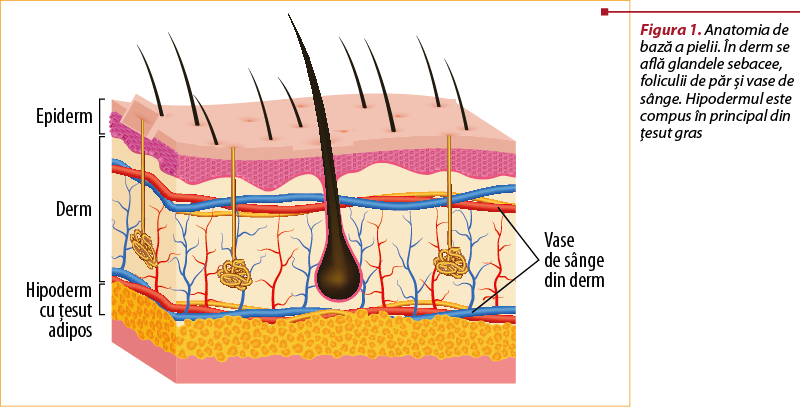
Suprafaţa unei arsuri este determinată adesea prin „regula lui 9”, care împarte corpul în secţiuni ce corespund la aproximativ 9% din suprafaţa corpului(11). De exemplu: un braţ, abdomenul şi capul reprezintă fiecare 9%; dacă toate aceste trei părţi ale corpului ar fi fost arse, s-ar estima că pacientul prezintă arsuri pe 27% din suprafaţa corpului. Severitatea arsurilor este în funcţie de sursa şi gradul arsurii şi de suprafaţa arsă a corpului. În plus, zona corpului unde s-a produs arsura este importantă; de exemplu, arsurile de la nivelul feţei, mâinilor sau picioarelor sunt considerate grave din cauza complicaţiilor care rezultă ca urmare a afectării căilor respiratorii, dexterităţii sau mişcării.
Infecţiile leziunilor arse
Infecţiile leziunilor cutanate arse sunt cauzate de microorganisme patogene care colonizează sau infectează o rană arsă, unde, de obicei, ţesuturile sunt devitalizate.
Potrivit American Burn Association (ABA), diferitele tipuri de infecţii ale plăgilor arse includ colonizarea plăgii, infecţia plăgii şi infecţia invazivă (celulita, fasciita necrozantă)(12).
Colonizarea plăgii se caracterizează prin prezenţa unor concentraţii scăzute de bacterii la suprafaţă, fără invazie sau semne sistemice/simptome de infecţie. În biopsiile tisulare obţinute din pielea colonizată, dar neinfectată, se izolează de obicei mai puţin de 105 bacterii pe gram de ţesut.
Infecţia plăgii este asociată cu o concentraţie mai mare de bacterii în plagă (>105 bacterii pe gram de ţesut), dar fără a penetra în ţesutul subcutanat.
O infecţie invazivă include concentraţii mari de bacterii (frecvent >105 bacterii pe gram de ţesut), penetrarea microorganismelor în întindere şi în profunzimea ţesutului subcutanat viabil, cu separarea supurativă a escarei (crustei) sau pierderea grefei şi cu prezenţa unui răspuns sistemic compatibil cu septicemia. Celulita reprezintă răspândirea infecţiei din plaga arsă în ţesuturile sănătoase din jur şi se manifestă prin eritem, induraţie, căldură şi sensibilitate în ţesutul care înconjoară rana arsă sau escara plăgii. Eritemul singur nu poate indica celulită. Fasciita necrozantă implică o infecţie invazivă agresivă, cu implicarea structurilor de sub piele (ex.: muşchi, oase, organe), cu următoarele semne: temperatura mai mare de 390C sau mai mică de 36,50C, tahicardie progresivă (>110 bătăi pe minut), tahipnee progresivă (>25 respiraţii pe minut).
Deoarece tratamentul arsurilor mai severe implică intervenţii chirurgicale, pot apărea şi infecţii ale plăgii chirurgicale. Se mai descrie şi impetigoul rănii arse, care este o infecţie secundară a pielii reepitelizate(11).
Atunci când microorganismele care au colonizat leziunea arsă invadează fluxul sanguin, se poate produce septicemie – un factor important de mortalitate la pacienţii arşi(3,11,13). Semnele de septicemie sunt: febră, tahicardie, tahipnee, leucocitoză, trombocitopenie, tensiunea arterială sistolică mai mică de 100 mm Hg, insuficienţă multiorganică.
Factorii de risc pentru dezvoltarea unei infecţii a plăgii arse
Aceştia sunt următorii(11): extremele de vârstă; comorbidităţi (ex.: obezitatea şi diabetul); imunosupresie (ex.: SIDA); dispozitive invazive (ex.: catetere); arsuri care implică mai mult de 30% din suprafaţa totală a corpului; arsuri care cuprind întreaga grosime a ţesutului cutanat; îngrijirea necorespunzătoare a arsurilor timpurii; incapacitatea de a acoperi arsurile sau eşuarea grefei de piele – rezultând răni deschise pentru perioade prelungite etc.
Patogenia şi etiologia infecţiilor leziunilor arse
Infecţiile leziunilor arse sunt frecvente deoarece pielea, o barieră fizică împotriva microbilor, a fost compromisă. Distrugerea termică a barierei cutanate şi depresia răspunsului imun local şi sistemic celular şi umoral al gazdei sunt factori esenţiali ce contribuie la apariţia complicaţiilor infecţioase în cazul pacienţilor cu arsuri severe(14). Plaga arsă, indiferent de gradul arsurii, este un mediu bogat în proteine, format din ţesut necrotic avascular (escară/crustă), care oferă o nişă favorabilă colonizării şi proliferării microbiene(15). Absenţa vascularizării zonei arse are ca rezultat migrarea deficitară a celulelor imune ale gazdei (cum ar fi celulele T) şi a agenţilor antimicrobieni în zonă, în timp ce substanţele toxice eliberate de ţesutul necrotic afectează răspunsul imun local al gazdei. În consecinţă, riscul de infecţie creşte proporţional cu dimensiunea arsurii(11).
Deşi suprafeţele rănilor arse sunt sterile imediat după arsură, în cele din urmă acestea vor fi colonizate cu microorganisme. Natura şi întinderea leziunii arse, împreună cu speciile şi concentraţiile de microorganisme care colonizează rana arsă pot favoriza riscul unei infecţii invazive(16,17). Bacteriile şi fungii sunt cei mai frecvenţi agenţi patogeni care contaminează rănile arse. Aceşti microbi formează pe leziunile arse, în 48-72 de ore de la rănire, biofilme multispecii (comunităţi complexe de agregate de microorganisme ataşate la nivelul leziunilor); biofilmele acţionează ca o barieră eficientă împotriva agenţilor antimicrobieni şi a sistemului imunitar al gazdei, rezultând colonizarea persistentă şi infecţia la locul formării biofilmului(11,18).
Infecţiile plăgilor arse apar frecvent în primele săptămâni de spitalizare. Staphylococcus aureus este cel mai frecvent agent patogen care infectează pacienţii arşi, deoarece stafilococii endogeni ai gazdei, localizaţi adânc în glandele sudoripare şi foliculii de păr, supravieţuiesc arsurii şi colonizează suprafaţa plăgii în primele 48 de ore, cu excepţia cazului în care se utilizează agenţi antimicrobieni topici(15). După o perioadă medie de 5 până la 7 zile, aceste răni sunt colonizate cu alţi microbi, bacterii Gram-pozitive, bacterii Gram-negative şi fungi, care pot proveni din flora normală a gazdei (gastrointestinală şi a tractului respirator superior) şi/sau din mediul spitalicesc, sau microbi care sunt transferaţi prin mâinile personalului medical(15,16). În ultimele decenii, agenţii patogeni Gram-negativi (ex.: Pseudomonas aeruginosa, Acinetobacter baumannii şi Klebsiella pneumoniae) au fost detectaţi ca fiind cei mai comuni agenţi etiologici ai infecţiei invazive, ca urmare a factorilor lor de virulenţă şi a rezistenţei antimicrobiene(19-22). Dacă apărarea organismului-gazdă şi măsurile terapeutice (inclusiv excizia ţesutului necrotic şi închiderea plăgii) sunt inadecvate sau întârziate, microbii invadează ţesutul viabil, fiind semnul distinctiv al unui infecţii invazive a plăgii arse.
Colonizarea rănilor de către fungi apare de obicei mai târziu, ca urmare a utilizării antibioticelor cu spectru larg(11,23). Rănile arse complicate de infecţii fungice constituie un predictor al mortalităţii la pacienţii cu o suprafaţă arsă a corpului de 30-60%(24).
Microorganismele transmise din mediul spitalicesc (ex.: Pseudomonas aeruginosa) tind să fie mai rezistente la agenţii antimicrobieni decât cele care provin din flora normală a pacientului(21,25). Cele mai frecvente microorganisme care colonizează şi infectează rănile arse sunt:
-
Bacterii Gram-pozitive – Staphylococcus aureus rezistent la meticilină (MRSA), stafilococi coagulază-negativi, Enterococcus spp., inclusiv enterococi resistenţi la vancomicină (VRE).
-
Bacterii Gram-negative – Pseudomonas aeruginosa, Acinetobacter baumannii, Klebsiella pneumoniae, Escherichia coli, Serratia marcescens, Enterobacter spp., Proteus spp., Bacteroides spp.
-
Fungi: Candida spp., Aspergillus spp., Fusarium spp., Alternaria spp., Rhizopus spp.;
-
Virusuri: Herpes simplex, citomegalovirus, virusul varicelo-zosterian.
Două specii bacteriene, MRSA şi P. aeruginosa, sunt printre cei mai răspândiţi agenţi patogeni care cauzează infecţia plăgilor arse. Aceste două specii s-au dovedit deosebit de dificil de tratat, deoarece posedă un număr mare de factori de virulenţă şi gene de rezistenţă antimicrobiană.
-
Staphylococcus aureus rezistent la meticilină. Aceşti stafilococi sunt bacterii Gram-pozitive şi unii dintre primii colonizatori ai rănilor arse. Posedă capacităţi atât pentru metabolismul aerob, cât şi pentru cel anaerob. MRSA locuieşte în glandele sudoripare, foliculii de păr şi pe mucoasele oamenilor. MRSA poate fi dificil de eradicat, deoarece adesea poate coloniza o gazdă pentru o lungă perioadă înainte de a provoca o infecţie, rămânând nedetectat şi netratat până când apar simptomele infecţiei(26). Pe lângă genele care conferă rezistenţă la antibiotice, factorii de virulenţă ai MRSA includ: proteine de aderenţă, proteine de colonizare, superantigene, exotoxine şi toxine formatoare de pori. Proteinele de aderenţă permit MRSA să adere la ţesuturile-gazdă, ceea ce face dificilă eliminarea acestora. Proteinele de colonizare ajută bacteriile să concureze mai eficient cu alte bacterii. Superantigenele provoacă un răspuns imun crescut în organism, uneori cu până la 20% mai mare decât cel declanşat de bacteriile care nu deţin aceşti factori de virulenţă. Acest lucru este foarte periculos pentru pacienţi (îndeosebi pentru pacienţii imunocompromişi), deoarece poate provoca febră mare, şoc, insuficienţă multiorganică şi/sau sindrom de şoc toxic. Toxinele formatoare de pori pot duce la scurgeri vasculare, şoc hipovolemic şi necroză tisulară(26).
-
Pseudomonas aeruginosa reprezintă cea mai frecventă sursă de infecţie a leziunilor arse, în special în mediul spitalicesc(11). Aceştia sunt bacili Gram-negativi facultativ aerobi, care trăiesc în intestinul uman. Aceste bacterii sunt cunoscute pentru tendinţa lor de a provoca boli la pacienţii imunocompromişi, cum ar fi cei cu SIDA sau fibroză chistică, însă rar la persoanele sănătoase(27). Printre factorii de virulenţă ai P. aeruginosa se regăsesc i) proteazele, factori de virulenţă care degradează integritatea barierelor fizice ale gazdei prin divizarea proteinelor şi aminoacizilor, permiţând o infiltrare mai profundă a infecţiei(27); ii) exotoxina A, care opreşte sinteza proteinelor, provocând leziuni locale ale ţesuturilor, imunosupresie şi moarte celulară(28); iii) hemolizinele, care acţionează ca detergenţi ce descompun lipidele din celulele epiteliale, permiţând bacililor, ca şi proteazele, să pătrundă în gazdă şi să favorizeze răspândirea infecţiei(28).
Semnele infecţiei plăgilor arse
Sunt descrise: schimbarea culorii plăgii (de exemplu, zone focale de roşu, maro sau negru), separarea supurativă a escarei, pierderea grefei, cu implicarea ţesutului viabil sau prezenţa unui răspuns sistemic compatibil cu septicemia, colorarea în verde a grăsimii subcutanate. Aceste semne pot fi însoţite de roşeaţă localizată, căldură şi sensibilitate locală(3,29). Infecţia leziunilor prin arsură este problematică, deoarece în aceste situaţii se întârzie vindecarea, se formează cicatrice, iar un risc foarte mare al infecţiei rănilor arse îl reprezintă septicemia sau sindromul de insuficienţă multiorganică, ceea ce necesită asistenţă medicală imediată şi intensivă. Septicemia prezintă un prognostic sever pentru pacient, rata mortalităţii fiind foarte mare(3,11,13).
Tratament
Înainte de tratarea arsurii, pentru recuperarea pacienţilor arşi trebuie abordate câteva aspecte de mare importanţă: căile respiratorii şi respiraţia; întreţinerea circulaţiei (homeostazia hemodinamică poate fi problematică ca urmare a întreruperii fluxului sanguin şi a pierderii de lichide); metabolismul pacienţilor arşi creşte, ca răspuns la rănire şi, prin urmare, aportul nutriţional trebuie să crească; de asemenea, trebuie luat în considerare managementul durerii(11).
Frecvenţa şi gravitatea complicaţiilor septice la pacienţii arşi impun necesitatea unei abordări diagnostice şi terapeutice precise. Astfel, un scop important în îngrijirea medicală a pacienţilor arşi îl reprezintă prevenirea infecţiei. Excizia timpurie şi grefarea sunt metode chirurgicale principale pentru reducerea riscului de infecţie şi a duratei spitalizării(30). O metaanaliză a tuturor studiilor controlate randomizate disponibile a constatat că excizia timpurie a redus rata mortalităţii la toţi pacienţii arşi care nu au suferit o leziune prin inhalare(31). O închidere rapidă şi permanentă a arsurilor severe, care au implicat toate straturile ţesutului cutanat, poate fi obţinută prin autogrefare (cu grefă de piele nevătămată de la acelaşi pacient).
Investigaţia microbiologică a tampoanelor de suprafaţă şi a biopsiilor din rănile arse oferă informaţii precise cu privire la tipul de infecţie şi la încărcătura bacteriană, dar nu oferă nicio indicaţie asupra profunzimii infecţiei(32,33). Investigaţia microbiologică a tampoanelor superficiale ar trebui, prin urmare, să fie completată cu examinarea histologică pentru a detecta posibila prezenţă a microorganismelor sub escară.
Un aspect important care poate accentua severitatea infecţiei îl reprezintă apariţia şi emergenţa rezistenţei antimicrobiene, mai ales în cazul izolatelor bacteriene nozocomiale. De aceea, este vital să cunoaştem microorganismele cel mai des implicate în etiologia infecţiilor plăgilor arse şi susceptibilitatea acestora la antibiotice. De subliniat că unele cercetări(2) au remarcat o diferenţă semnificativă a profilelor de rezistenţă antimicrobiană între pacienţii arşi şi cei nearşi, precum şi tendinţe temporale diferite ale ratelor de rezistenţă antimicrobiană. Prin urmare, supravegherea periodică a modelelor de rezistenţă la antibiotice în unităţile de arşi ar putea ajuta medicii să aleagă în mod corespunzător antibioticele pentru tratamentul cel mai eficient. Unele testări(34) au remarcat că piperacilina+tazobactam pentru Pseudomonas aeruginosa şi vancomicina şi linezolid pentru Staphylococcus aureus au fost cele mai eficiente şi pot fi utilizate în tratamentul empiric al acestor infecţii, până la obţinerea rezultatelor testării susceptibilităţii la antibiotice.
În concluzie, infecţiile rănilor arse reprezintă o importantă problemă de sănătate publică, fiind printre cele mai frecvente cauze de morbiditate şi mortalitate la pacienţii arşi. Intervenţia imediată pentru tratarea rănilor arse şi prevenirea infecţiilor, ca şi cunoaşterea agenţilor patogeni (specii şi rezistenţă antimicrobiană) cel mai des izolaţi în cadrul acestor infecţii reprezintă un deziderat important în managementul arsurilor.
Bibliografie
-
Sedat Y, Tarik Z, Nurkan T, Targut N, Yusuf Z, Gokhan M, Mehmet H. Bacteriological profile and antibiotic resistance. Journal of Burn Wound and Rehabilitation. 2005;26(6):488.
-
Huang Z, Gan Y, Yang K, Gao L, Xiong B. Characteristics and Evolution of Microbial Drug Resistance in Burnt Patients. Journal of Burn Care & Research. 2020; https://doi.org/10.1093/jbcr/iraa039.
-
Fonseca JA, Hospenthal, DR. Burn Wound Infections. 2019. Available at: http://emedicine.medscape.com/article/213595-overview.
-
WHO. Burns. 2018. Available at: http:/www.who.int/news-room/fact-sheets/detail-burns.
-
Lowin J, Poudel AN, Price PE, Potokar T. A structured review to assess the current status of cost-based burns research in Nepal. J Burn Care Res. 2020 Aug;11; doi: 10.1093/jbcr/iraa125.
-
American Burn Association. Burn Incidence and Treatment in the United States. 2007. Available at: http://www.ameriburn.org/resources_factsheet.php.
-
Gomez R, Murray CK, Hospenthal DR, Cancio LC, Renz EM, Holcomb JB, et al. Causes of mortality by autopsy findings of combat casualties and civilian patients admitted to a burn unit. J Am Coll Surg. 2009 Mar;208(3):348-54.
-
Pangli H, Papp A. The relation between positive screening results and MRSA infections in burn patients. Burns. 2019 Nov;45 (7):1585-1592.
-
Albrecht MC, Griffith ME, Murray CK, Chung KK, Horvath EE, Ward JA. Impact of Acinetobacter infection on the mortality of burn patients. J Am Coll Surg. 2006 October;203:546-50.
-
Keen EF 3rd, Robinson BJ, Hospenthal DR, et al. Prevalence of multidrug-resistant organisms recovered at a military burn center. Burns. 2010 Sept;36:819-25.
-
Church D, Elsayed S, Reid O, Winston B, Lindsay R. Burn Wound Infections. Clinical Microbiology Reviews. 2006;19(2),403-434.
-
Greenhalgh DG, Saffle JR, Holmes JH 4th, Gamelli RL, Palmieri TL, Horton JW. American Burn Association consensus conference to define sepsis and infection in burns. J Burn Care Res. 2007 Nov-Dec;28(6):776-90.
-
Manning J. Sepsis in the Burn Patient. Crit Care Nurs Clin North Am. 2018 Sept;30(3):423-430.
-
Alexander, JW. Mechanism of immunologic suppression in burn injury.
-
J Trauma. 1990;30:S70–S75.
-
Erol S, Altoparlak U, Akcay MN, Celebi F, Parlak M. Changes of microbial flora and wound colonization in burned patients. Burns. 2004;30:357–361.
-
Manson WL, Pernot PC, Fidler V, Sauer EW, Klasen J. Colonization of burns and the duration of hospital stay of severely burned patients. J Hosp Infect. 1992;22:55-63.
-
Barret JP, Herndon DN. Effects of burn wound excision on bacterial colonization and invasion. Plast Reconstr Surg. 2003;111:744–750.
-
Stoodley P, Sauer K, Davies DG, Costerton JW. Biofilms as complex differentiated communities. Annu Rev Microbiol. 2002;56:187–209.
-
Tredget EE, Shankowsky HA, Joffe AM, Inkson TI, Volpel K, Paranchych W, Kibsey PC, Alton JD, Burke FJ. Epidemiology of infections with Pseudomonas aeruginosa in burn patients: the role of hydrotherapy. Clin Infect Dis. 1992;15:941–949.
-
Revathi G, Puri J, Jain BK. Bacteriology of burns. Burns. 1998;24:347–349.
-
Clark NM, Patterson J, Lynch III JP. Antimicrobial resistance among gram-negative organisms in the intensive care unit. Curr Opin Crit Care. 2003;9:413–423.
-
Dalamaga M, Karmaniolas K, Chavelas C, Liatis S, Matekovits H, Migdalis I. Stenotrophomonas maltophilia: a serious and rare complication in patients suffering from burns. Burns. 2003;29:711–713.
-
Burdge JJ, Rea F, Ayers L. Noncandidal, fungal infections of the burn wound.
-
J Burn Care Rehabil. 1988;9:599–601.
-
Horvath EE, Murray CK, Vaughan GM, et al. Fungal wound infection (not colonization) is independently associated with mortality in burn patients. Ann Surg. 2007 Jun;245(6):978-85.
-
Heggers JP, McCoy L, Reisner B, Smith M, Edgar P, Ramirez RJ. Alternate antimicrobial therapy for vancomycin-resistant enterococci burn wound infections. J. Burn Care Rehabil. 1998;19:399–403.
-
Zetola N, Francis JS, Nuermberger EL, Bishai WR. Community-acquired meticillin-resistant Staphylococcus aureus: an emerging threat. Lancet Infect Dis. 2005;5,275-286.
-
Lyczak JB, Cannon CL, Pier GB. Establishment of Pseudomonas aeruginosa infection: lessons from a versatile opportunist. Microbes and Infection. 2000;2,1051-1060.
-
Van Delden C, Iglewski BH. Cell-to-cell signaling and Pseudomonas aeruginosa infections. Emerging Infectious Diseases. 1998;4(4).
-
Greenhalgh DG, Saffle JR, Holmes JH 4th, Gamelli RL, Palmieri TL, Horton JW. American Burn Association consensus conference to define sepsis and infection in burns. J Burn Care Res. 2007 Nov-Dec;28(6):776-90.
-
Rowan MP, Cancio LC, Elster EA, Burmeister DM, Rose LF, Natesan S, et al. Burn wound healing and treatment: review and advancements. Crit Care. 2015 Jun 12;19:243.
-
Avni T, Levcovich A, Ad-El DD, Leibovici L, Paul M. Prophylactic antibiotics for burns patients: systematic review and meta-analysis. BMJ. 2010 Feb 15;340:c241.
-
Herjinder K, Jyothi B, Anup R, Savinder R, Vijay G. Bacterial profile of blood and burn wound infections in burn patients, proceeding of national symposium on Tribal Health, 2008.
-
Mago V. Burn wound septicemia, analysis of burn wound infections burn ward. Journal of Burn care and Research. 2009;30(3):540.
-
Chaudhary NA, Munawar MD, Khan MT, et al. Epidemiology, Bacteriological Profile, and Antibiotic Sensitivity Pattern of Burn Wounds in the Burn Unit of a Tertiary Care Hospital. Cureus. 2019 June;11(6):e4794. DOI 10.7759/cureus.4794.
Articole din ediţiile anterioare
Tratamentul și prevenirea infecţiilor de tract urinar la femei - implicaţii în practica medicilor de familie
Infecțiile de tract urinar (ITU) au o prevalență crescută la nivel global. Deși nu reprezintă o patologie gravă în lipsa complicațiilor, gestionare...