The breeding in captivity of different species of turtles and tortoises in many cases does not correlate with the needs of feeding and microclimate, frequently leading to the development of a disease that has never been recorded in wild specimens. The most frequently produced are severe metabolic changes that can evolve or may favor other pathologies. Most cases, consecutive to poor feeding, are diagnosed with hypovitaminosis, severe metabolic syndromes, nutritional secondary hyperparathyroidism and haemorrhagic septicemia. As secondary pathologies caused by primary metabolic disorders are generalized infection or sepsis and ulcerative or necrotic stomatitis. In many cases the primary diagnosis is difficult because of the chronic evolution, in most situations presenting late to the doctor, when symptoms are evident to the owner. The therapeutic conduct is hampered by a number of derived pathologies which amplifies the primary symptoms and pathology changes, especially the general metabolism, complicating the treatment regimens.
Orientări clinico-terapeutice în patologia testudidelor de companie
Clinical and therapeutic guidelines for Testudines pets
First published: 10 aprilie 2017
Editorial Group: MEDICHUB MEDIA
DOI: 10.26416/PV.26.1.2017.577
Abstract
Rezumat
În multe situații, creșterea în captivitate a unor specii de broaște țestoase nu se corelează cu necesitățile de hrănire și microclimat, conducând frecvent la dezvoltarea unei patologii care nu a fost niciodată înregistrată la exemplarele sălbatice. Cel mai frecvent sunt produse modificări metabolice care pot evolua sever sau pot favoriza alte patologii secundare. Cele mai multe cazuri, consecutive hrănirii necorespunzătoare, sunt diagnosticate cu hipovitaminoze, sindroame metabolice severe, septicemie hemoragică și hiperparatiroidismul nutrițional secundar. Ca patologii secundare determinate de dereglări metabolice primare sunt infecțiile generalizate sau septicemiile și stomatitele necrotice sau ulcerative. În multe cazuri, diagnosticul este dificil, în primul rând ca urmare a evoluției cronice, în majoritatea situațiilor prezentarea la medic fiind târzie, atunci când simptomatologia este evidentă pentru proprietar. Conduita terapeutică este îngreunată de o serie de patologii derivate care amplifică simptomatologia primară și modificările patologice, în special metabolismul general, complicând schemele terapeutice.
Întreținerea în captivitate a unor specii tot mai diverse de animale a condus la extinderea noțiunii de „animal de companie”, fiind crescute și chiar reproduse specii de animale la mare distanță de locul de origine. Cel mai frecvent, lipsa cunoștințelor despre biologia speciei sau cunoașterea parțială a necesităților a condus la apariția unor grave erori de întreținere, care în timp s-au transformat în patologie specifică, cel mai adesea fiind asociată cu deficiențe metabolice grave. Broaștele țestoase au devenit animale de companie preferate de adulți sau copii, în special datorită conformației ciudate și aspectului deosebit față de alte specii de animale de companie. Aceste specii sunt încadrate taxonomic în Clasa Reptilia, Subclasa Anapsida, Ordinul Testudines. Acest ordin este divizat în mai multe familii și genuri, care includ numeroase specii de broaște țestoase terestre sau acvatice, specii în extincție sau încă prezente în mediul natural, majoritatea fiind adevărate fosile vii (primele specii ale acestui ordin formându-se acum peste 157 de milioane de ani). Dintre aceste specii, multe au devenit animale de companie, atrăgând oamenii prin formă, culori sau obiceiuri comportamentale. Restrângerea habitatului ca urmare a extinderii și intensificării activității umane (agricultură, exploatații forestiere sau acvatice, baraje, turism etc.) a condus la diminuarea populațională a multor specii, iar în numeroase cazuri a determinat chiar extincția sau reducerea populațională la un număr de indivizi, riscant pentru activitatea reproductivă (ca diversitate genetică) și de menținere a speciei. Un exemplu elocvent îl reprezintă speciile genului Chelonoidis, care fie o parte a dispărut, fie sunt pe cale de dispariție, fiind incluse în programe internaționale de protecție. Multe alte specii au un regim legislativ special, însă din necunoaștere sunt preluate din mediul natural, așa cum se întâmplă frecvent cu specii ale genului Testudo. În ultimii ani au început să fie crescute în captivitate diferite specii ale Familiei Testudinidae, și în special țestoase din genul Testudo:
- T. graeca - T. g. graeca (țestoasa africană), T. g. soussensis (țestoasa marocană), T. g. marokkensis (țestoasa marocană nordică), T. g. nabeulensis (țestoasa tunisiană), T. g. cyrenaica (țestoasa libiană), T. g. ibera (țestoasa iberică), T. g. armeniaca (țestoasa armenească), T. g. buxtoni (țestoasa de Marea Caspică), T. g. terrestris (țestoasa libiană), T. g. zarudnyi (țestoasa de Azerbaidjan), T. g. whitei (țestoasa algeriană);
- Testudo hermanni - Testudo hermanni hermanni (țestoasa lui Herman vestică), Testudo hermanni boettgeri (țestoasa lui Herman estică), care populează și zonele sudice și estice din țara noastră, Testudo hermanni hercegovinensis (țestoasa de Dalmația);
- Testudo horsfieldii - țestoasa rusească de stepă sau țestoasa terestră a lui Horsfield - una dintre cele mai populare în captivitate;
- Testudo kleinmanni - țestoasa egipteană;
- Testudo marginata - țestoasa grecească.
Întreținerea în captivitate a acestor specii provenite din regiuni diferite nu s-a corelat cu asigurarea unor condiții corespunzătoare de viață, în special cu amenajarea și organizarea corectă a unor terarii care să ofere parametrii de confort sau cel puțin o temperatură adecvată și o dietă corespunzătoare. Cel mai frecvent, lipsa cunoștințelor despre biologia acestor specii sau cunoașterea parțială a ecobiologiei lor a condus la apariția unor grave erori de întreținere în captivitate, care în timp s-au transformat în patologie specifică, adeseori fiind dezvoltate deficiențe metabolice grave.
Juvenilii de țestoase care ajung în punctele de vânzare din magazine sunt ținuți în condiții nepotrivite cu necesitățile lor metabolice, deseori asigurându-se temperaturi mai ridicate decât intervalul de confort, pentru a obliga broscuțele să fie agitate și să manifeste o vioiciune exagerată care să atragă cumpărătorii. La acestea se adaugă și hrănirea cu vegetale obținute din culturi intensive și care conțin cantități mari de compuși chimici nocivi sau se utilizează formule de premixuri peletate sau granulate care (în special la vârstele mici) determină dezechilibre digestive și favorizează dereglări metabolice evolutive, cu consecințe patologice grave atât pe termen scurt, cât și pe intervale de timp mari. De multe ori, dereglările produse la vârste mici încep să determine semne clinice după mai multe luni, fiind bine cunoscută și descrisă de mulți autori capacitatea compensatorie uriașă a acestor specii și a chelonienilor în general. Afectarea generală a metabolismului are consecințe directe asupra statusului imunitar și a capacității organismului de a face față agresiunilor infecțioase. Diferite specii de virusuri sau bacterii care în mod natural nu afectează testudidele reușesc în aceste condiții să producă, singure sau asociate, stări morbide, care în multe situații evoluează agravant și chiar letal.
O altă problemă specială este reprezentată de faptul că patologia reptilelor, în general, include o serie de particularități care se referă atât la etiologie și patogeneză, cât și la diagnostic și conduită terapeutică. Testudidele prezintă un grad de dificultate sporit privind patologia și intervenția medicală, din două motive: diferențe anatomo-fiziologice semnificative (chiar față de alte familii sau ordine cu care au legături filogenetice strânse) și necesități ecobiologice particulare. Din punct de vedere taxonomic, familiile și subfamiliile încadrează o multitudine de specii cu comportamente sau patologii extrem de diferite, uneori chiar în cadrul aceluiași gen. Țestoasele terestre sunt frecvent purtătoare de bacterii patogene, fără a dezvolta stări clinice și aparent fără a prezenta afectări ale organelor sau țesuturilor unde sunt cantonate acestea.
Țestoasele de apă dulce au devenit și ele animale de companie preferate de mulți adulți sau copii, în special datorită conformației ciudate și vioiciunii pe care o manifestă când sunt mici. În ultimii 25-30 de ani, o extindere largă au avut-o diferite specii ale Subfamiliei Deirochelynae, în special țestoase din genul Chrysemys (cea mai cunoscută și răspândită fiind C. picta) și cele din genul Trachemys (în special subspeciile de T. scripta - T. scripta scripta și T. scripta elegans), cunoscute ca țestoase cu tâmple roșii, țestoase cu tâmple galbene sau țestoase californiene. Întreținerea în captivitate a acestor specii provenite din regiunile continentale americane nu s-a corelat cu asigurarea unor condiții corespunzătoare de viață, în special cu amenajarea și organizarea corectă a unor terarii sau acvaterarii care să ofere parametrii de confort sau cel puțin o temperatură adecvată și o dietă corespunzătoare. Cel mai frecvent, lipsa cunoștințelor despre biologia acestor specii sau cunoașterea parțială a ecobiologiei lor a condus la apariția unor grave erori de întreținere în captivitate, care în timp s-au transformat în patologie specifică, cel mai frecvent fiind dezvoltate deficiențe metabolice grave. Aceste specii provin din zona centrală și sudică a Americii de Nord și până în regiunile de nord și centru ale Americii de Sud, regiuni geografice cu climă caldă și caracterizate de două sezoane principale. În zona europeană, aceste țestoase au fost frecvent asimilate ca necesități cu emidinele autohtone și în special cu cele din genul Emys (cea mai cunoscută fiind E. orbicularis), specii care prezintă mari diferențe fiziologice și anatomice, având cu totul alte necesități față de condițiile oferite de regiunile cu climă temperată.
Juvenilii de Trachemys și Chrysemys care ajung în punctele de vânzare din magazine sunt ținuți în condiții care nepotrivite cu necesitățile lor metabolice (pH dezechilibrat, schimburi frecvente de apă, densitate populațională mare, care favorizează acumularea de amoniac și hidrogen sulfurat). În multe situații se asigură temperaturi mai ridicate decât intervalul de confort, pentru a obliga broscuțele să fie agitate și să manifeste o vioiciune exagerată cu mișcări ample care atrag cumpărătorii. La acestea se adaugă și hrănirea cu produse liofilizate sau formule de premixuri peletate sau granulate care (în special la vârstele mici) determină dezechilibre digestive și favorizează dereglări metabolice evolutive cu consecințe patologice grave atât pe termen scurt, cât și pe intervale de timp mari. De multe ori, dereglările produse la vârste mici încep să prezinte semne clinice după mai multe luni, fiind bine cunoscută și descrisă de mulți autori capacitatea compensatorie uriașă a acestor specii și a chelonienilor în general. Afectarea generală a metabolismului are consecințe directe asupra statusului imunitar și a capacității organismului de a face față agresiunilor infecțioase. Diferite specii de virusuri sau bacterii care în mod natural nu afectează emidinele reușesc în aceste condiții să producă, singure sau asociate, stări morbide care în multe situații evoluează agravant și chiar letal.
Țestoasele acvatice sunt frecvent purtătoare de bacterii patogene Gram-negative, fără a dezvolta stări clinice și aparent fără a prezenta afectări ale organelor sau țesuturilor unde sunt cantonate acestea.
Diferite specii de Yersinia spp. sunt izolate relativ frecvent de la țestoase acvatice clinic sănătoase, la acestea asociindu-se Mycobacterium spp., Pasteurella spp. și Pseudomonas spp., în special pe țesuturile tractului digestiv sau respirator. De asemenea, există mai multe studii care relevă că 38% până la 47% dintre emidinele întreținute în captivitate sunt purtătoare de Salmonella spp., în special la nivel digestiv.
Întreținerea în captivitate în condițiile amintite permite acestor bacterii să atace țesuturile sau organele în care sunt cantonate, să se multiplice, să genereze faze bacteriemice și să se răspândească prin intermediul torentului circulator în alte organe, unde alterează funcția acestora și determină distrucții tisulare, apoi încep să dezvolte faze septicemice, cu afectarea gravă a structurii vaselor sangvine, în final determinând moartea. Fazele patogenetice și manifestările clinice prezintă diferențe în funcție de asocierile bacteriene care capătă valențe de patogenitate.
Asocierile dintre Yersinia spp. și Vibrio spp. determină forme septicemice lente, în care inițial se constată inapetența, țestoasele stau retrase și preferă zonele întunecate. Această fază poate dura o săptămână sau mai multe săptămâni. Ulterior se constată scăderi ale densității și durității plăcilor de la nivelul plastronului, tendința de exfoliere a straturilor de solzi, inclusiv a celor imaturi („năpârlire” excesivă), iar la nivelul joncțiunilor dintre plăci sau chiar sub solzi se pot constata hemoragii (peteșii) de culoare roșu-aprins până la nuanțe albastru-violacee, uneori întreaga suprafață a plastronului devenind marmorată cu nuanțe vineții.
În cazul suprapunerilor de Aeromonas spp., manifestările sunt mai intense, se constată afectarea hemoragică atât a plastronului, cât și a carapacei, ambele prezentând o scădere evidentă a durității. Apar hemoragii cutanate (peteșii, sufuziuni), în special în regiunea pericloacală și zona cervicală distală. Frecvent, Aeromonas spp. determină alterarea funcției renale, produce blocaj renal și exitus înainte ca manifestările hemoragice să devină evidente.

În asocierile cu Pseudomonas spp. sau germeni Gram-pozitivi (de regulă, Corynebacterium spp. și mai rar tulpini coagulazo-pozitive de Staphylococcus spp.), se constată o reducere a durității (înmuierea) doar la nivelul carapacei, în timp formându-se două adâncituri simetrice dorso-caudale, cu apariția de hemoragii cutanate evidente (echimoze, peteșii) în toată regiunea posterioară. Frecvent în septicemia cu aceste specii (în special cu Corynebacterium spp.) apar abcese hepatice și fragilitate vasculară accentuată, cu producerea de hemoragii interne. Consecutiv acumulării de sânge în cavitatea generală, apar compresiuni pe sacii respiratori, dificultăți respiratorii care evoluează agravant și chiar sincopă cu exitus.

Asocierile cu Salmonella spp. se manifestă în primele faze prin inapetență, diaree cu fecale mucoase verzui-închise sau negricioase, dificultăți respiratorii, după o perioadă de câteva săptămâni putându-se constata „înmuierea” carapacei și a plastronului, dar fără exfolieri de solzi, în fazele avansate producându-se hemoragii interne spontane și exitus. Asocierea cu Mycoplasma spp. determină în primele faze manifestări respiratorii (dispnee și expulzarea de mucozități sau formarea de spumozități nazale mai evidente în timpul efortului expirator). Aceasta evoluează în mai multe săptămâni, perioadă în care colonizează spațiul mezobronșial și sacii aerieni. În fazele septicemice se constată „înmuierea” evidentă a plastronului și, mai rar, o reducere a durității carapacei, hemoragii cutanate punctiforme, edem gelatinos în regiunea cervicală, care uneori blochează posibilitatea retragerii capului, țestoasa căpătând aspect de animal împăiat. Moartea survine, de regulă, în urma hemoragiilor interne spontane.

Conduita terapeutică este complexă în toate cazurile. În primele faze trebuie susținute funcțiile de bază și volemia. Se intervine prin administrarea intracelomică sau epicelomică de fluide complexe, asocieri de soluții de rehidratare cu aminoacizi, complexuri minerale și soluții trofice. În situația manifestării inapetenței pe termen lung, se poate recurge la hrănirea forțată prin sondă intragastrică, administrând piureuri diluate din pește (în special, ficat de pește) sau complexuri proteice rehidratate. Fluidoterapia se poate face la volume de 15-25 ml/kg/zi, în funcție de specie și de vârstă. Este importantă asigurarea antibioterapiei, care trebuie să țină cont în primul rând de asocierea bacteriană, în special dacă sunt germeni Gram-pozitivi sau Gram-negativi. Alegerea antibioticului sau a combinației de antibiotice (eventual asociate cu chimioterapice) va ține cont de compatibilitatea cu specia de țestoasă, precum și cu vârsta acesteia. Administrările se pot face subcutanat (în faldurile cervicale laterale) sau intramuscular (în membrele posterioare), la intervale care se vor corela cu specia, activitatea metabolică și temperatura ambientală. În evoluțiile respiratorii se pot face lavaje nazale cu soluții saline și antibiotice, pentru a elimina detritusurile și aglomerările de mucus, prevenind formarea spumozităților care pot fi fatale. Toate manipulările și manoperele terapeutice vor fi efectuate cu mare atenție, pentru a nu crește riscul hemoragic. Pe toată durata tratamentului nu se vor face schimburi de apă, iar temperatura se va corecta la intervalul optim de confort care trebuie asigurat în funcție de specie. La revenirea apetitului, hrănirea se va face ponderat, la intervale mari de timp, pentru a limita riscul hemoragiilor interne.

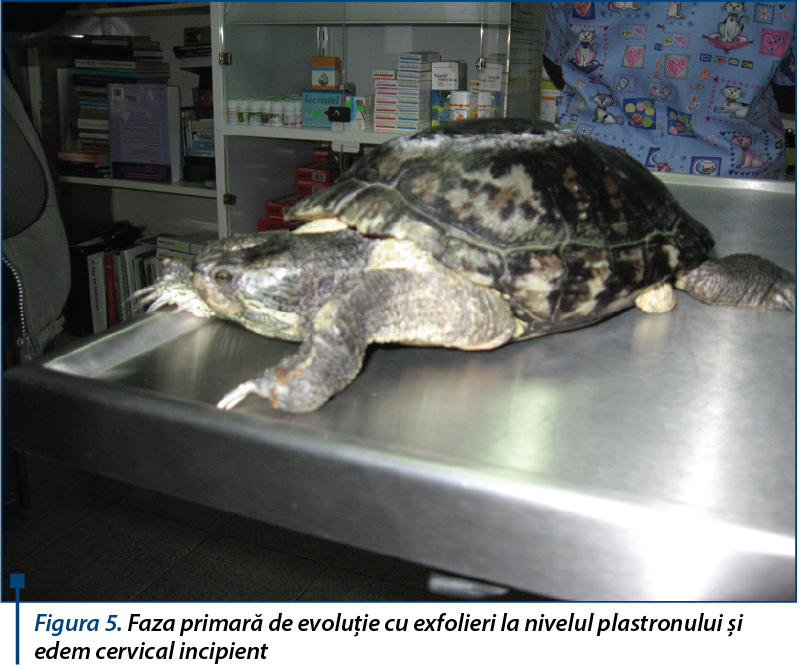

Hipovitaminozele evoluează grav atât la țestoasele acvatice, cât și la cele terestre. Hipovitaminoza A este una dintre bolile metabolice care evoluează tot mai frecvent la țestoasele acvatice crescute în captivitate. Este o boală specifică țestoaselor reproduse artificial și care după ecloziune sunt cazate în spații inadecvate, fiind hrănite parcimonios, cu rații dezechilibrate nutritiv. A fost prima dată descrisă la specii ale genurilor Chrysemys și Trachemys, popular numite țestoase californiene sau țestoasa cu tâmple roșii. La alte specii de chelonieni acvatici sau tereștri, hipovitaminoza A nu a fost diagnosticată decât sub forma unor cazuri excepționale, la animale subnutrite sau menținute ani de-a rândul în condiții de mediu total improprii. În general, la țestoasele terestre (majoritar vegetariene) care consumă imediat după ecloziune plante bogate în caroteni se consideră că este imposibilă hipovitaminoza A. La țestoasele californiene (genurile Chrysemys și Trachemys), după ecloziune puii sunt transmiși destul de repede către centrele de comercializare, transportul și apoi păstrarea în punctele de vânzare însumând perioade în care condițiile de mediu (lumină, temperatură, pH-ul apei, concentrația de amoniac și hidrogen sulfurat din apă) nu sunt asigurate la nivel optim. Condițiile defavorabile de mediu sensibilizează și dereglează metabolismul. În cazul asocierii mediului defavorabil cu o nutriție dezechilibrată (administrarea de hrană condiționată), în majoritatea situațiilor conduce la alterarea metabolismului, malabsorbție și hipovitaminoză A, cu consecințe patologice grave. Nivelul scăzut de vitamină A în hrană afectează în primul rând epiteliile, determinând hipercheratoză și metaplazie scuamoasă. În general, chelonienii au o rezistență foarte mare la condițiile de mediu defavorabile, manifestând clinic tardiv deficiențele metabolice. Asigurarea unei diete dezechilibrate și sărace în vitamina A conduce la încetinirea ritmului de creștere și la subdezvoltare corporală, constatare care a permis formularea unei concluzii greșite: această hrănire este favorabilă obținerii unor țestoase de talie mică, ce permit întreținerea în spații reduse, fiind extrem de comode proprietarilor care vor astfel de animale de companie. De multe ori, veterinarii recomandă hrănirea, chiar a puilor de țestoase, cu cantități reduse de hrană, pe cât posibil hrană sintetică. Consecințele acestei hrăniri sunt devastatoare pe termen lung pentru țestoase. Modificările epiteliale afectează toate țesuturile și organele, cu consecințe grave mai ales asupra mucoaselor oculare, digestive, respiratorii și genito-urinare. În multe cazuri sunt afectate chiar epiteliile glandelor endocrine și exocrine, determinând disfuncții secretorii și excretorii. Epiteliile normale sunt treptat înlocuite cu epitelii modificate, care se descuamează continuu. Țesuturile descuamate se aglomerează frecvent în diferite canale sau canalicule (pancreatic, renal, oculo-nazal), formând dopuri care blochează tranzitul parțial sau total. La nivelul sacilor conjunctivali se acumulează detritus celular care blochează cele două canale lacrimale (canalul glandei antero-mediale Harder și canalul glandei postero-laterale). Glandele lacrimale cresc în volum, determinând edem palpebral (blefaro-edem pseudoalergic), ușor de identificat clinic din cauza măririi exagerate a pleoapelor. Evoluția la nivel ocular este agravantă: apar blefaro-spasm (globul ocular este mascat complet de pleoapele puternic tumefiate), blefarită, conjunctivită, rinită cu dificultate respiratorie (dispnee, respirație șuierătoare, respirație bucală, respirație agonică). Complexitatea semnelor concentrate pe zona oculo-nazală conduce frecvent la stabilirea unui diagnostic fals de blefaro-conjunctivită infecțioasă și instituirea greșită a unei terapii antiinfecțioase (fie topică - colire sau unguente oftalmice, fie antibioterapie generală - uneori injectarea zilnică a țestoasei chiar pe perioade excesiv de lungi), fără însă a se înregistra succes. În formele grave de hipovitaminoză A se pot produce infecții ale urechii mijlocii, cu acumularea de detritusuri și formarea de abcese temporale, vizibile la exterior, cu conținut steril. La femelele adulte, formele avansate de hipovitaminoză A pot fi o cauză a retenției de ouă, în majoritatea situațiilor acestea însă se resorb și sunt reintegrate în circuitul metabolic. În cazul instituirii tardive a unei terapii adecvate sau în lipsa terapiei, modificările avansează și sunt afectate grav funcțiile hepatice și renale. Se constată distrofie renală, incapacitate excretorie și distrofie grasă hepatică. În unele situații, hipovitaminoza A conduce la dereglarea metabolismului fosfo-calcic și evoluează cu distrofie osoasă: hipomineralizarea matricei osoase, fragilizarea oaselor (oase casante sau oase de „sticlă”), înmuierea armăturii osoase a carapacei și plastronului (uneori pot apărea șanțuri și delimitări evidente ale plăcilor osoase, cu exfolierea masivă a solzilor chitinoși de acoperire). În fazele finale se constată fragilizarea vaselor sangvine și ruperea spontană, producându-se hemoragii localizate sau generalizate. Pe suprafața carapacei și a plastronului se observă, sub solzi, peteșii sau sufuziuni care, de regulă, conduc la ideea producerii și a unor hemoragii interne. Dereglarea metabolică este uneori evidențiată clinic prin edem sero-gelatinos generalizat (cervical, membre, apertura toracică, pericloacal).
Diagnosticul este relativ simplu și se poate stabili numai pe baza semnelor clinice care sunt evidente sau uneori chiar frapante. Edemul palpebral (care se manifestă primar) apare încă de la început și converge spre blefaro-spasm și blefarită edematoasă. În majoritatea situațiilor, țestoasele încetează hrănirea (refuză chiar alimentele preferate) și frecvent elimină fecale diareice verzui coafate în mucus. În fazele avansate, pe lângă modificările oculare evidente, se constată simptomatologia respiratorie, hemoragii localizate la nivelul plastronului și edemul sero-gelatinos subcutanat generalizat. Conduita terapeutică implică două direcții de acțiune. Se intervine medicamentos prin administrarea injectabilă a două doze de vitamina A (5000 UI/kg) la interval de două săptămâni. În cazurile grave se poate administra încă o doză de 1500-2000 UI/kg la 3-4 săptămâni de la a doua administrare. În cazul abceselor temporale (unice sau bilaterale) se intervine prin incizia directă a pielii și chiuretarea zonei (în majoritatea cazurilor presiunea internă asigură evacuarea spontană la incizarea pielii, eliminându-se un conținut consistent, cazeos, de culoare alb-gălbuie), apoi se badijonează local cu betadină și se pudrează cu antibiotice sau sulfamide. Pielea nu se suturează, asigurând evacuarea completă a secrețiilor. După intervenție, țestoasa nu se introduce în apă 48-72 de ore, perioadă în care doar se pulverizează apă cutanat, pentru a preveni deshidratarea. În cazul asocierii cu osteodistrofia metabolică, se administrează injectabil și o doză unică de 500 UI/kg de vitamină D, asociată cu săruri de calciu (se recomandă administrarea a 4-5 doze de calciu gluconic - 50 mg/kg, injectate i.m. la interval de o săptămână). O greșeală frecventă în osteodistrofia metabolică primară sau asociată hipovitaminozei A este injectarea zilnică a unor doze mari (exagerate uneori) de calciu sau asocieri de calciu-magneziu. Excesul de calciu ionic se excretă renal, ajungând în tubii uriniferi blocați de celulele epiteliale descuamate, formând blocuri minerale care conduc la blocaj renal și exitus. În multe cazuri, după prima administrare de vitamina A, la 2-3 săptămâni apetitul revine, fiind recomandată administrarea orală a unor complexuri vitamino-minerale (1 doză săptămânală timp de 2-3 luni, apoi 1 doză pe lună). O formă bună de vitamine A și D naturale o reprezintă uleiul din ficat de cod, acceptat ușor de țestoase la administrările orale și utilizat metabolic foarte bine.




A doua direcție terapeutică o reprezintă asigurarea unui mediu de viață optim. Apa din bazin trebuie să aibă un pH neutru sau chiar slab alcalin, similar pH-ului apelor stagnante în care au evoluat aceste specii și care le condiționează strict metabolismul. Temperatura apei în perioada de tratament va fi de 21-22 °C (maximum 23 °C), asigurând un metabolism mai lent și o exfoliere minimală a epiteliilor, diminuând în acest fel distrucțiile și riscul hemoragic. Este recomandabil ca apa să fie curățată prin filtrare, evitându-se pe cât posibil schimburile de apă (se poate adăuga apă proaspătă pentru a înlocui apa evaporată, iar la nevoie se poate schimba maximum 1/5 din volumul de apă). Pe durata tratamentului se va face hrănirea cu pește integral (pești mici întregi sau felii de pește), utilizând toate componentele peștelui: oase, piele, solzi, musculatură, viscere. Peștele integral asigură toate trofinele necesare, în rapoarte optime de utilizare digestivă, asigurând un metabolism normal. Este recomandabilă hrănirea țestoaselor acvatice cu rații formate majoritar din pește integral, prevenind hipovitaminoza A și alte boli metabolice.
Osteodistrofia metabolică (ODM) - sau hiperparatiroidismul nutrițional secundar - este determinată de condițiile de mediu necorespunzătoare, spații inadecvate, țestoasele având rații dezechilibrate nutritiv și uneori chiar furaje care nu fac parte din dieta uzuală a acestor specii. Este o boală secundar-nutrițională, care apare foarte rar sau doar excepțional la țestoasele sălbatice care preiau din hrana animală un raport mineral optim și cantitățile suficiente de vitamină D metabolizabilă pentru dezvoltare. La țestoasele terestre, dereglarea metabolică este uneori evidențiată clinic prin edem sero-gelatinos generalizat (cervical, membre, apertura toracică, pericloacal).
Diagnosticul este relativ simplu, prin paleta largă de modificări care determină simptomatologie evidentă. Frecvent, proprietarii se prezintă cu țestoase care au modificări osoase evidente sau fracturi spontane, consecutiv osteodistrofiei generalizate. Demineralizarea oaselor avansează uneori până la fragilizarea matricei, cu apariția oaselor casante (oase „de sticlă”). În majoritatea cazurilor, osteodistrofia metabolică se asociază cu o transformare gravă a musculaturii (periostită fibroasă care degenerează în miozită distrofică fibroasă sau chondro-fibroasă), evidențiată ca îngroșare (chiar aspect balonizant) a musculaturii membrelor sau mandibulare. Modificările osoase conduc la deformări ale oaselor lungi (radio-ulnar, humerus, femur sau fibulă) și chiar la deformări grave ale coloanei vertebrale (scolioză, lordoză). În unele cazuri s-a constatat fracturarea vertebrelor sacro-lombare, cu cifozarea zonei. Modificările osoase, ligamentare și musculare conduc la adoptarea de posturi anormale (uneori chiar ciudate), cu ridicarea exagerată a capului în mers, mers înțepenit, extensie forțată a membrelor, ridicare exagerată a capului, contracții spontane sau poziție de „statuie” (tetanie hipocalcemică). Am constatat la multe cazuri de osteodistrofie metabolică asocierea în faze avansate a prolapsului cloacal parțial, ușor reponibil, determinat de hipocalcemia severă.
Unele cazuri de osteodistrofie mandibulară cu gonflarea maseterilor (miozită fibroasă) au rămas cu sechele în dezvoltarea structurii anatomice, la vârsta adultă prezentând brevignatism inferior avansat. Modificările mandibulare se corelează cu dificultățile în hrănire, astfel încât țestoasa devine pentru toată viața dependentă de mărunțirea peștilor. Intervenția terapeutică include două direcții: intervenția de urgență pentru simptomatologia acută și refacerea mediului de viață concomitent cu restabilirea hrănirii cu rații echilibrate nutrițional. O greșeală frecventă în aceste situații este administrarea injectabilă a unor doze mari de calciu gluconic sau gluconolactat de calciu și magneziu. Imposibilitatea metabolică de utilizare a calciului, precum și necorelarea raportului fosfo-calcic conduc la excreția renală intensă, uneori cu blocarea renală sau distrofie renală severă. În toate cazurile, după evaluarea radiografică generală (o radiografie a ansamblului scheletic) prin care se evidențiază gradul de demineralizare, se intervine prin administrarea de vitamină D3 (doze de 300-400 UI/kg) intramuscular. Metabolismul fosfo-calcic se susține prin administrarea orală a unor doze mici de calciu gluconic (50 mg/kg) împreună cu un complex fosfat multimineral (30-35 mg/kg) și un complex polivitaminic. Este recomandabil ca doza zilnică să fie divizată în două administrări (la interval de 10-12 ore), facilitând absorbția digestivă și prevenind spasmele intestinale determinate de ionii de calciu. Administrarea complexului vitamino-mineral se face 3-4 săptămâni, asigurând la fiecare 10 zile o doză de 300-400 UI de vitamină D3/kg, injectate intramuscular.
O bună reglare a metabolismului fosfo-calcic se asigură prin administrarea de calcitonină (similară Salmon Calcitoninei utilizate în osteoporoza umană). Se administrează două doze a 50 UI calcitonină/kg intramuscular, la interval de două săptămâni. Administrarea trebuie făcută numai după evaluarea nivelului de calciu plasmatic, în caz contrar se induce tetanie hipocalcemică, uneori cu efect letal. După intervenția de urgență, care reprezintă de fapt stabilizarea metabolismului fosfo-calcic, se trece la intervenția de durată: refacerea condițiilor de mediu și hrănirea cu rații echilibrate.

Infecții generalizate sau septicemii consecutive dezechilibrelor metabolice - afectarea generală a metabolismului are consecințe directe asupra statusului imunitar și a capacității organismului de a face față agresiunilor infecțioase. Diferite specii de virusuri sau bacterii care în mod natural nu afectează emidinele reușesc în aceste condiții să producă, singure sau asociate, stări morbide care, în multe situații, evoluează agravant și chiar letal. Virusurile constituie o categorie relativ restrânsă și mai frecvent acționează ca factori secundari, complicând patologia în bacterioze sau uneori suprapunându-se în probleme metabolice cronice. Sunt și virusuri care acționează primar, generând entități morbide bine conturate, așa cum sunt herpesvirozele „de primăvară” (trecerile bruște de la sezoane reci la sezoane calde fără o perioadă de adaptare într-un terariu de tranziție), herpesvirozele generalizate la indivizii extenuați după sezoanele de reproducție sau cu metabolism dereglat care stau retrași, preferă locurile ascunse și refuză chiar și combinațiile vegetale preferate. Diagnosticarea precoce permite stabilirea unei conduite terapeutice adecvate, înainte ca leziunile să se agraveze. De regulă, modificările mucoasei bucale și apariția unei salive gelatinoase, asociate cu sensibilitate bucală și creșterea exagerată a valvulei maxilare, asigură prezumția diagnostică.
Diagnosticul tardiv presupune în unele situații detectarea și a unor factori etiologici bacterieni sau micotici care complică leziunile și simptomatologia. În aceste situații se va recurge la administrarea de antivirale pe cale generală (acyclovir în doze de 60-80 mg/kg) asociate cu antibiotice sau chimioterapice, pentru a combate infecțiile secundare.
Există și viroze în care intervenția terapeutică este iluzorie. Atât în herpesviroze, iridoviroze, cât și în paramyxoviroze, diagnosticul se stabilește histologic. Este importantă diferențierea manifestărilor clinice, în general de stomatite, rinite și gastroenterite evolutive, de iatropatiile generate prin administrarea de antiinflamatoare cortizonice în urma cărora apar modificări majore la nivelul tractusului digestiv superior (în special stomatite). În paramyxoviroză se înregistrează atât modificări respiratorii, cât și nervoase, histologic constatându-se incluzii eozinofilice în pulmon și creier, intensitatea acestor manifestări și frecvența de apariție fiind mai mare la testudinidele care nu au fost introduse la hibernat.
Diferite specii bacteriene sunt izolate relativ frecvent de la țestoase acvatice clinic sănătoase, la acestea asociindu-se Mycobacterium spp., Pasteurella spp. și Pseudomonas spp., în special pe țesuturile tractusului digestiv sau respirator. De asemenea, există mai multe studii care relevă că 42% până la 57% din testudidele întreținute în captivitate sunt purtătoare de Mycobacterium spp. și Pasteurella spp. în special la nivel respirator. În captivitate se diagnostichează relativ frecvent boala tractusului respirator superior (BTRS), în multe situații evoluția fiind letală. Conduita terapeutică este complexă în toate cazurile. În primele faze trebuie susținute funcțiile de bază și volemia. Se intervine prin administrarea intracelomică sau epicelomică de fluide complexe, asocieri de soluții de rehidratare cu aminoacizi, complexuri minerale și soluții trofice. În situația manifestării inapetenței pe termen lung, se poate recurge la hrănirea forțată prin sondă intragastrică, administrând piureuri diluate din combinații de vegetale. Fluidoterapia se poate face la volume de 15-25 ml/kg/zi, în funcție de specie și de vârstă. Este importantă asigurarea antibioterapiei, care trebuie să țină cont în primul rând de asocierea bacteriană, în special dacă sunt asociați și alți germeni Gram-pozitivi sau Gram-negativi. Alegerea antibioticului sau a combinației de antibiotice (eventual asociate cu chimioterapice) va ține cont de compatibilitatea cu specia de țestoasă, precum și cu vârsta acesteia. Administrările se pot face subcutanat (în faldurile cervicale laterale) sau intramuscular (în membrele posterioare), la intervale care se vor corela cu specia, activitatea metabolică și temperatura ambientală. În evoluțiile respiratorii se intervine și prin lavaje nazale cu soluții saline și antibiotice, pentru a elimina detritusurile și aglomerările de mucus, prevenind formarea spumozităților sau a altor complexe obstructive care pot fi fatale.
Asocierea Pseudomonas spp. sau a Pasteurella testudinis cu Aeromonas spp. sau Klebsiella spp. determină și simptomatologie respiratorie, iar la nivelul mucoasei oro-faringiene apar eroziuni și depozite vâscoase abundente, care uneori pot conduce la obliterare și asfixie. Atrage atenția dispneea și refuzul hranei, iar la examinarea clinică a zonei oro-faringiene sunt evidente modificările mucoasei și uneori chiar prezența de stomatite ulcerative, necrotice sau hemoragice. Pseudomonozele evoluează cu precădere la schimbările de sezon, în urma hibernărilor defectuoase și la pui în primul an de viață (când sunt și transformări morfofiziologice importante).
Este importantă intervenția rapidă și în special menținerea hidratării (administrarea intracelomică în urgență de fluide complexe circa 15-25 ml/kg GV/zi). Pentru reechilibrarea hidro-electrolitică de durată și pentru hrănire se vor face hrăniri prin sonda intragastrică cu fluide nutritive complexe (jumătate din volumul gastric al individului administrat la 4-5 zile). Antibioterapia va ține cont de rata metabolică, temperatura ambientală (pentru majoritatea speciilor fiind recomandat intervalul 29-30°C) și farmacodinamica substanței utilizate. În cazurile cu refuz de hrană total se vor administra i.m., iar acolo unde indivizii acceptă hrănirea este de preferat administrarea orală (în hrană), care asigură absorbție lentă și titru ridicat pe o perioadă mai lungă. Administrarea orală este de preferat și în stomatitele cu depozite gelatinoase și eroziuni la nivelul mucoasei. În aceste situații este recomandabilă asocierea metronidazolului sub formă de pensulații sau badijonări, după debridarea riguroasă.
O patologie diferită apare în infecțiile cu Escherichia coli sau specii de Salmonella spp. și Clostridium spp. Se constată clinic enterite sau gastroenterite, afecțiuni respiratorii (în asocierile cu Clostridium spp.) sau afecțiuni ale tractusului urogenital inferior (în asocierile cu Escherichia coli). Unii autori descriu și modificări tegumentare severe datorate formelor septicemice la care se asociază Pasteurella testudinis. În toate aceste situații este recomandabilă antibioterapia sistemică și topică, cu asocieri de antibiotice și chimioterapice cu spectru larg, pentru a preveni infecțiile secundare. În formele septicemice este importantă supravegherea medicală, pentru a preveni crizele asfixice (asigurarea de lavaje bucale periodice cu soluții saline asociate cu antibiotice și chimioterapice) și pentru a interveni rapid în crizele tetanice.
Dintre bolile cu etiologie micotică, cel mai frecvent sunt diagnosticate dermatitele cu evoluție cronică. În general, dermatitele micotice evoluează localizat (afectarea unor zone circumscrise cu contur relativ regulat) și trebuie diferențiate de dermatitele veziculoase cu etiologie bacteriană determinate de Pseudomonas spp. sau Aeromonas spp.
Dermatitele micotice nu au tendințe expansive la testudinide, iar administrarea topică de produse cu fluconazol sau clotrimazol câteva săptămâni va remedia situația. Se consideră că boala s-a remis atunci când pielea se cicatrizează complet.
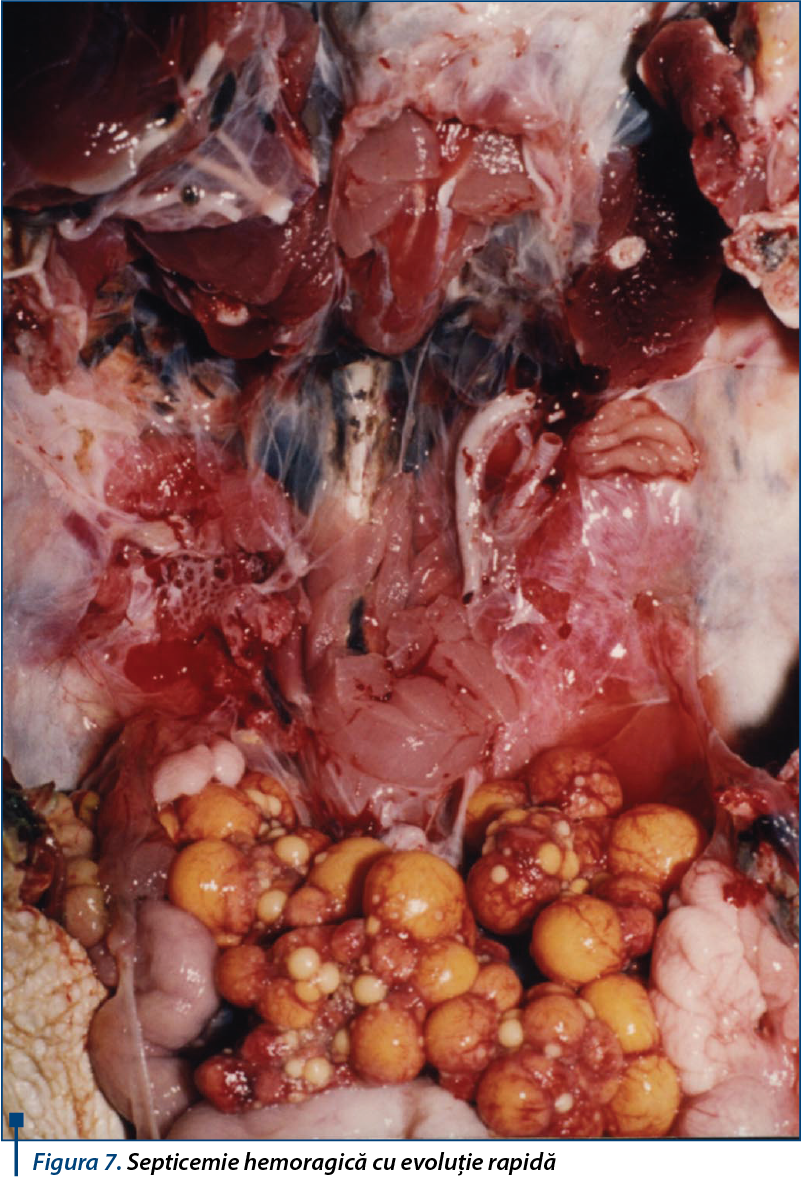
Țestoasele acvatice sunt frecvent purtătoare de bacterii patogene Gram-negative, fără a dezvolta stări clinice și aparent fără a prezenta afectări ale organelor sau țesuturilor unde sunt cantonate acestea. Există mai multe studii care relevă că 38% până la 47% dintre emidinele întreținute în captivitate sunt purtătoare de Salmonella spp., în special la nivel digestiv. Întreținerea în captivitate în condițiile descrise anterior permite acestor bacterii să atace țesuturile sau organele în care sunt cantonate, să se multiplice, să genereze faze bacteriemice și să se răspândească prin intermediul torentului circulator în diferite organe, unde alterează funcția acestora și apoi determină distrucții tisulare, încep să dezvolte faze septicemice cu afectarea gravă a structurii vaselor sangvine, iar în final determină moartea. Fazele patogenetice și manifestările clinice prezintă diferențe în funcție de asocierile bacteriene care capătă valențe de patogenitate. Asocierile cu Salmonella spp. se manifestă în primele faze prin inapetență, diareei cu fecale mucoase verzui-închise sau negricioase, dificultăți respiratorii, iar după o perioadă de câteva săptămâni putându-se constata „înmuierea” carapacei și a plastronului, dar fără exfolieri de solzi, în fazele avansate producându-se hemoragii interne spontane și exitus. Diferite specii de Yersinia spp. sunt izolate relativ frecvent de la țestoase acvatice clinic sănătoase, la acestea asociindu-se Mycobacterium spp., Pasteurella spp. și Pseudomonas spp., în special pe țesuturile tractusului digestiv sau respirator. Asocierile dintre Yersinia spp. și Vibrio spp. determină forme septicemice lente, în care inițial se constată inapetența, țestoasele stau retrase și preferă zonele întunecate. Această fază poate dura o săptămână sau mai multe săptămâni. Ulterior se constată scăderi ale densității și durității plăcilor de la nivelul plastronului, tendința de exfoliere a straturilor de solzi, inclusiv a celor imaturi („năpârlire” excesivă), iar la nivelul joncțiunilor dintre plăci sau chiar sub solzi se pot constata hemoragii (peteșii) de culoare roșu-aprins până la nuanțe albastru-violacee, uneori întreaga suprafață a plastronului devenind marmorată, cu nuanțe vineții. În cazul suprapunerilor de Aeromonas spp., manifestările sunt mai intense, se constată afectarea hemoragică atât a plastronului, cât și a carapacei, ambele prezentând o scădere evidentă a durității. Apar hemoragii cutanate (peteșii, sufuziuni), în special în regiunea pericloacală și în zona cervicală distală. Frecvent, Aeromonas spp. determină alterarea funcției renale, produce blocaj renal și exitus înainte ca manifestările hemoragice să devină evidente. În asocierile cu Pseudomonas spp. sau germeni Gram-pozitivi (de regulă, Corynebacterium spp. și mai rar tulpini coagulazo-pozitive de Staphylococcus spp.) se constată o reducere a durității (înmuierea) doar la nivelul carapacei, în timp formându-se două adâncituri simetrice dorso-caudale și apariția de hemoragii cutanate evidente (echimoze, peteșii) în toată regiunea posterioară. Frecvent, în septicemia cu aceste specii (în special cu Corynebacterium spp.) apar abcese hepatice și fragilitate vasculară accentuată, cu producerea de hemoragii interne. Consecutive acumulării de sânge în cavitatea generală, apar compresiuni pe sacii respiratori, dificultăți respiratorii care evoluează agravant și chiar sincopă cu exitus. Asocierea cu Mycoplasma spp. determină în primele faze manifestări respiratorii (dispnee și expulzarea de mucozități sau formarea de spumozități nazale mai evidente în timpul efortului expirator). Evoluează în mai multe săptămâni, perioadă în care colonizează spațiul mezobronșial și sacii aerieni. În fazele septicemice se constată „înmuierea” evidentă a plastronului și mai rar o reducere a durității carapacei, hemoragii cutanate punctiforme, edem gelatinos în regiunea cervicală, care uneori blochează posibilitatea retragerii capului, țestoasa căpătând aspect de animal împăiat. Moartea survine de regulă în urma hemoragiilor interne spontane. Conduita terapeutică este complexă în toate cazurile. În primele faze trebuie susținute funcțiile de bază și volemia. Se intervine prin administrarea intracelomică sau epicelomică de fluide complexe, asocieri de soluții de rehidratare cu aminoacizi, complexuri minerale și soluții trofice. În situația manifestării inapetenței pe termen lung, se poate recurge la hrănirea forțată prin sondă intragastrică, administrând piureuri diluate din pește (în special ficat de pește) sau complexe proteice rehidratante. Fluidoterapia se poate face la volume de 15-25 ml/kg/zi, în funcție de specie și de vârstă.
Este importantă asigurarea antibioterapiei, care trebuie să țină cont în primul rând de asocierea bacteriană, în special dacă sunt germeni Gram-pozitivi sau Gram-negativi. Alegerea antibioticului sau a combinației de antibiotice (eventual asociate cu chimioterapice) va ține cont de compatibilitatea cu specia de țestoasă, precum și cu vârsta acesteia. Administrările se pot face subcutanat (în faldurile cervicale laterale) sau intramuscular (în membrele posterioare), la intervale care se vor corela cu specia, activitatea metabolică și temperatura ambientală. În evoluțiile respiratorii se pot face lavaje nazale cu soluții saline și antibiotice, pentru a elimina detritusurile și aglomerările de mucus, prevenind formarea spumozităților, care pot fi fatale. Toate manipulările și manoperele terapeutice vor fi efectuate cu mare atenție, pentru a nu crește riscul hemoragic. Pe toată durata tratamentului nu se vor face schimburi de apă, iar temperatura se va corecta la intervalul optim de confort care trebuie asigurat în funcție de specie. La revenirea apetitului, hrănirea se va face ponderat, la intervale mari de timp, pentru a limita riscul hemoragiilor interne.
Bibliografie
2. J Chitty & A Raftery - Essentials of Tortoise Medicine and Surgery. Wiley Blackwell. p. 38. ISBN 978 1 4051 9544 7, 2013.
3. Chen, T., and K. Lue. 1998. Ecological notes on feral populations of Trachemys scripta elegans in northern Taiwan. Chelonian Conservation and Biology 3(1):87-90.
4. Frye F. – Reptile care: an atlas of diseases and treatments, vol I and II, Neptune City, NJ: TFH, 1991.
5. Jenkins J. – Medical managements of reptile patients. Compend Contin Educ Pract vet, June 1991.
6. Jakob Christensen-Dalsgaard, Christian Brandt, Katie L. Willis, Christian Bech Christensen, Darlene Ketten, Peggy Edds-Walton, Richard R. Fay, Peter T. Madsen and Catherine E. Carr - Specialization for underwater hearing by the tympanic middle ear of the turtle, Trachemys scripta elegans. Proceedings of the Royal Society B. The Royal Society. 279 (1739): 2816–2824, 2012.
7. Holz R. M., Holz P – Electrocardiography in anaesthetised red-eared sliders (Trachemys scripta elegans). Res Vet Sci 58:67-69, 2000.
8. H Mohan-Gibbons & T Norton - Turtles, tortoises and terrapins. Blackwell Publishing. ISBN 978 0 8138 0078 3, 2010.
9. Packard, G.C., J.K. Tucker, D. Nicholson, and M.J. Packard. 1997. Cold tolerance in hatching slider turtles (Trachemys scripta). Copeia 997(2):339-345.
10. Willer C. J., Lewbart G. A., Lemons C. – Aural abcesses in wild eastern box turtles from North Carolina: Aerobic Bacterial Isolates and distribution of lesions. J Herp Surg 13(2):4-9, 2003.
Articole din ediţiile anterioare
Actualizarea protocolului de diagnostic în leptospiroza canină
Prezenta lucrare se constituie într-o sinteză a datelor existente în literatura de specialitate cu privire la performanţele testelor de diagnos...
Abordarea clinică şi paraclinică a pacienţilor cu meningită-arterită steroid-responsivă (MASR)
Meningita-arterită steroid-responsivă (MASR) reprezintă o patologie inflamatorie a sistemului nervos central, frecvent întâlnită la tineretul canin...
Managementul urgenţelor oncologice veterinare
Situaţia de urgenţă în oncologie poate fi definită ca o afecţiune patologică determinată de evoluţia clinică a sindroamelor paraneoplazice cance...
Performanţele testelor de biologie moleculară în diagnosticul parvovirozei canine
Testele de biologie moleculară reprezintă cronologic cele mai noi și mai moderne tehnici de investigare, inclusiv pentru identificarea și caracteri...