Aromatase inhibitors (AIs) represent a class of oncological drugs used in the treatment of patients with hormonepositive breast cancer. As a result of the action they exert on the cancerous tissue, unlike their precursors (for example, tamoxifen), this class is considered to be the first-choice treatment in breast cancer for postmenopausal patients. Thus, due to the increased effectiveness, this study was intended to analyze the compliance and tolerability of patients from Iaşi city to this treatment, comparing the data thus obtained with a study conducted in 2021 in Wisconsin, USA. It should be noted that the patients who were included in the present study generally did not receive other oncological treatments, which determined the objective analysis of adverse reactions to AIs.
Complianţa şi tolerabilitatea pacientelor cu cancer de sân la administrarea inhibitorilor de aromatază
Compliance and tolerability of breast cancer patients to aromatase inhibitors administration
First published: 14 martie 2024
Editorial Group: MEDICHUB MEDIA
DOI: 10.26416/Farm.216.1.2024.9298
Abstract
Rezumat
Inhibitorii de aromatază (IA) reprezintă o clasă de medicamente oncologice utilizate în tratamentul pacientelor cu cancer mamar hormono-pozitiv. Ca urmare a acţiunii pe care aceştia o exercită, spre deosebire de precursorii lor, cum ar fi, de pildă, tamoxifenul, această clasă este considerată a fi
tratamentul de elecţie în cancerul mamar la pacientele aflate în perioada de postmenopauză. Astfel, datorită eficacităţii crescute, s-a dorit ca, prin studiul realizat, să se analizeze complianţa şi tolerabilitatea pacientelor din Iaşi la acest tratament, comparând datele astfel obţinute cu un studiu
desfăşurat în 2021 în Wisconsin, SUA. Este de menţionat faptul că pacientele care au fost incluse în studiul de faţă nu au primit, în general, alte tratamente oncologice, ceea ce a determinat analizarea obiectivă a reacţiilor adverse la IA.
Introducere
Cancerul de sân este cel mai întâlnit tip de cancer diagnosticat în Statele Unite ale Americii şi reprezintă a doua cauză de mortalitate, acest rezultat apărând ca urmare a complianţei scăzute la tratament a pacientelor(1). Cel mai frecvent subtip histologic al cancerului mamar, întâlnit în rândul femeilor, este reprezentat de cancerul de sân hormono-pozitiv(2). Astfel, terapiile endocrine au devenit foarte utilizate în eradicarea acestei patologii, întrucât creşterea, respectiv replicarea celulelor tumorale, este dependentă de semnalizarea estrogenică(3,4).
Menţinerea nivelului estrogenic este dependentă de vârsta de reproducere a pacientei. În premenopauză, 17β-estradiolul este sintetizat la nivelul ovarelor, exercitându-şi efectul asupra organelor-ţintă. La femeile aflate în postmenopauză, în schimb, funcţia ovariană dispare, estrogenii circulanţi scad, aceştia fiind sintetizaţi predominant în ţesuturile adipoase, precum şi în alte ţesuturi extragonadale(2). Tratamentul iniţial de elecţie în cancerul mamar, la femeile aflate în postmenopauză, a fost dominat de utilizarea tamoxifenului. Ulterior, ca urmare a apariţiei reacţiilor adverse severe, precum creşterea riscului de dezvoltare a cancerului endometrial şi a evenimentelor tromboembolice, complianţa pacientelor a scăzut(5).
Date fiind aceste constatări, s-a descoperit clasa de medicamente numită inhibitori de aromatază. Mecanismul de acţiune constă în inhibarea conversiei periferice a androgenilor la estrogeni, diminuând astfel creşterea tumorii estrogen-dependente(1). În urma transformării, estrogenul îşi exercită activitatea la nivelul ţesuturilor prin legarea de receptorii specifici de estrogen cu specificitate înaltă. Astfel, pentru eradicarea cancerului de sân, una dintre cele mai utilizate metode o reprezintă modularea ligandului sau a receptorilor specifici în cazul în care acesta este hormono-pozitiv(5). Reprezentanţii acesteia se subclasifică în IA nesteroidieni, cu mecanism reversibil, care au ca reprezentanţi anastrozolul şi letrozolul, şi în IA steroidieni, cu mecanism ireversibil, exemestanul fiind principalul reprezentant utilizat în terapia actuală, întrucât formestanul necesită administrarea intramusculară a substanţei, această cale de administrare fiind una dureroasă(3).
În general, IA reprezintă o clasă de medicamente bine tolerată. Totuşi, efectele secundare ale acesteia includ, cu precădere, simptome vasomotorii, precum şi simptome musculo-scheletale sau pierderi de masă osoasă(3). În cazul anastrozolului, cea mai întâlnită reacţie adversă este astenia, urmată de simptomele gastrointestinale, de bufeuri şi artralgii. Alte reacţii adverse includ apariţia erupţiilor cutanate uscate, a edemelor periferice, precum şi a sindromului flu-like (febră, frisoane şi mialgii). Spre deosebire de acesta, letrozolul prezintă ca reacţii adverse principale durerile musculo‑scheletale, artralgiile, urmate de simptome vasomotorii. Mai puţin frecvente sunt instalarea greţurilor, a anorexiei şi a vărsăturilor(6). O consecinţă a administrării letrozolului o reprezintă şi riscul de a dezvolta evenimente tromboembolice, dar şi creşterea transaminazelor, fapt dovedit cu precădere la pacientele cu boală metastazată. Exemestanul, IA steroidian, prezintă mai puţine reacţii adverse, dintre care cele mai frecvente sunt simptomele vasomotorii, precum şi simptomele musculo‑scheletale(7).
Astfel, dată fiind complianţa diferită la tratament a pacientelor cu cancer mamar, precum şi riscul de a dezvolta o multitudine de reacţii adverse în urma administrării inhibitorilor de aromatază, ne propunem să studiem complianţa unui grup restrâns de paciente din Iaşi la tratamentul oncologic administrat, precum şi tolerabilitatea acestuia.
Materiale şi metodă
În această analiză au fost selectate 100 de paciente voluntare, diagnosticate cu cancer mamar hormono-pozitiv, cărora li s-a prescris un inhibitor de aromatază şi care nu urmează, în acelaşi timp, alte tratamente ale căror reacţii adverse ar putea interfera cu cele generate de chimioterapie. Pacientele au fost intervievate când s-au prezentat în farmacie pentru eliberarea prescripţiilor medicale oncologice. Întrebările adresate s-au referit la: tolerabilitatea faţă de tratament, uşurinţa administrării tratamentului, evoluţia parametrilor biochimici în timpul administrării medicamentului, apariţia reacţiilor adverse. Sondajul s-a efectuat într-o farmacie comunitară din oraşul Iaşi, România, în perioada 1 ianuarie 2023 – 28 februarie 2023. Informaţiile obţinute au fost utilizate strict pentru această lucrare de cercetare şi respectă confidenţialitatea pacientelor.
Rezultate şi discuţie
Rezultatele obţinute în urma analizării datelor furnizate de către pacientele din Iaşi, în cadrul studiului desfăşurat la 100 de paciente voluntare, au fost comparate cu cele ale studiului din Wisconsin, realizat la 179 de subiecţi(1).
În rândul pacientelor s-a înregistrat administrarea anastrozolului, letrozolului şi a exemestanului. Din totalul pacientelor intervievate, 28% au primit anastrozol, 54% letrozol şi 18% exemestan, spre deosebire de pacientele din Wisconsin, cărora li s-a administrat cu precădere anastrozol (85% dintre acestea). Letrozol au primit doar 10%, iar exemestan, 5% dintre acestea.
Una dintre întrebările-cheie adresate pacientelor s-a axat pe tolerabilitatea la tratament, respectiv pe rezultatele analizelor. Astfel, s-a observat că, din totalul pacientelor cărora li s-a administrat anastrozol, 71% au avut rezultatul analizelor favorabil şi au continuat astfel tratamentul, iar la 29% s-au constatat creşterea transaminazelor, precum şi modificarea altor parametri biochimici. În cazul letrozolului, 63% dintre paciente au avut rezultatele bune, iar 37% îndoielnice, acestea din urmă necesitând o atenţie deosebită ulterioară. Pacientele cu exemestan au obţinut toate analizele în parametri optimi. Datele obţinute au fost centralizate în Figura 1.
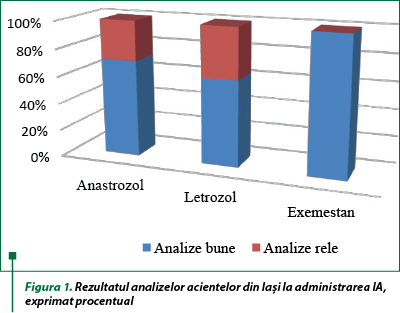
De asemenea, din totalul pacientelor cărora li s-a administrat anastrozol, 20 au prezentat efecte secundare în urma tratamentului în Iaşi, iar 125 în Wisconsin. Letrozolul a determinat reacţii adverse la 34 de paciente din Iaşi, respectiv la 15 din Wisconsin. În urma tratamentului cu exemestan, 14 paciente din Iaşi au prezentat efecte secundare şi şapte din Wisconsin. Astfel, exprimând procentual datele anterioare, am obţinut Figura 2.
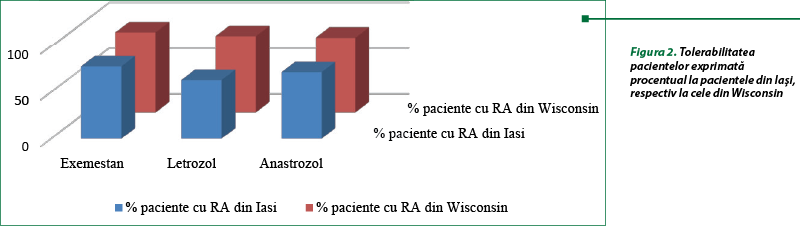
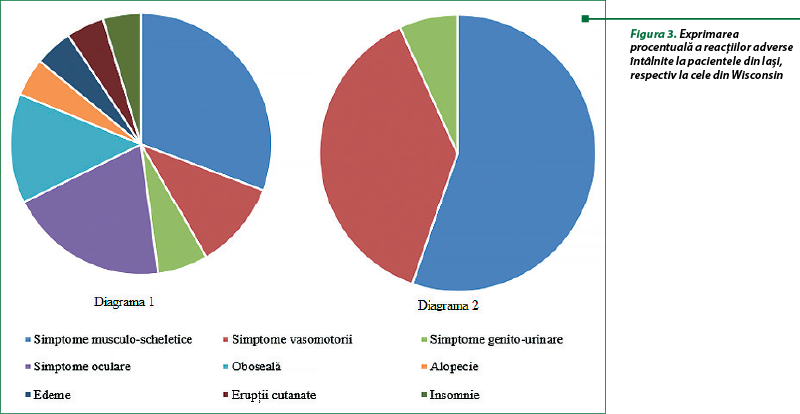
Odată determinat gradul de tolerabilitate al pacientelor aflate în studiul clinic, am analizat reacţiile adverse pe care acestea le resimt în urma administrării tratamentului. Astfel, 59% au prezentat simptome musculo‑scheletale, 38% simptome oculare (scăderea acuităţii vizuale, lăcrimare, senzaţia de corp străin), 26% oboseală, 21% simptome vasomotorii (bufeuri, transpiraţii), 12% simptome genito-urinare (uscăciunea mucoasei vaginale, candidoză), iar 9% alopecie, edeme periferice cu retenţie de apă, insomnie, precum şi erupţii cutanate.
Comparativ cu datele obţinute în urma aplicării metodei chestionarului la pacientele din Iaşi, în cazul celor din Wisconsin, 73% au prezentat simptome musculo‑scheletale, 50% simptome vasomotorii (transpiraţii, bufeuri), iar 9% simptome genito-urinare (uscăciune vaginală, incontinenţă urinară).
Astfel, în urma analizei complianţei şi tolerabilităţii la tratamentul cu inhibitori de aromatază ale pacientelor din Iaşi, atât individual, cât şi comparativ, cu rezultatele obţinute la pacientele din Wisconsin. Figura 3 ilustrează un număr mai mare de reacţii adverse la pacientele din Iaşi decât la cele din Wisconsin, precum şi o pondere diferită a acestora. De asemenea, molecula predominantă în prescripţiile acestora a fost, pe de o parte, letrozolul, în cazul studiului nostru, iar anastrozolul, în cazul celui din Wisconsin. Aşadar, conform analizei făcute şi a reacţiilor adverse întâlnite în literatură, se poate afirma faptul că tratamentul se alege în funcţie nu doar de clasa din care face parte, ci şi de profilul de siguranţă, de tolerabilitatea pacienţilor la apariţia eventualelor efecte adverse.
Concluzii
Ca orice tip de tratament, prescrierea acestuia constă în analizarea balanţei risc-beneficiu. Astfel, când vine vorba despre studierea complianţei şi tolerabilităţii pacienţilor la tratament, ne referim atât la obţinerea unor rezultate bune care să ajute la stagnarea şi/sau la eradicarea bolii, cât şi la menţinerea sau creşterea calităţii vieţii. Deşi amintite puţin în literatură, multe dintre reacţiile adverse ale IA, cum ar fi uscăciunea ochilor, lăcrimarea excesivă, senzaţia de corp străin la nivel oftalmic, respectiv scăderea acuităţii vizuale, au îngreunat viaţa de zi cu zi a pacientelor oncologice. S-a evidenţiat astfel balanţa risc-beneficiu a administrării inhibitorilor de aromatază, cu scopul de a reduce frecvenţa şi intensitatea reacţiilor adverse apărute la administrarea tratamentului.
Autor corespondent: Conf. univ. dr. Georgiana Atodiresei-Pavalache E-mail: georgianapavalache@gmail.com
Conflict de interese: niciunul declarat.
Suport financiar: niciunul declarat.
Acest articol este accesibil online, fără taxă, fiind publicat sub licenţa CC-BY.

Bibliografie
-
Ernst A, Flynn KE, Weil EM, et al. Aromatase Inhibitor Symptom Management Practices: A Retrospective Study. Clin Breast Cancer. 2021;21(1):e38-e47.
-
Molehin D, Filleur S, Pruitt K. Regulation of aromatase expression: Potential therapeutic insight into breast cancer treatment. Mol Cell Endocrinol. 2021;531:111321.
-
Chumsri S. Clinical utilities of aromatase inhibitors in breast cancer. Int J Womens Health. 2015;7:493-499.
-
Hamadeh IS, Patel JN, Rusin S, Tan AR. Personalizing aromatase inhibitor therapy in patients with breast cancer. Cancer Treat Rev. 2018;70:47-55.
-
Jacob L, Hadji P, Kostev K. Age-related differences in persistence in women with breast cancer treated with tamoxifen or aromatase inhibitors in Germany. J Geriatr Oncol. 2016;7(3):169-175.
-
Chumsri S, Howes T, Bao T, Sabnis G, Brodie A. Aromatase, aromatase inhibitors, and breast cancer. J Steroid Biochem Mol Biol. 2011;125(1):13-22.
-
Miron L. Manual de Medicaţie Oncologică pentru Clinicieni. 2022. Ediţia a doua. (Prior&Books, ed.)