Ectopic pregnancy is a gynecological emergency which in the absence of correctly and quickly diagnostic and an appropriate intervention can be fatal. The frequency of ectopic pregnancy varies between 0.58 and 1.3 %; in the last 20 years its prevalence increased by 60% due to the high incidence of acute pelvic inflammatory disease incorrectly diagnosed and treated as well as the increasing number of tubal surgical interventions. This article reviews the modern medical therapeutic approach of uncomplicated ectopic pregnancy.
Principii de tratament cu metotrexat al sarcinii extrauterine necomplicate
The treatment with Metotrexat of uncomplicated ectopic pregnancy
First published: 15 noiembrie 2014
Editorial Group: MEDICHUB MEDIA
DOI: 10.26416/Gine.3.2.2014.5089
Abstract
Rezumat
Sarcina extrauterină reprezintă o urgenţă ginecologică severă care, în lipsa unui diagnostic stabilit corect şi rapid, precum şi a unei intervenţii adecvate, poate fi fatală. Frecvenţa sarcinii extrauterine variază între 0.58 şi 1.3 %, în ultimii 20 ani, observându-se o creştere a acesteia cu 60% din cauza incidenţei ridicate a bolii inflamatorii pelvine acute incorect diagnosticate şi tratate, precum şi a creşterii numărului de intervenţii de chirurgie tubară. Articolul de faţă îşi propune trecerea în revistă a tratamentului medical, precum şi atitudinea terapeutică modernă în abordarea sarcinii extrauterine necomplicate.
Introducere
Sarcina extrauterină (ectopică) este definită ca implantarea sacului gestaţional în afara cavităţii uterine (ek=în afară; topos=loc)(1,2,3).
Istoric. Sarcina extrauterină a fost descrisă prima oară în anul 936 î.Hr. de un medic arab, Albucasis. În secolul al XVII-lea e menţionată de Mauriceau ca o posibilă complicaţie obstetricală. În 1883, Tait practica primele salpingectomii.
Incidenţă. În ţările occidentale, incidenţa sarcinilor extrauterine se situează între 1 şi 2%(2,27).
Sarcina extrauterină este principala cauză de mortalitate maternă, însă, datorită metodelor moderne de diagnostic şi tratament, mortalitatea cauzată de sarcina extrauterină este în scădere, astfel că în 1970 erau 35 decese/10.000 sarcini ectopice, 1989, 4 decese/10.000 sarcini ectopice la nivel mondial(2,3,5).
Factorii de risc ai sarcinii ectopice sunt numeroşi şi incomplet descoperiţi din care enumerăm: vârsta peste 35 de ani, tabagism cronic (peste 20 ţigări/zi)(7), antecedente patologice de salpingită sau TBC inaparente sau tratate ce pot determina stenoze inflamatorii(6), sechele ale intervenţiilor chirurgicale tubare-risc de recidivă pe bontul tubar restant în urma tratamentului operator conservator(4) malformaţii tubare (trompe hipoplazice, diverticul tubar).
Localizare (Bouyer, 2002)
-
tubară 95-96%: interstiţială (cornuală) 2-3%, istmică 12%, ampulară (70%)
-
cervicală <1%
-
ovariană 3%
-
peritoneală (abdominală) 1%
Cea mai rară formă de sarcină ectopică (sub 1%) este cea localizată la nivelul tranşei de histerorafie post-operaţie cezariană ST şi reprezintă o condiţie ameninţătoare de viaţă(9,10,11,12), incidenţa acesteia fiind în creştere din cauza creşterii numărului de operaţii cezariene.
Sarcina heterotopică reprezintă coexistenţa unei sarcini extrauterine cu o sarcină intrauterină şi apare exclusiv în cursul manevrelor de reproducere umană asistată(11).
Manifestare clinică
Sarcina extrauterină necomplicată (neruptă) se caracterizează prin triada simptomatică amenoree-metroragii-durere şi prin prezenţa unei tumori latero-uterine la tactul vaginal.
Sarcina extrauterină ruptă reprezintă o urgenţă chirurgicală (abdomen acut chirurgical) şi se manifestă prin durere bruscă „în pumnal” localizată în abdomenul inferior urmată de lipotimie.
Examene paraclinice
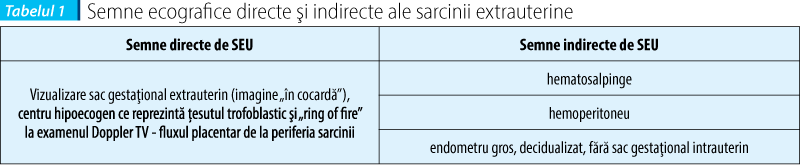
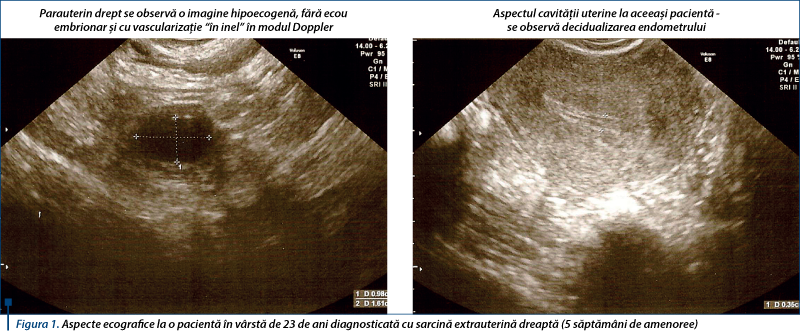
Ecografia transvaginală sau abdominală
Ultrasonografia, în special cu sonda intravaginală, permite vizualizarea sarcinii de la 6-7 săptămâni de amenoree(4,13,14).
Rezonanţa magnetică nucleară distinge masele anexiale şi diferenţiază conţinutul seros de cel hemoragic, dar nu poate preciza cauzele hemoragiei.
Explorări hormonale
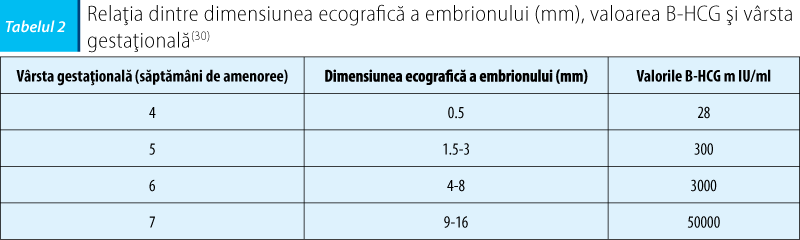
Dozarea cantitativă, în dinamică a b-HCG, glicoproteină secretată de sinciţiotrofoblast-apare în sângele matern la aproximativ 9 zile după peak-ul ovulator al LH. Valorile fracţiunii b a HCG se dublează din 48 în 48 ore în prima lună de sarcină(15,16).
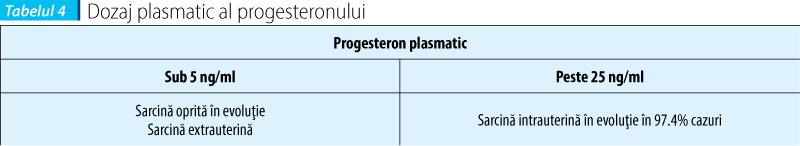
Dozaj plasmatic al progesteronului(17)
Celioscopia reprezintă o modalitate utilă de diagnostic, chiar şi de tratament, a sarcinii extrauterine. În sarcina ectopică necomplicată evidenţiază tumefacţie violacee, alungită în sensul trompei, sânge în cantitate mică în fundul de sac Douglas(17).
Puncţia fundului de sac Douglas (culdocenteza) se efectuează sub anestezie generală cu ajutorul unui ac spinal şi se pătrunde în fundul de sac Douglas prin fornixul vaginal posterior. Dacă prezintă cheaguri de sânge, negricioase, aspect lactat şi hematocrit <15%, se consideră test pozitiv. Puncţia franc pozitivă e indicaţie de laparotomie de urgenţă.
Laparotomia exploratorie, cel mai specific mod de diagnostic al sarcinii extrauterine(18).
Tratamentul medicamentos al sarcinii
extrauterine
Tratamentul conservator este indicat în cazul pacientelor cu sarcină extrauterină necomplicată. Alegerea acestei modalităţi de tratament trebuie stabilită în funcţie de scorul Fernandez(20,21,22,31).
Tratamentul medical cu metotrexat e indicat la pacientele cu sarcină extrauterină necomplicată (neruptă), stabile hemodinamic, cu simptomatologie minimă şi fără lichid intraperitoneal(23). Metotrexatul este antagonist al acidului folic care inhibă folatreductaza, enzimă care transformă acidul folic în acid tetrahidrofolic, forma activă a acidului folic. Acidul tetrahidrofolic este deosebit de important în sinteza nucleotizilor pirimidinici, astfel sunt împiedicate sinteza ADN-ului şi multiplicarea celulară(24,25).


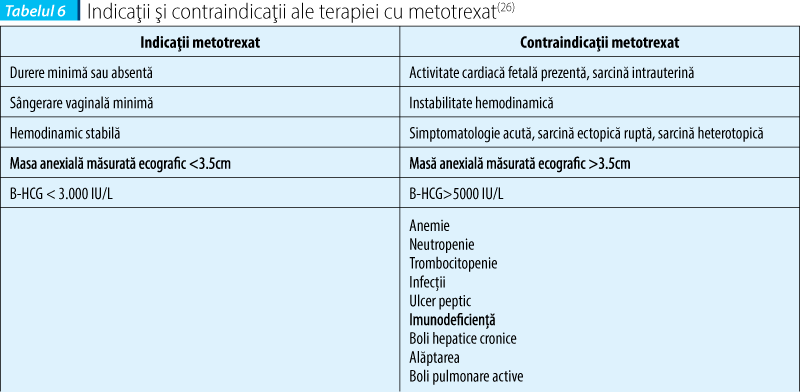

În sarcina ectopică, metotrexatul previne proliferarea celulelor citotrofoblastului, reduce viabilitatea celulară şi sinteza de B-HCG şi implicit a progesteronului, determinând resorbţia sarcinii ectopice şi remodelarea tisulară(24).
Pacientele care vor urma tratamentul cu metotrexat trebuie să nu aibă contraindicaţii, să-şi exprime opţiunea pentru tratamentul medical prin consimţământ scris, să revină la control la fiecare 6 săptămâni, să nu consume alcool cel puţin 7 zile după terminarea tratamentului, să nu alăpteze, să nu se expună la soare (poate declanşa dermatită), să nu urmeze tratament concomitent cu AINS, aspirină, penicilină, trimetroprim, diuretice, antimalarice, suplimente de acid folic, ciclosporine, retinoizi şi să întrerupă activitatea sexuală deoarece poate declanşa ruperea sarcinii ectopice.
Metotrexatul poate fi administrat oral, intravenos, intramuscular sau injectat direct în sacul gestaţional sub control laparoscopic în caz de sarcină extrauterină cornuală sau cervicală. Înainte de administrarea tratamentului se impune recoltarea unui set complet de analize ce cuprinde hemoleucograma, creatinină serică, B-HCG, markerii hepatici, grupă sangvină şi Rh.
Administrarea intramusculară în doză unică a metotrexatului e cea mai folosită metodă în tratamentul sarcinii ectopice. Se administrează 50 mg/m2 în doză unică. Monitorizarea ulterioară a pacientei este foarte importantă. Înainte de administrarea injecţiei cu metotrexat se recoltează B-HCG seric, apoi se va recolta în zilele 4 şi 7 după administrarea metotrexatului(22). Aproximativ 14-20% dintre paciente vor necesita repetarea dozei dacă nivelul B-HCG scade cu mai puţin de 15% după administrarea metotrexatului. Se pot administra maximum 4 doze de metotrexat, iar terapia multiplă va fi însotiţă de administrarea concomitentă de Leucovorin (acid folinic), antagonist al metotrexatului pentru a reduce din efectele adverse severe ce pot apărea la doze multiple de metotrexat(2).
Discuţii şi concluzii
Medicul poate să indice terapia cu doze multiple atunci când sarcina este cornuală, cervicală, activitatea cordului e prezentă, B-HCG>3500 UI/L(28).
În primele zile după administrarea IM a metotrexatului, aproximativ jumătate din paciente afirmă dureri pelviabdominale ce pot fi controlate cu analgezice. Durerea poate fi provocată de distensia tubară datorată avortului tubar sau formării hematomului. (Stovall, 1993). Totuşi nu este recomandată administrarea antialgicelor din cauza faptului că maschează simptomatologia în caz de complicare a sarcinii extrauterine, respectiv ruperea trompei uterine.
Administrarea mifepristonei 600 mg oral asociat dozei unice de metotrexat nu a arătat rată mai mare de succes al tratamentului medical al sarcinii extrauterine (Rozenberg and co. 2003).
Injectarea de metotrexat (1 mg/kg) sub control laparoscopic sau ultrasonografic direct în sacul gestaţional, cu sau fără clorură de potasiu, pentru a produce moartea fetală, prezintă avantajul că minimalizează efectele adverse sistemice. Metoda a arătat că are aceeaşi rată de succes ca şi administrarea IM (Fernandez, 1995).
Chimioterapia combinată - metotrexat + actinomicin D + ciclofosfamidă este utilă la vârste gestaţionale mari (Bakri şi Badawi, 1990).
După terminarea tratamentului medical se indică folosirea unei metode contraceptive cel puţin 6 luni datorită riscului teratogen al metotrexatului(26).
La toate pacientele Rh negative, fără izoimunizare, cu sarcină extrauterină confirmată medical, trebuie să se recomande administrarea de imunoglobulină anti-D(32).
Evoluţia pacientelor tratate medical trebuie monitorizată săptămânal prin dozarea B-HCG (până când nivelul B-HCG scade sub 20 UI/L) şi ecografie TV. Nu se poate exclude posibilitatea rupturii tubare pe baza scăderii valorii B-HCG, după terapia medicamentoasă(33).
Embolizarea arterelor uterine reprezintă o tehnică de radiologie intervenţională ce a câştigat teren din ce în ce mai mult în ultimii ani, utilizată cu succes în asociere cu metotrexat. Tehnica constă în embolizarea selectivă a arterelor uterine (ramurile cervicale), fiind eficientă în tratarea sarcinii ectopice cervicale, dar şi abdominale, salpingiene sau inserate la nivelul cicatricei post-operaţie cezariană(34), deoarece produce oprirea din evoluţie a embrionului şi rezorbţia acestuia, păstrarea permeabilităţii trompei, respectiv conservarea fertilităţii. Valorile ridicate ale B-HCG, precum şi deschiderea unor colaterale utero-ovariene ce nu se pot vizualiza angiografic reprezintă un dezavantaj în ceea ce priveşte succesul metodei(34,35).
Sarcina ectopică reprezintă încă o cauză de mortalitate maternală, în ciuda metodelor moderne de diagnostic şi tratament, ajungând la 6.5%(29). Evoluţia ulterioară a pacientelor cu antecedente de sarcină extrauterină este nefavorabilă în majoritatea cazurilor, aproximativ jumătate rămân sterile, iar 15% vor recidiva. Deşi frecvenţa sarcinilor ectopice a crescut din 1970, mortalitatea a scăzut datorită mijloacelor moderne şi accesibile de diagnostic şi tratament.
Bibliografie
Goldner TE, Lawson HW, Xia Z, Atrash HK Surveillance for ectopic pregnancy-United States, 1970-1989. MMWR CDC Surveill Summ. 1993 Dec 17; 42(6):73-85.
Varma R, Gupta J. Tubal ectopic pregnancy. Clin Evid (Online) 2009;Pii:1406.
Lansac J, Lecompte P. Gynecologie pour le practicien. Simep, Ed. Paris, 1989.
Leke RJ, Goyaux N, Matsuda T, Thonneau PF - Ectopic pregnancy in Africa: a population-based study. Obstet Gynecol. 2004 Apr; 103(4):692-7.
Levi CS, Lyons EA. The first trimester. In: Rumack CM, Wilson SR, Charboneau JW, Levine D, editors. Diagnostic Ultrasound. 4th ed. Chapter 30. Philadelphia: Elsevier; 2011. pp. 1099–110.
Kirsch JD, Scoutt LM. Imaging of ectopic pregnancy. Appl Radiol. 2010;39:10–25.
Bouyer J, Coste J, Shojaei T, Pouly JL, Fernandez H, Gerbaud L, Job-Spira N. Risk factors for ectopic pregnancy: a comprehensive analysis based on a large case–control, population-based study in France. Am J Epidemiol. 2003;157:185–194.
Seow KM, Huang LW, Lin YH, Lin MY, Tsai YL, Hwang JL. Cesarean scar pregnancy: Issues in management. Ultrasound Obstet Gynecol. 2004;23:247–53.
Ash A, Smith A, Maxwell D. Caesarean scar pregnancy. BJOG. 2007;114:253–63.
Ludwig M, Kaisi M, Bauer O, Diedrich K. The forgotten child: A case of heterotopic, intra-abdominal and intrauterine pregnancy carried to term. Hum Reprod. 1999;14:1372 -4.
Varma R, Mascarenhas L, James D. Successful outcome of advanced abdominal pregnancy with exclusive omental insertion. Ultrasound Obstet Gynecol. 2003;21:192–4.
AIUM practice guideline for the performance of obstetric ultrasound examinations. American Institute of Ultrasound in Medicine J Ultrasound Med. 2010 Jan; 29(1):157-66.
Shalev E, Yarom I, Bustan M, Weiner E, Ben-Shlomo I. Transvaginal sonography as the ultimate diagnostic tool for the management of ectopic pregnancy: experience with 840 cases. Fertil Steril. 1998 Jan; 69(1):62-5.
Barnhart K, Mennuti MT, Benjamin I, Jacobson S, Goodman D, Coutifaris C. Prompt diagnosis of ectopic pregnancy in an emergency department setting. Obstet Gynecol. 1994 Dec; 84(6):1010-5.
Silva C, Sammel MD, Zhou L, Gracia C, Hummel AC, Barnhart K. Human chorionic gonadotropin profile for women with ectopic pregnancy. Obstet Gynecol. 2006 Mar; 107(3):605-10.
Horne AW, Shaw JL, Murdoch A, McDonald SE, Williams AR, Jabbour HN, Duncan WC. Placental growth factor: a promising diagnostic biomarker for tubal ectopic pregnancy.Critchley HO J Clin Endocrinol Metab. 2011 Jan; 96(1):E104-8.
Robson SJ, O’Shea RT, Aust NZJ. Undiagnosed ectopic pregnancy: a retrospective analysis of 31 ‘missed’ ectopic pregnancies at a teaching hospital. Obstet Gynaecol. 1996 May; 36(2):182-5.
Carr RJ, Evans P. Ectopic pregnancy. Prim Care 2000; 27:169–183.
Mittal S. Non-surgical management of ectopic pregnancy. Obs Gyn Com 1999; 1:23-28.
Cohen MA, Sauer MV. Expectant management of ectopic pregnancy. Clin Obstet Gynecol 1999; 42:48–54.
Buster JE, Pisarska MD. Medical management of ectopic pregnancy. Clin Obstet Gynecol 1999; 42:23–30.
Lipscomb GH, McCord ML, Stovall TG, et al. Predictors of success of methotrexate treatment in women with tubal ectopic pregnancies. N Engl J Med. 1999;341:1974–1978.
Nama V, Manyonda I. Tubal ectopic pregnancy: diagnosis and management. Arch Gynecol Obstet. 2009 Apr; 279(4):443-53.
Barnhart KT, Gosman G, Ashby R, Sammel M. The medical management of ectopic pregnancy: a meta-analysis comparing “single dose” and “multidose” regimens. Obstet Gynecol,2003;101(4):778-84.
Metotrexat. Prospect şi informaţii pentru utilizator, Martie 2012.
Why women die. Report on confidential enquiries into maternal deaths in the United Kingdom 1994-1996. Norwich: Stationery Office; 1998.
Tulandi T. Current protocol for ectopic pregnancy. Contemp Obstet Gynecology 1999; 44:42.
Lansac L, Lecompte P. Gynecologie pour le practicien.Simep, Ed. Paris, 1989.
Cartwright P, DiPietro D. Beta HCG is a diagnostic and for suspected ectopic pregnancy. Obstet Gynecol. 1984; 63:76.
Fernandez H, Lelaidier C, Thouvenez V et al. The use of pretherapeutic, predictive score to determine inclusion criteria for the non-surgical management of ectopic pregnancy. Hum Reprod 1991, 6:995-998.
Copel JA, Gollin YG, Grannum PA: Alloimunization disorders and pregnancy. Semin Perinatol 1991 15 (3): 251-256
Lipscomb GH, Puckett KJ, Bran D, Ling FW. Management of separation painafter single dose Methotrexat therapy for ectopic pregnancy. Obstet Gynecol 1999, 93:590.
Dumitraşcu MC, Horhoianu V. Embolizarea arterelor uterine. Ed. Univ. “Carol Davila” Bucureşti, 2008.
Einarsson J.I., Michel S., Young A.E. Delayed spontaneous expulsion of a cervical ectopic pregnancy: A case report. Journal of Minimally Invasive Gynecology.2005. 12. 2: 165-167.
Articole din ediţiile anterioare
A rare case of complete hydatidiform mole with prolonged evolution – clinical case
Mola hidatiformă, cunoscută drept sarcină molară, reprezintă o boală gestaţională trofoblastică cu punct de plecare placentar şi capacitate de meta...
Embolizarea în sarcina ectopică cervicală
Embolizarea arterelor uterine este o metodă minim invazivă, ce aparţine radiologiei intervenţionale, prin care se poate trata cu succes sarcina ect...