The thyroid gland pathology during pregnancy is one of the most common disease which involves serious complications upon the pregnant women`s body and fetus. Thyroid hormones play a critical role in fetal development. During pregnancy, increased levels of thyroid hormone synthesis are required to meet fetal needs. Nowadays, in our country there are no clinical guides about monitoring of thyroid function in pregnancy, so in consequence we will discuss about the clinical involvement of thyroid pathology, which includes hyperthyroidism, hypothyroidism, nodules (benign or malignant) and autoimmune pathology. At the same time, we will discuss about the consequences of high-levels of hCG on thyroid hormones and the comparison between a pregnant healthy woman and another one with thyroid pathology will be revealed. In this article we will explain the physiology and physiopathology of thyroid gland during pregnancy and we will also discuss about the clinical manifestations that appear on pregnant women. We will present normal and pathological values of thyroid hormones and their specific reference ranges. The effects of thyroid pathology on fetus growth, which also includes fetus malformations that may appear, represent another interesting fact that will be debated în this article. In the end of the article it will be presented the screening importance in thyroid pathology starting with the first trimester of pregnancy and the importance of immediate initiation of specific drugs administration.
Monitorizarea funcţiei tiroidiene în sarcină
Monitoring of thyroid function în pregnancy
First published: 15 martie 2016
Editorial Group: MEDICHUB MEDIA
Abstract
Rezumat
Patologia glandei tiroide este una dintre cele mai frecvente afecţiuni ale sarcinii, cu repercusiuni deopotrivă materne şi fetale. Hormonii tiroidieni au un rol critic în dezvoltarea fetală, motiv pentru care sinteza hormonilor tiroidieni este crescută pe parcursul sarcinii, în scopul satisfacerii nevoilor fetale. Dat fiind faptul că ghidurile naţionale actuale nu cuprind monitorizarea funcţiei tiroidiene în sarcină, considerăm oportună revizuirea actualizată a patologiei tiroidiene, incluzând hipotiroidismul şi hipertiroidismul, nodulii tiroidieni (benigni şi maligni) şi boala autoimună. Un interes special merită a fi acordat consecinţelor nivelurilor înalte ale hCG asupra funcţiei tiroidiene, comparând evoluţia sarcinii în absenţa şi în prezenţa patologiei tiroidiene. Ne propunem reanalizarea fiziologiei şi fiziopatologiei glandei tiroide în sarcină, precum şi manifestările clinice ale bolii tiroidiene pe fondul sarcinii. De asemenea, prezentăm valorile normale şi patologice ale hormonilor tiroidieni, specifice sarcinii. Efectele patologiei tiroidiene asupra creşterii şi dezvoltării fetale, incluzând aspectele disruptive, reprezintă un alt aspect interesant de discuţie. În final, articolul subliniază importanţa screening-ului tiroidian efectuat în primul trimestru de sarcină şi a iniţierii imediate a tratamentului specific.
Fiziologia funcţiei tiroidiene materne şi fetale
Hormonii tiroidieni sunt factorii determinanţi esenţiali implicaţi în dezvoltarea creierului, dezvoltarea somatică la sugari şi totodată în desfăşurarea activităţii metabolice la adulţi. Pentru a le menţine disponibilitatea permanentă, ei sunt captaţi în depozite mari în circulaţie şi în glanda tiroidă; în plus, biosinteza hormonilor tiroidieni şi secreţia lor fiind menţinute în limite înguste, printr-un mecanism de reglare foarte sensibil, la minime modificări ale concentraţiei hormonale în circulaţia sangvină.
Există doi hormoni tiroidieni biologic activi: Tiroxina (T4) şi Triiodotironina (T3); T4 este produs exclusiv de glanda tiroidă, în timp ce T3 este un produs al tiroidei, dar şi al multor altor ţesuturi, fiind obţinut prin eliminarea iodului din T4. Glanda tiroidă conţine cantităţi mari de T4 şi T3 încorporate în tireoglobulină, proteină în cadrul căreia hormonii tiroidieni sunt sintetizaţi şi stocaţi, ceea ce le asigură o biodisponibilitate rapidă.
Există o serie de aspecte importante care trebuie luate în considerare atunci când intră în discuţie o afectare tiroidiană în timpul sarcinii sau atunci când femeile cu afectare tiroidiană tratată în antecedente rămân însărcinate.
Datorită schimbărilor fiziologiei tiroidei induse de sarcină, reflectate în modificările valorilor hormonale de laborator, ghidurile Asociaţiei Americane a Tiroidei (ATA) pentru diagnosticarea şi gestionarea bolii tiroidiene în timpul sarcinii şi post-partum recomandă folosirea unor intervale de referinţă trimestriale specifice pentru TSH şi intervalele de referinţă trimestriale specifice pentru free T4(1).
Nevoile metabolice crescute în timpul unei sarcini normale induc schimbări majore care constau într-o creştere a concentraţiei serice a globulinei de legare a tiroxinei (TBG) şi stimularea receptorului de tireotropină (TSH) de către gonadotropina corionică umană (hCG). În timpul sarcinii, concentraţiile serice ale TBG cresc de aproximativ două ori sub stimulul estrogenic al producţiei; pentru a menţine în limite normale concentraţia hormonilor tiroidieni liberi în timpul acestei perioade, nivelul de sinteză al T3 şi T4 trebuie să crească. Concentraţiile totale T4 şi T3 cresc în prima jumătate a sarcinii, stabilizându-se la aproximativ 20 de săptămâni de gestaţie, moment în care se ajunge la o nouă stare de echilibru şi rata de producţie totală a hormonilor tiroidieni revine la valorile anterioare sarcinii. Prin urmare, nivelul de TBG ridicat duce la o creştere a concentraţiilor serice totale atât de T4, cât şi de T3(2).
hCG face parte, alături de TSH, din familia hormonilor glicoproteici, având o subunitate a comună şi o subunitate b specifică, dar considerabil asemănătoare TSH-ului, ceea ce conferă acestui hormon uşoară activitate de stimulare tiroidiană. Concentraţiile serice ale hCG încep să crească imediat după fertilizare şi ating maximul la 10-12 săptămâni de gestaţie, când concentraţiile serice totale ale T3 şi T4 cresc şi ele; concentraţiile serice ale hormonilor liberi tiroidieni înregistrează o creştere uşoară, rămânând de obicei în limite normale, iar TSH-ul scade corespunzător, pentru 10-20% dintre femeile însărcinate, concentraţiile serice fiind tranzitor scăzute sau nedetectabile. Acest hipertiroidism temporar, adesea subclinic, trebuie să fie considerat fiziologic, cu atât mai mult, cu cât scăderea ulterioară a hCG-ului pe parcursul sarcinii este urmată de normalizarea funcţiei tiroidiene.
O serie de studii populaţionale susţin limita inferioară a intervalului de referinţă pentru TSH la femeile gravide sănătoase în timpul primului trimestru de sarcină între 0,03 şi 0,1 mU/L. Într-unul dintre cele mai mari studii, incluzând peste 13.000 de femei gravide, intervalul de referinţă (2,5 - percentila 97,5) pentru TSH în primul trimestru a fost de 0,08 la 2,99 mU/L(3). Astfel, în cazul în care laboratorul nu prevede intervale de referinţă trimestriale specifice pentru TSH (mU/l), pot fi utilizate următoarele intervale de referinţă:
- primul trimestru: 0,1 până la 2,5 mU/L;
- al doilea trimestru: 0,2-3,0 mU/L;
- al treilea trimestru: 0,3-3,0 mU/L.
T4 liber dozat prin tehnici uzuale de laborator nu este un parametru sigur, fiind necesară aplicarea metodelor şi intervalelor de referinţă trimestru-specifice(1). În lipsa acestora, dozarea T4 total este o modalitate mai eficientă de monitorizare a funcţiei tiroidiene în sarcină.
În ceea ce priveşte necesarul de iod, acesta este crescut la femeile gravide datorită creşterii producţiei materne de T4 necesar menţinerii statusului eutiroidian şi creşterii clearance-ului renal de iod(3). Deficitul sever de iod în timpul sarcinii are ca rezultat o reducere a producţiei materne de tiroxină, o reducere consecutivă a transferului placentar al tiroxinei şi, în consecinţă, afectarea dezvoltării neurologice fetale(4). Pe de altă parte, consumul excesiv de iod poate determina hipotiroidism fetal şi guşă. Organizaţia Mondială a Sănătăţii (OMS) recomandă din anul 2007 administrarea a 250 mcg de iod pe zi în timpul sarcinii şi alăptării. Institutul american de medicină recomandă un aport zilnic de iod de 220 mcg în timpul sarcinii şi de 290 mcg în timpul alăptării. Asigurarea aportului de iod în Statele Unite ale Americii se face prin includerea a 150 mcg de iod în majoritatea suplimentelor prenatale recomandate şi în perioada de lactaţie(5). Dată fiind concentraţia acestui element în sol, în România, aportul de iod din alimentaţie este insuficient, 64% din populaţia ţării prezentând, conform raportului OMS/2004, deficit moderat de iod; prevenţia deficitului de iod prin iodarea universală a sării a fost legiferată prin HG 568/2002, modificată prin HG 1904/2006, care prevede fortificarea cu 30 mg iod/kg sare, utilizată obligatoriu în fabricarea pâinii şi a produselor de panificaţie şi opţional în hrana animalelor şi în industria alimentară. Deficitul de iod în sarcină este diagnosticat prin concentraţia iodului urinar sub 150 mcg/L.
Pe parcursul săptămânilor 10-12 de gestaţie apare tireotropina fetală, iar tiroida fătului devine capabilă să concentreze iodul şi să sintetizeze iodotironine în concentraţii mici până în săptămâna a 20-a, pentru ca ulterior secreţia tiroidiană să crească gradual; la termen, concentraţia de TSH fetal este crescută, în timp ce hormonii tiroidieni sunt semnificativ scăzuţi, pentru ca la 48 de ore după naştere TSH-ul să scadă de la 50-80 mU/L la 10-15 mU/L, concordant cu creşterea hormonilor tiroidieni la valori uşor mai mari faţă de cele ale vârstei adulte. Proporţia de hormoni tiroidieni care traversează placenta pare a fi semnificativă, dat fiind faptul că absenţa congenitală a tiroidei se asociază cu concentraţii fetale ale hormonilor tiroidieni de 20-50% din valorile fetale normale; atât TRH, TSH, cât şi anticorpii antireceptor TSH traversează placenta, marcând statusul tiroidian fetal.
Hipertiroidismul în sarcină
Hipertiroidismul, caracterizat prin supresia tireotropinei şi creşterea tiroxinei libere şi/sau a triiodotironinei, este relativ mai puţin frecvent în timpul sarcinii, având o incidenţă de 0,1-0,4% dintre sarcini(5).
Deşi hipertiroidismul de orice cauză poate complica sarcina, boala Graves şi hipertiroidismul hCG-mediat reprezintă cele mai frecvente cauze. Boala Graves, de obicei, devine mai puţin severă în timpul etapelor tardive ale sarcinii datorită unei scăderi a concentraţiei de anticorpi îndreptaţi împotriva receptorului pentru TSH sau, mai rar, datorită unei schimbări în activitatea anticorpilor de la stimulare la blocare(4). Hipertiroidismul hCG-mediat poate apărea tranzitoriu în prima jumătate a gestaţiei şi este de obicei mai sever decât boala Graves(6).
Gradul afectării materne şi fetale în hipertiroidism depinde de gravitatea anomaliilor biochimice(5). Multe dintre simptomele nespecifice asociate cu sarcina sunt similare cu cele asociate hipertiroidismului, incluzând tahicardie, intoleranţă la căldură şi transpiraţie excesivă(2,7). Relativ mai specifice sunt anxietatea, tremorul mâinilor şi pierderea în greutate, în condiţiile unui aport alimentar normal sau crescut; guşa şi oftalmopatia sunt înalt sugestive pentru hipertiroidismul Graves(2). Sarcina complicată de hipertiroidism insuficient controlat asociază creşterea ratei avortului spontan şi a naşterii premature. Absenţa simptomatologiei în contextul unui titru scăzut al TSH-ului caracterizează hipertiroidismul subclinic(8).
Diagnosticul de hipertiroidism în timpul sarcinii se bazează pe constatarea unor valori serice suprimate (<0,1 mU/L) sau nedetectabile (<0,01 mU/L) ale TSH-ului şi niveluri crescute de hormoni tiroidieni care depăşesc limitele normale pentru sarcină(8).
Dacă nivelul TSH este <0,1 mU/l, trebuie obţinută valoarea lui T4 liber; dacă T4 liber este în limite normale pentru sarcină, nivelul de T3 liber ar trebui să fie, de asemenea, măsurat. În cazul în care nivelul hormonilor tiroidieni liberi este discordant cu valoarea serică a TSH-ului şi cu manifestările clinice, trebuie să fie măsurat T4 total(9) (figura 1). Anticorpii antireceptor TSH sunt pozitivi la 95% dintre pacientele cu boală Graves.
Dintre copiii născuţi din mame cu tiroidită Graves, 1-5% prezintă hipertiroidism datorat transferului transplacentar de anticorpi specifici. Incidenţa este crescută la femeile al căror titru de anticorpi este crescut(9). Caracteristicile hipertiroidismului fetal constau în creşterea alurii ventriculare (>160 b/min), guşă, vârstă osoasă avansată şi retard de creştere intrauterină. Monitorizarea fetală a gravidelor cu boala Graves trebuie să vizeze semnele de tireotoxicoză fetală, prin determinarea sistematică a frecvenţei cardiace fetale şi a creşterii fetale, îndeosebi atunci când nivelurile materne de anticorpi antireceptor TSH dozate la 20-24 de săptămâni de gestaţie sunt crescute cu mai mult de 3 ori valoarea-prag superioară(3) (figura 1).
Hipertiroidismul hCG-mediat este de obicei tranzitoriu şi nu necesită tratament. Opţiunile terapeutice pentru femeile gravide cu hipertiroidism cu semnificaţie clinică datorat bolii Graves sau cu boală tiroidiană nodulară sunt limitate, deoarece terapia poate afecta fătul. Obţinerea rezultatelor optime fetale şi materne depinde de controlul hipertiroidismului, prin administrarea celor mai mici doze medicamentoase capabile să reducă şi să menţină concentraţia serică a T4 liber la limita maximă a normalului pentru femeile neînsărcinate. Evaluarea nivelului de T4 liber şi/sau T4 total trebuie să fie frecventă şi sistematică, la intervale de patru săptămâni, cu ajustarea corespunzătoare a medicaţiei(8). Indicaţia terapeutică constă în creşterea T4 total şi/sau T3 total de peste 1,5 ori faţă de valoarea-prag superioară a hormonilor în afara sarcinii sau în creşterea marcată a nivelurilor trimestru-specifice ale T4 liber. Dat fiind faptul că administrarea iodului radioactiv este absolut contraindicată în sarcină, prima linie de tratament preoperator a bolii Graves, a adenomului toxic, a guşii toxice polinodulare sau a bolii trofoblastice gestaţionale o constituie tioamidele (Methimazole, Propilthiouracil, Carbimazole). Propilthiouracilul este administrat de elecţie în primul trimestru, deoarece, deşi traversează bariera placentară, legarea puternică de proteinele plasmatice face ca această traversare să fie mai lentă şi se asociază cu cea mai redusă rată de efecte teratogene. În trimestrul al doilea este recomandată trecerea la doze echivalente de Methimazole din cauza hepatotoxicităţii rare, dar deosebit de grave a Propilthiouracilului. În trimestrul al treilea, adesea tratamentul poate fi întrerupt. Dozele minime de tratament sunt reprezentate de 100-150 mg/zi în 2-3 prize de Propilthiouracil, 5-10 mg/zi de Methimazole sau 5-15 mg/zi Carbimazole, 300 mg de Propilthiouracil fiind echivalent cu 10-15 mg de Methimazole. Tratamentul concomitent cu b-blocanţi de tipul atenololului (25-50 mg/zi) sau propranololului (60-80 mg/zi în 3-4 prize) trebuie limitat la formele moderate şi severe de hipertiroidism, pe o durată maximă de 2-6 săptămâni, din cauza riscului restricţiei de creştere şi a hipoglicemiei fetale. Tiroidectomia este rezervată cazurilor cu boală Graves şi intoleranţă alergică sau agranulocitară la tioamide.
Hipotiroidismul în sarcină
Cele mai frecvente cauze de hipotiroidism în timpul sarcinii sunt tiroidita cronică autoimună (Hashimoto) şi guşa hipotiroidiană prin deficit de iod; ablaţia tiroidei prin administrare de iod radioactiv sau tulburările hipofizei ori hipotalamusului sunt cauze rare, dar care pot deopotrivă complica sarcina.
Manifestările clinice ale hipotiroidismului, atunci când există, sunt nespecifice, putând fi uşor atribuite stării de gestaţie: oboseală, intoleranţă la frig, constipaţie şi creştere în greutate.
Diagnosticul de hipotiroidism primar în timpul sarcinii se bazează pe constatarea unei concentraţii crescute a tirotropinei serice, definită folosind intervalele de referinţă TSH trimestriale specifice pentru femeile gravide(8). Pentru femeile în primul trimestru de sarcină, cu o valoare a TSH-ului peste 2,5 mU/L, sau peste 3 mU/L în al doilea şi al treilea trimestru, trebuie măsurată, de asemenea, tiroxina liberă(7). Hipotiroidismul cu semnificaţie clinică este definit ca o concentraţie ridicată de TSH trimestrial specific în concordanţă cu o concentraţie scăzută a T4 liber(8). Hipotiroidismul subclinic este definit ca o concentraţie ridicată de TSH seric şi o concentraţie normală de T4 liber(8). Femeile cu hipotiroidism central hipofizar sau boală hipotalamică nu vor avea concentraţii crescute de TSH în timpul sarcinii. Anticorpii antitiroid-peroxidază (ATPO), ca markeri ai prezenţei bolii autoimune, au fost corelaţi cu creşterea riscului de avort spontan, naştere prematură, macrosomie fetală şi cu creşterea mortalităţii perinatale în general(16). Administrarea de levotiroxină în doze medii de 50 mcg/zi gravidelor cu status eutiroidian, dar cu niveluri crescute de ATPO, care s-a dovedit a dezvolta până la finalul sarcinii în procent de 20% o formă de hipotiroidism subclinic, are ca efect scăderea semnificativ statistică a ratei de avort spontan şi naştere prematură(17). Dat fiind faptul că screening-ul anticorpilor antitiroidieni nu este universal acceptat, autori de referinţă în specialitate recomandă administrarea de T4 pacientelor cu titruri crescute de anticorpi şi avort recurent în antecedente, TSH fiind monitorizat atent prin dozări seriate la un interval de 4 săptămâni; aministrarea de T4 devine obligatorie dacă ATPO se însoţesc de creşterea tireotropinei dincolo de limita trimestru-specifică(18) (figura1).
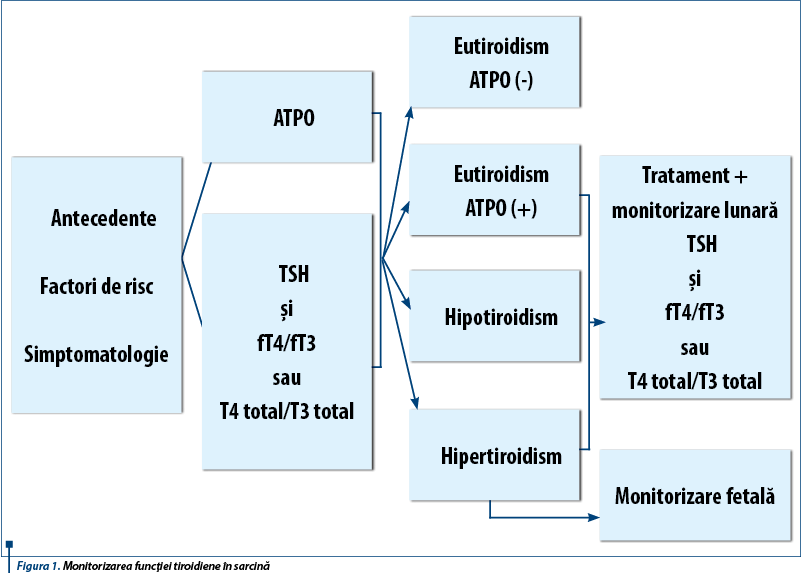
Hipotiroidismul congenital apare în contextul ageneziei sau disgeneziei tiroidiene fetale, al dishormonogenezei congenitale sau deficienţei de iod. Impactul nefast pe care hipotiroidismul îl are asupra evoluţiei sarcinii constituie o certitudine, dar de peste 10 ani endocrinologii şi obstetricienii dezbat eficacitatea screening-ului pentru afecţiunile tiroidiene subclinice, în sensul efectuării sale de rutină sau indicat de simptomatologie şi factori de risc. Dată fiind prevalenţa globală a afectării tiroidiene, apreciată la 1/1000 sarcini, considerată insuficientă pentru a justifica screening-ul în sarcină, majoritatea societăţilor profesionale, incluzând Asociaţia Americană a Tiroidei (ATA), Societatea de Endocrinologie Americană şi Colegiul American de Obstetrică şi Ginecologie (ACOG) recomandă screening-ul individualizat; ATA recomandă măsurarea TSH-ului seric la femeile gravide în cazul în care acestea sunt simptomatice, dacă provin dintr-o regiune cunoscută cu un deficit major de iod, dacă au antecedente personale sau heredocolaterale de boală tiroidiană, anticorpi antiperoxidază tiroidiană, diabet de tip I, istoric de naştere prematură sau avort, istoric de radiaţii la nivelul capului sau gâtului, obezitate morbidă (IMC ≥40 kg/m2), infertilitate sau vârsta mai mare de 30 de ani(13,14). La femeile care îndeplinesc criteriile de selecţie se determină TSH seric în primul trimestru. Dacă TSH-ul seric este normal, nu sunt necesare teste suplimentare; dacă nivelul de TSH este >2,5 mU/L, T4 liber trebuie măsurat pentru a determina gradul de hipotiroidism(13,14,15) (figura 1). Cu toate acestea, o asemenea abordare subdiagnostichează până la o treime din femeile cu hipotiroidism şi datele preliminare sugerează că screening-ul universal este rentabil dacă se constată faptul că tratamentul îmbunătăţeşte IQ-ul descendenţilor(14). În acest sens, o serie de studii observaţionale au sugerat faptul că descendenţii femeilor cu disfuncţie tiroidiană subclinică au un risc crescut de dezvoltare neurocomportamentală deficitară, sarcinile fiind grevate de o rată crescută a complicaţiilor de tipul morţii fetale in utero, naşterii premature sau decolării premature a placentei normal inserate. Cel mai recent studiu pe această temă, „Controlled Antenatal Thyroid Screening Trial”, cuprinzând aproape 22.000 de sarcini, constată faptul că tratamentul hipotiroidismului subclinic nu are nici un beneficiu asupra IQ-ului copiilor până la 3 ani, dovedindu-se ineficient în îmbunătăţirea funcţiei cognitive. Studiul condus de „Eunice Kennedy-Shriver” National Institute of Child Health and Human Development Maternal-Fetal Medicine Units Network va aduce în curând concluzii edificatoare(19). Până atunci, screening-ul universal al hipotiroidismului pentru femeile gravide asimptomatice în timpul primului trimestru de sarcină rămâne controversat.
Prognosticul favorabil matern şi fetal depinde de tratarea hipotiroidismului matern cu hormoni tiroidieni (T4). Scopul tratamentului este de a menţine TSH-ul seric al mamei în intervalul de referinţă trimestru-specific, respectiv 0,1-2,5 mU/L, 0,2-3 mU/L şi 0,3-3 mU/L(9). Femeile cu hipotiroidism preexistent care devin gravide au nevoie de o cantitate mai mare de T4 în timpul sarcinii. Dozele necesare pot creşte cu mai mult de 50 de procente în timpul sarcinii, iar creşterea necesarului apare încă din a cincea săptămână de gestaţie(11).
Tiroidita post-partum are o prevalenţă variabilă, între 1% şi 17%, atingând 25% în rândul pacientelor cu diabet zaharat de tip I, 42% între cele cu antecedente de tiroidită post-partum şi 40-60% în rândul pacientelor ATPO pozitive(20). Disfuncţia tiroidiană poate apărea consecutiv pierderii unei sarcini sau după o naştere normală, la paciente eutiroidiene sau cu terapie de substituţie tiroidiană, sub formă de tiroidită post-partum, caracterizată de un hipertiroidism tranzitor, urmat sau nu de un hipotiroidism pasager sau permanent, sau sub formă de exacerbare a unei tiroidite cronice limfocitare (Hashimoto) care poate necesita creşterea tranzitorie sau permanentă a dozelor hormonale.
Bibliografie
2. Glinoer D. The regulation of thyroid function in pregnancy: pathways of endocrine adaptation from physiology to pathology. Endocr Rev 1997; 18:404.
3. Dashe JS, Casey BM, Wells CE, et al. Thyroid-stimulating hormone in singleton and twin pregnancy: importance of gestational age-specific reference ranges. Obstet Gynecol 2005; 106:753.
4. Stricker R, Echenard M, Eberhart R, et al. Evaluation of maternal thyroid function during pregnancy: the importance of using gestational age-specific reference intervals. Eur J Endocrinol 2007; 157:509.
5. Gilbert RM, Hadlow NC, Walsh JP, et al. Assessment of thyroid function during pregnancy: first-trimester (weeks 9-13) reference intervals derived from Western Australian women. Med J Aust 2008; 189:250.
6. Fitzpatrick DL, Russell MA. Diagnosis and management of thyroid disease in pregnancy. Obstet Gynecol Clin North Am 2010; 37:173.
7. Ain KB, Mori Y, Refetoff S. Reduced clearance rate of thyroxine-binding globulin (TBG) with increased sialylation: a mechanism for estrogen-induced elevation of serum TBG concentration. J Clin Endocrinol Metab 1987; 65:689.
8. Stagnaro-Green A, Abalovich M, Alexander E, et al. Guidelines of the American Thyroid Association for the diagnosis and management of thyroid disease during pregnancy and postpartum. Thyroid 2011; 21:1081.
9. Spencer CA, LoPresti JS, Patel A, et al. Applications of a new chemiluminometric thyrotropin assay to subnormal measurement. J Clin Endocrinol Metab 1990; 70:453.
10. Abalovich M, Gutierrez S, Alcaraz G, et al. Overt and subclinical hypothyroidism complicating pregnancy. Thyroid 2002; 12:63.
11. Krassas GE, Pontikides N, Kaltsas T, et al. Disturbances of menstruation in hypothyroidism. Clin Endocrinol (Oxf) 1999; 50:655.
12. Hallengren B, Lantz M, Andreasson B, Grennert L. Pregnant women on thyroxine substitution are often dysregulated în early pregnancy. Thyroid 2009; 19:391.
13. Surks MI, Ortiz E, Daniels GH, et al. Subclinical thyroid disease: scientific review and guidelines for diagnosis and management. JAMA 2004; 291:228.
14. Committee on Paţient Safety and Quality Improvement, Committee on Professional Liability. ACOG Committee Opinion No. 381: Subclinical hypothyroidism în pregnancy. Obstet Gynecol 2007; 110:959.
15. De Groot L, Abalovich M, Alexander EK, et al. Management of thyroid dysfunction during pregnancy and postpartum: an Endocrine Society clinical practice guideline. J Clin Endocrinol Metab 2012; 97:2543.
16. Thangaratinam S, Tan A, Knox E, Kilby MD, Franklyn J, Coomarasamy A. Association between thyroid autoantibodies and miscarriage and preterm birth: meta-analysis of evidence. BMJ. 2011;342:d2616.
17. Negro R, Formoso G, Mangieri T, Pezzarossa A, Dazzi D, Hassan H Levothyroxine treatment in euthyroid pregnant women with autoimmune thyroid disease: effects on obstetrical complications.J Clin Endocrinol Metab. 2006;91(7):2587.
18. Ross D.S. Overview of thyroid disease in pregnancy, UpToDate, Literature review current through: Mar 2015.
19. Casey B, de Veciana M, Thyroid screening în pregnancy. Am J Obstet Gynecol. 2014 Oct;211(4):351-353.e1. doi: 10.1016/j.ajog.2014.08.013.
20. Nicholson WK, Robinson KA, Smallridge RC, Ladenson PW, Powe NR. Prevalence of postpartum thyroid dysfunction: a quantitative review. Thyroid. 2006;16(6):573.
http://www.uptodate.com/contents/overview-of-thyroid-disease-in-pregnancy/abstract/28
Articole din ediţiile anterioare
Rezultate la gravidele care asociază tiroidită autoimună şi COVID-19
Infecţiile cu agenţii patogeni din familia Coronaviridae (în special SARS-CoV-2) influenţează cu precădere axul tiroidian, manifestându-s...
Trombembolismul pulmonar asociat sarcinii - status fiziologic procoagulant
Sarcina reprezintă o stare procoagulantă cu risc de dezvoltare a trombembolismului pulmonar, prin creşterea fiziologică a factorilor procoagulanţi ...
Infecţia cu Virusul Herpes Simplex în sarcină
Infecţia cu virusurile Herpes Simplex (VHS) reprezintă un grup complex de infecţii, care pot avea drept gazdă organismul uman. Există două tipuri d...
Trombofilia ereditară şi complicaţiile obstetricale mediate de placentă
Trombofilia se referă la o predispoziţie către o stare de hipercoagulabilitate şi poate fi identificată în 30-50% din cazurile de tromboembolism ve...