Introduction. The objective of this review is to provide an overview to the family physician regarding the diagnosis of congenital anomalies of the kidney and urinary tract (CAKUT) in children. The aim is to promptly guide pediatric patients with these anomalies towards specialized services, significantly contributing to preventing the onset of chronic kidney disease in adults. Methodology. We conducted a review of specialized medical literature, encompassing articles and studies published on this topic (PubMed, Cochrane, BMJ, Elsevier, JAMA Network, The Lancet, New England Journal of Medicine, Springer Nature, Wiley). Conclusions. Antenatal hydronephrosis (ANH) is defined as the dilation of the renal pelvis and/or calyces. ANH, generally considered a marker of CAKUT, is the most common anomaly detected prenatally via ultrasound, occurring in 0.5-1% of all pregnancies. Ultrasound assessment is the best method for diagnosing and monitoring hydronephrosis both prenatally and postnatally. It is a noninvasive, readily available, rapid, non-radiating, and cost-effective examination method. Throughout history, various classification systems have existed based on the specialty of study. A unified classification system applicable in both prenatal and postnatal consultations to describe urinary tract (UT) dilation would be beneficial for promoting communication across specialties. Moreover, developing a common classification system would facilitate unambiguous information transfer between various care providers involved in the care of pregnant women and infants, leading to more rigorous research on specific outcomes, such as the resolution of renal dilation, specific uropathies, risks of urinary tract infection, chronic kidney disease stages II or more advanced, hypertension, proteinuria, and surgical interventions.
Hidronefroza antenatală – marker-surogat al anomaliilor congenitale ale rinichilor şi tractului urinar la copil
Antenatal hydronephrosis – surrogate marker of congenital kidney and urinary tract anomalies in children Suggested citation for this article: Picioreanu I, Picioreanu DM. Antenatal hydronephrosis – surrogate marker of congenital kidney and urinary tract anomalies in children. Medic.ro. 2024;157(1):12-20.
First published: 29 martie 2024
Editorial Group: MEDICHUB MEDIA
DOI: 10.26416/Med.157.1.2024.9451
Abstract
Rezumat
Introducere. Obiectivul acestei revizuiri este de a oferi o imagine de ansamblu medicului de familie asupra diagnosticului anomaliilor congenitale ale rinichiului şi tractului urinar (ACRTU) la copil, pentru a orienta cât mai prompt pacientul pediatric cu aceste anomalii către serviciile specializate, contribuind semnificativ la prevenirea apariţiei bolii renale cronice la adult. Metodologie. Am efectuat o revizuire a literaturii de specialitate medicală care a cuprins articolele şi studii publicate pe această temă (PubMed, Cochrane, BMJ, Elsevier, JAMA Network, The Lancet, New England Journal of Medicine, Springer Nature, Wiley). Concluzii. Hidronefroza antenatală (HAN) este definită ca dilatarea renală a pelvisulului şi/sau calicelor. HAN, considerată în general un marker al ACRTU, este cea mai frecventă anomalie detectată prenatal ecografic şi apare la 0,5-1% din totalul sarcinilor. Evaluarea ecografică este cea mai bună metodă pentru diagnosticul şi urmărirea hidronefrozei, atât prenatal, cât şi postnatal. Este o metodă de examinare neinvazivă, disponibilă, rapidă, neiradiantă şi cu costuri reduse. Din punct de vedere istoric, au existat mai multe sisteme de clasificare, în funcţie de specialitatea de studiu. Un singur sistem de clasificare, care poate fi utilizat atât în consultaţia prenatală, cât şi în cea postnatală, pentru a descrie dilatarea tractului urinar (TU), ar fi benefic în promovarea comunicării între specialităţi. Mai mult, dezvoltarea unui sistem de clasificare comun ar permite un transfer de informaţii fără ambiguităţi în interpretările specifice diverşilor furnizori care îngrijesc gravida şi sugarul, ar genera o cercetare mai riguroasă a rezultatelor pentru o mai bună corelare a constatărilor ecografice prenatale cu consecinţele specifice, cum ar fi rezoluţia dilataţiei renale, uropatiile specifice, riscurile de infecţie a tractului urinar, boala renală cronică în stadiul II sau mai avansat, hipertensiunea arterială şi proteinuria sau intervenţiile chirurgicale.
Obiectivul acestei revizuiri este de a oferi o imagine de ansamblu medicului de familie asupra managementului anomaliilor congenitale ale rinichiului şi tractului urinar (ACRTU) la copil, pentru a înţelege şi a orienta cât mai prompt pacientul pediatric cu aceste anomalii către serviciile specializate, contribuind semnificativ la prevenirea apariţiei bolii renale cronice la adult.
Anomaliile congenitale ale rinichilor şi tractului urinar (congenital anomalies of the kidneys and urinary tracts – CAKUT) sunt tulburări embrionare ce apar în timpul dezvoltării intrauterine şi care constau într-un spectru de defecte la nivelul rinichilor şi al căilor de evacuare a urinei, ce includ ureterele, vezica urinară şi uretra(1,2).
Hidronefroza antenatală (HAN) este un marker al potenţialelor anomalii renale congenitale, dar de obicei nu poate identifica o anumită boală.
Mesaje-cheie(3):
-
HAN este un marker-surogat al anomaliilor renale potenţial congenitale.
-
HAN uşoară se va rezolva adesea spontan.
-
HAN moderate până la severe sunt frecvent asociate cu ACRTU.
-
Informaţiile ultrasonografice prenatale şi postnatale sunt esenţiale pentru evaluarea postnatală şi management.
Hidronefroza antenatală, definită ca dilatarea renală a pelvisului şi/sau calicelor, este cea mai frecventă anomalie detectată prenatal ecografic, ce apare în 0,5-1% din totalul sarcinilor(4-6). Deşi este postulat în general ca un marker al ACRTU, o tulburare specifică nu a putut fi identificată. Cu toate acestea, este bine cunoscut faptul că rezultatul depinde de etiologia subiacentă. Pe de altă parte, mai mult de jumătate din cazurile de HAN se rezolvă spontan până la sfârşitul gestaţiei sau în timpul primului an de viaţă(5).
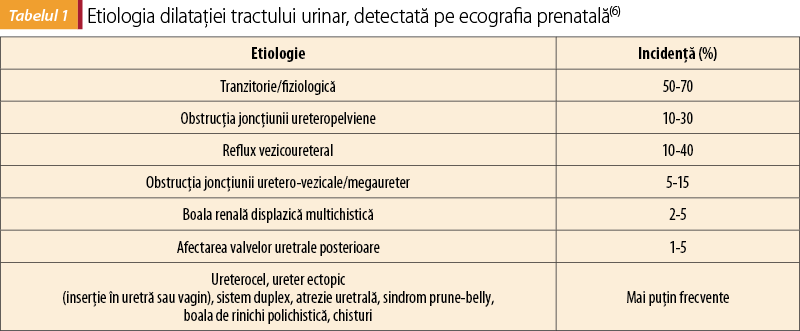
Diagnosticul diferenţial include o mare diversitate de ACRTU, variind de la anomalii uşoare, cum ar fi cele tranzitorii sau HAN izolate, la altele mai importante precum cele congenitale de grad înalt cu reflux vezicoureteral (RVU) sau obstrucţia joncţiunii ureteropelviene (OJUP)(5).
Cauza principală poate fi, de asemenea, o severă obstrucţie a tractului urinar inferior (OTUI), cum ar fi valva posterioară a uretrei (VPU), care reprezintă o îngroşare a faldurilor mucoasei uretrei posterioare, realizând astfel un obstacol în calea evacuării urinei din vezica urinară la exterior, sau sindromul prune-belly (PBS), ce necesită diagnostic şi tratament precoce, reprezentând deci o urgenţă(5).
În ciuda progreselor continue în înţelegerea bazei genetice şi a rezultatelor ACRTU, încă nu există un consens în ceea ce priveşte semnificaţia clinică, evaluarea postnatală şi managementul sugarilor cu hidronefroză antenatală(5,6). În consecinţă, sugarii care nu au patologii remarcabile fie ar fi supuşi unor intervenţii semnificativ invazive, fie ar exista riscul neglijării unei anomalii importante, eludând anumite investigaţii(5).
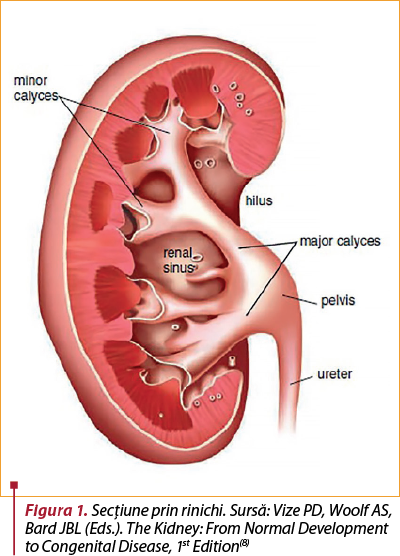
Anatomia şi fiziopatologia hidronefrozei prin obstrucţie de joncţiune ureteropelviană (OJUP)(7)
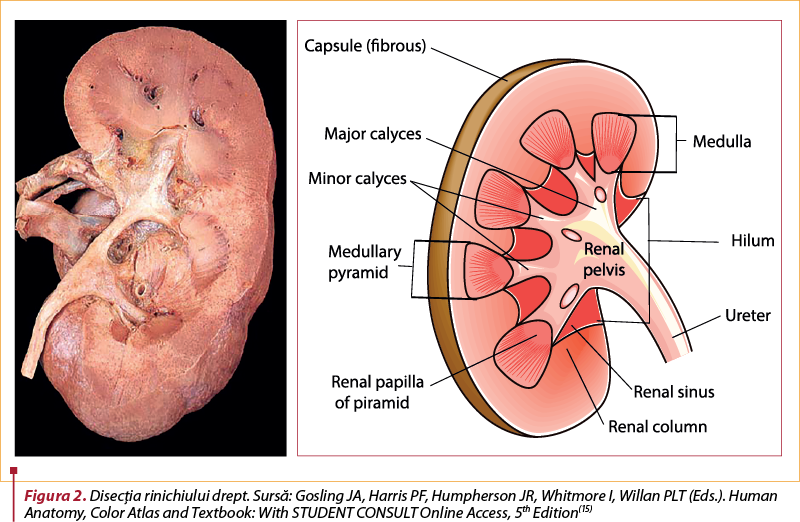
Rinichiul are două părţi principale:
1. Parenchimul renal – cea mai importantă parte care produce urină, cu două suborgane:
a) Medulara (măduva renală). Structura sa este oarecum asemănătoare cu cea a plămânului. Această parte a parenchimului renal este mai rapid expandabilă şi comprimabilă în comparaţie cu cortexul renal. În funcţie de gradul de stenoză al JUP şi de intervalul de timp, medulara devine mai scurtă şi îşi pierde forma piramidală. Limita inferioară a grosimii parenchimatoase renale normale este de 7,5 mm în perioada neonatală, 8 mm la vârsta de 1 an şi 10 mm la vârsta de 2 ani(7).
b) Cortexul (substanţa corticală). Este cea mai importantă parte funcţională a rinichiului. Grosimea normală a cortexului este >3 mm la sugari. Structura sa este oarecum similară cu cea a ficatului, relativ dură. Prin urmare, compresia sau subţierea acestuia ar determina un risc semnificativ de afectare renală. În astfel de cazuri, separarea corticomedulară se pierde, iar grosimea cortexului scade. Este un parametru obiectiv, deoarece, opus sistemului pelvicaliceal, nu este afectat de hidratare, umplerea vezicii urinare, poziţie şi respiraţie. Subţierea de lungă durată a corticalei este asociată cu funcţia renală scăzută şi cu scăderea numărului de nefroni. Prin urmare, cortexul comprimat şi subţiat sugerează leziuni renale. O grosime a cortexului mai mică de 1,5 mm – cu alte cuvinte, pierderea a mai mult de jumătate din cortex – este în cea mai mare parte asociată cu atrofie renală şi leziuni renale ireversibile(7).
2. Sistemul pelvicaliceal colectează şi trimite urina în ureter. Sistemul colector are două suborgane:
a) Pelvis renal. Complianţa pelvisului renal este foarte mare la sugari. Pelvisul renal se măreşte semnificativ pentru a proteja parenchimul renal, chiar şi la o creştere uşoară a presiunii din acest segment. Prin urmare, riscul de afectare a parenchimului renal este scăzut şi necesită timp pentru a se produce. Cu toate acestea, riscul de afectare renală este mare la cei cu complianţă scăzută a configuraţiei pelvice intrarenale.
b) Calicele renale. Comparativ cu pelvisul renal, expansibilitatea calicelor este mai mică, astfel încât dilatarea acestora înseamnă un risc mai mare de hidronefroză în comparaţie doar cu dilatarea pelvisului renal. Pe de altă parte, calicele se măresc pentru a proteja parenchimul renal.
Diagnostic
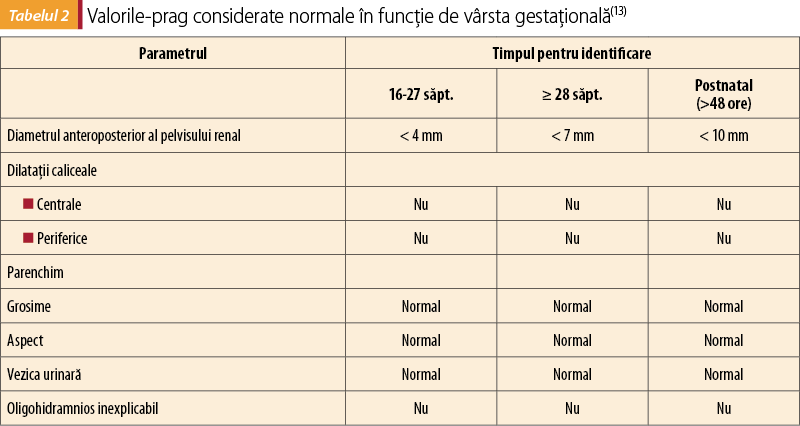
Evaluarea prenatală
Evaluarea ecografică se efectuează în mod obişnuit în timpul sarcinii, cu o medie de două ecografii pentru gravidele fără risc şi patru ecografii pentru gravidele cu risc crescut(5,9). În România, se recomandă minimum trei-patru ecografii (incluzând ecografiile morfologice) sau ori de câte ori consideră medicul obstetrician că este necesară, pe parcursul sarcinii(10). Ecografia urinară (EU) este cea mai bună metodă pentru diagnosticul şi urmărirea hidronefrozei, atât prenatal, cât şi postnatal(6). Este o metodă de examinare neinvazivă, disponibilă, rapidă, neiradiantă şi cu costuri reduse. Aceasta arată dimensiunea rinichilor, grosimea şi aspectul parenchimului (ecogenitate, diferenţiere corticomedulară, chisturi corticale), severitatea hidronefrozei, dilatarea ureterală şi anatomia vezicii urinare(6,7). Există două beneficii importante ale ultrasunetelor: 1) determină rapid prezenţa şi severitatea hidronefrozei; 2) decide momentul şi necesitatea altor intervenţii, astfel încât este important în prezent a stabili cele mai recente criterii pentru determinarea cu exactitate a severităţii hidronefrozei, pentru a putea prezice cine poate dezvolta leziuni renale şi cine are nevoie de intervenţie în comparaţie cu cine poate fi urmărit conservator(6,7).
Rinichii şi vezica urinară pot fi vizualizate în mod sigur la sfârşitul primului trimestru. Incidenţa detectării prenatale a dilataţiei TU după primul trimestru este de 1-2%, dar unele studii raportează o incidenţă de până la 5%(11).
În primul trimestru, megavezica este cel mai frecvent definită ca o dimensiune longitudinală a vezicii urinare ≥7 mm. Mai târziu, în timpul sarcinii, este adesea acceptată o dimensiune sagitală (în mm) mai mare decât vârsta gestaţională (în săptămâni) +12. Megavezica poate fi asociată cu un perete vezical îngroşat, care a fost definit ca fiind >3 mm. Oligohidramniosul este prezent în aproximativ jumătate din toate cazurile(11).
Doi factori afectează rinichiul la sugarii cu hidronefroză a joncţiunii ureteropelviene (JUPHN): complianţa pelvisului renal şi gradul de stenoză al JUP. În primul rând, hidronefroza se dezvoltă ca un răspuns anatomic protector. Dacă stenoza este severă şi persistă o perioadă lungă de timp, atunci afectarea renală apare ca răspuns funcţional(7).
Sisteme de clasificare a hidronefrozei
Din punct de vedere istoric, au existat mai multe sisteme de clasificare, în funcţie de specialitatea de studiu.
Un singur sistem de clasificare, care poate fi utilizat atât în consultaţia prenatală, cât şi în cea postnatală, pentru a descrie dilatarea tractului urinar, ar fi benefic în promovarea comunicării între specialităţi. Mai mult, dezvoltarea unui sistem de clasificare comun ar permite un transfer de informaţii fără ambiguităţi în interpretările specifice diverşilor furnizori care îngrijesc gravida şi sugarul. În plus, un sistem de clasificare comun ar genera o cercetare mai riguroasă a rezultatelor pentru o mai bună corelare a constatărilor ecografice prenatale cu consecinţele specifice, cum ar fi rezoluţia dilataţiei renale, uropatiile specifice, riscurile de infecţie a tractului urinar, boala renală cronică stadiul II sau mai avansat, hipertensiunea arterială şi proteinuria sau intervenţiile chirurgicale(6,12).
A) Diametrul anterior-posterior (AP) al pelvisului renal (APDRP)
Diametrul AP este un parametru variabil, deoarece pelvisul renal este extrem de dinamic, înregistrând modificări semnificative în funcţie de hidratare, umplerea vezicii urinare, poziţie (decubit dorsal) şi respiraţie, astfel încât măsurarea diametrului AP al pelvisului renal nu este standardizată, existând un consens doar la 64% dintre medici(7). Unii ecografişti măsoară diametrul AP în cel mai mare punct al pelvisului renal, în timp ce alţii îl măsoară în plan vertical. Cu toate acestea, APDRP este măsurată în mare parte la marginea parenchimului (hilus), în timpul secţiunii transversale a rinichiului(7).
Dezavantaje/limite ale măsurării APDRP(7):
-
Rata diferenţelor operatorilor este foarte mare.
-
Diametrul AP este mic la sugarii deshidrataţi.
-
Diametrul AP este mic în vezica goală.
-
Diametrul AP este mic în expir.
-
Diametrul AP măsurat în decubit dorsal este departe de a fi perfect.
-
Diametrul AP (chiar mic) este foarte riscant în prezenţa configuraţiei pelviene intrarenale.
Hidronefroza poate fi moderată chiar dacă diametrul AP este mare la sugarii cu configuraţie pelviană extrarenală (pelvisul renal se găseşte în afara grosimii parenchimului renal). Pe de altă parte, hidronefroza poate fi foarte severă, cu subţierea semnificativă a parenchimatosului, chiar dacă diametrul AP este redus la sugarii cu configuraţie pelviană intrarenală (pelvisul renal se află în interiorul parenchimului renal). Prin urmare, atunci când calitatea parenchimului, care este cel mai important factor în determinarea gradului de hidronefroză, este omisă şi diametrul AP în sine este acceptat ca singura constatare a severităţii hidronefrozei, unii sugari pot suferi o intervenţie chirurgicală inutilă, în timp ce unii pot avea afectare renală permanentă, din cauza întârzierii unei intervenţii chirurgicale prompte(7).
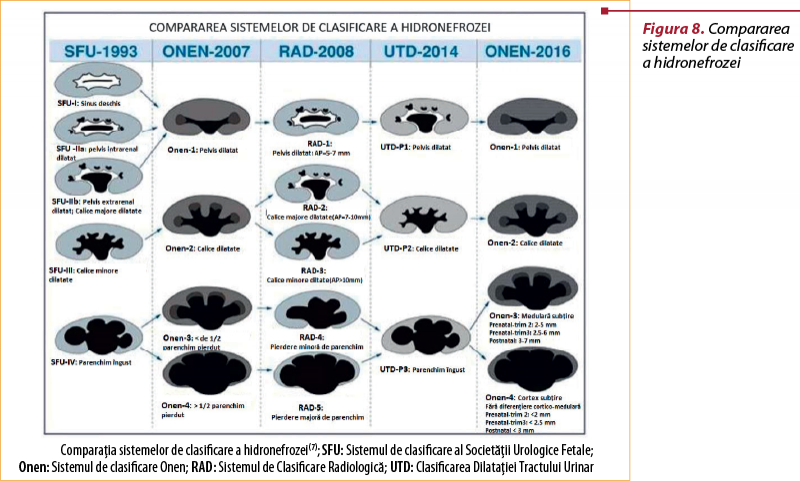
B) Sistemul de clasificare al Societăţii de Urologie Fetală (SFU)
Acest sistem de clasificare a fost dezvoltat în 1993. Este cantitativ şi subiectiv. Toate gradele SFU sunt extrem de variabile între operatori şi clinicieni. Prin urmare, nu este popular între alte discipline, decât la urologii pediatri(7).
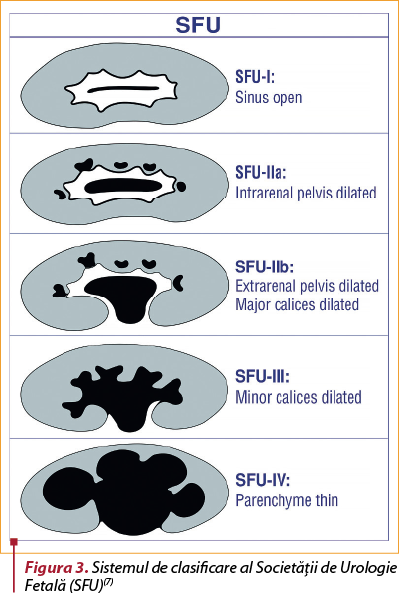
Dezavantaje/limite ale clasificării SFU(7):
-
SFU-1 şi SFU-2a. Ambele indică grade diferite de dilatare pelviană renală. Prin urmare, este confuz şi foarte dificil să se diferenţieze unul de celălalt. Mai mult, urmărirea, tratamentul şi prognosticul acestor două grade sunt similare; toate se rezolvă spontan, fără afectare renală.
-
SFU-2b şi SFU-3. Ambele reprezintă grade diferite de dilatare caliceală. Este foarte dependent de operator în diferenţierea dilataţiei calicelor periferice (minore) de cele majore, din cauza unei discrepanţe mari de interpretare între operatori.
-
SFU-3. Deşi reprezintă doar dilatarea caliceală, imaginile folosite pentru SFU-3 în articolul original arată clar subţierea severă a medularei. Acest lucru provoacă o confuzie semnificativă în rândul medicilor şi al radiologilor.
-
SFU-4. Reprezintă subţierea minimă a parenchimului medular (de exemplu, 6 mm) şi subţierea severă a parenchimului cortical (de exemplu, 2 mm) şi rinichi hidronefrotici asemănători chistului de acelaşi grad. Definiţia largă a SFU-4 nu reuşeşte să demonstreze cu acurateţe severitatea hidronefrozei şi, prin urmare, induce în eroare în privinţa unui tratament prompt. Nu sugerează cine are nevoie de intervenţie chirurgicală şi cine poate fi urmărit în siguranţă nonoperator. Primul exemplu (medulara subţire) poate fi urmărit în siguranţă nonoperator, în timp ce al doilea (cortex subţire) necesită în mod clar o intervenţie chirurgicală. Această definiţie largă face prognosticul dificil de prezis în cazurile de JUPHN.
C) Sistemul de clasificare radiologică(7)
Sistemul de gradare radiologică a fost parţial modificat de SFU pentru utilizare postnatală. Are acelaşi sistem de notare ca SFU; în plus, include diametrul AP pentru gradele 1, 2 şi 3. Acest sistem de clasificare împarte pierderea parenchimului în două grade diferite, sugerând importanţa parenchimului renal pentru a determina severitatea hidronefrozei, clasificare oarecum similară sistemului de notare Onen. Hidronefroza de gradul 4 reprezintă o pierdere uşoară a parenchimului; gradul 5 semnifică pierderea severă a parenchimului.
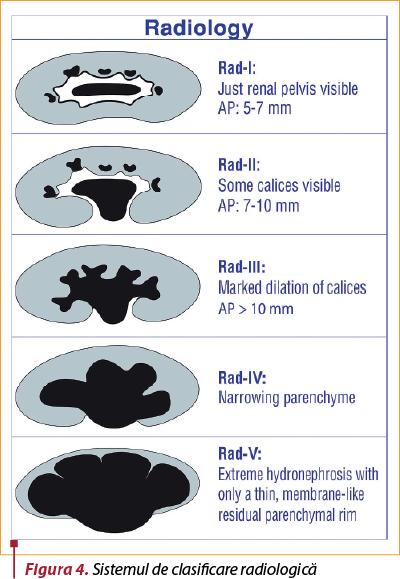
Dezavantaje/limite ale sistemului de clasificare radiologică(7):
-
Gradele 1 şi 2 de radiologie (SFU-1 şi SFU-2a). Ambele indică grade diferite de dilatare pelviană renală. Prin urmare, este confuz şi foarte dificil să se diferenţieze unul de altul. Mai mult, urmărirea, tratamentul şi prognosticul acestor două grade sunt similare; toate se rezolvă spontan fără afectare renală.
-
Utilizarea diametrului AP face acest sistem de clasificare şi mai confuz, deoarece gradele SFU şi diametrul AP nu sunt corespondente pentru mulţi pacienţi, în funcţie de diferitele configuraţii pelviene renale.
-
Gradele 4 şi 5 radiologice. Gradul 4 reprezintă o pierdere uşoară a parenchimului, în timp ce gradul 5 reprezintă o pierdere severă a parenchimului. Este complet dependent de operator, nu este decisiv şi nu diferenţiază clar clasele 4 şi 5.
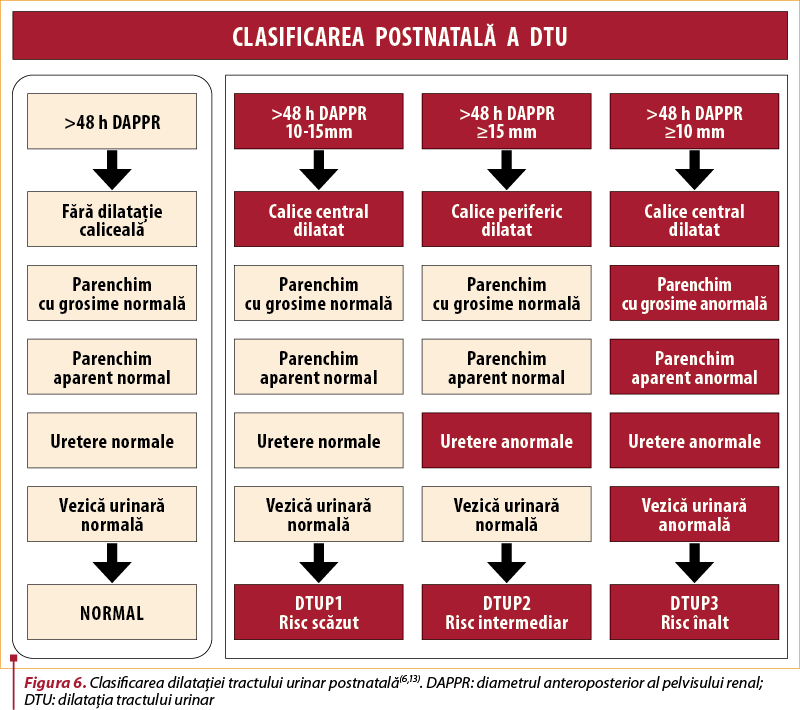
D) Clasificarea dilataţiei tractului urinar – DTU (urinary tract dilation – TUD)
DTU a fost creat retrospectiv pe baza revizuirii, combinării şi rezumării literaturii actuale, deci nu este un sistem de clasificare bazat pe dovezi(7). Această clasificare a fost formată în urma colaborării a opt societăţi: Colegiul American de Radiologie (ACR), Institutul American de Ultrasunete în Medicină (AIUM), Societatea Americană de Nefrologie Pediatrică (ASPN), Societatea de Urologie Fetală (SFU), Societatea de Medicină Materno-Fetală (SMFM), Societatea de Urologie Pediatrică (SPU), Societatea de Radiologie Pediatrică (SPR) şi Societatea Radiologilor în Ultrasunete (SRU)(6).
Prin urmare, în martie 2014, a fost organizat un meeting de consens, convocat pentru a unifica descrierile DTU şi pentru a crea o schemă standardizată pentru ecografia perinatală şi postnatală în evaluarea sugarului(6). Principalul obiectiv al consensului a fost acela de a crea un sistem de clasificare care să includă parametrii ecografici pentru tractul urinar (TU) aplicabili atât fătului, cât şi copiilor, care pot standardiza limbajul atât al ecografistului, cât şi al clinicianului cu metodele de evaluare şi măsurare a rinichilor şi căilor urinare, pentru a descrie o boală într-un mod unic(13).
Sistemul de clasificare DTU utilizează şase rezultate ecografice pentru a descrie tractul urinar(14):
1. Diametrul anteroposterior al pelvisului renal (DAPPR).
2. Dilatare caliceală, cu distincţie între calicele central şi calicele periferice postnatale.
3. Grosimea parenchimului renal.
4. Aspectul parenchimatos renal (distincţie între corticală şi medulară).
5. Anomalii ale vezicii urinare.
6. Anomalii ureterale.
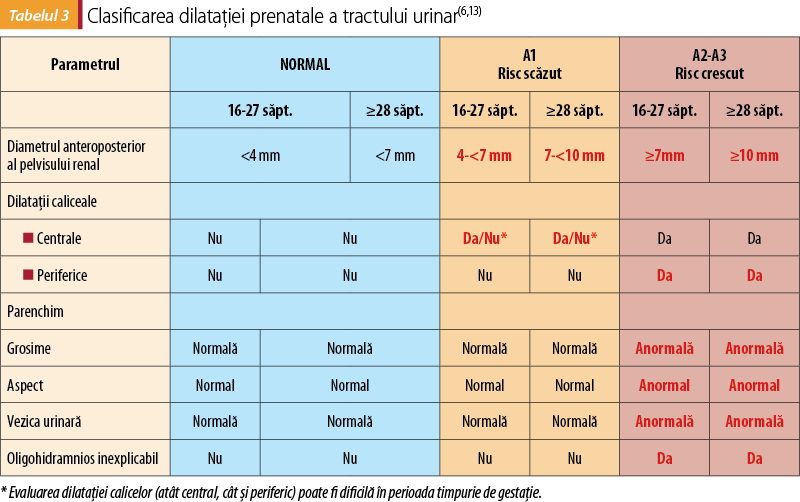
Antenatal (aplicabil după 16 săptămâni de gestaţie):
DTU A1
-
Diametrul pelvian renal anteroposterior
-
16 până la 27 de săptămâni: 4 mm până la <7 mm
-
≥28 de săptămâni: 7 mm până la <10 mm.
-
Cu sau fără dilatarea caliceală centrală.
DTU A2-3
-
Diametrul pelvian renal anteroposterior
-
16 până la 27 de săptămâni: ≥7 mm
-
≥28 de săptămâni: ≥10 mm.
-
Dilataţie caliceală periferică.
-
Grosimea sau aspectul anormal al parenchimului.
-
Ureter sau vezică urinară anormală.
-
Oligohidramnios inexplicabil.
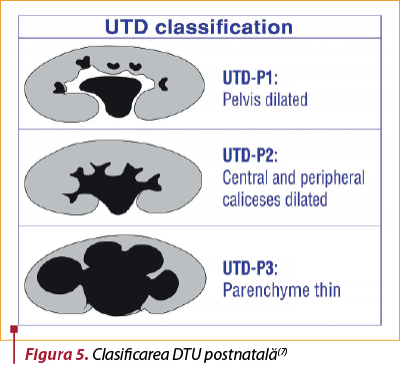
Postnatal (aplicabil după 48 de ore de viaţă):
DTU P1 (risc scăzut)
-
Diametrul pelvian renal anteroposterior 10 mm până la <15 mm.
-
Dilataţie caliceală centrală.
DTU P2 (risc intermediar)
-
Diametrul pelvian renal anteroposterior ≥15 mm.
-
Dilataţie caliceală periferică.
-
Ureterul anormal.
DTU P3 (risc ridicat)
-
Diametrul pelvian renal anteroposterior ≥15 mm.
-
Dilataţie caliceală periferică.
-
Grosime sau aspect parenchimatos anormal.
-
Ureterul anormal.
-
Vezica urinară anormală.
Dezavantajele/limitările clasificării DTU
-
Lipsa corelaţiei dintre perioada prenatală şi postnatală în ceea ce priveşte definirea şi clasificarea DTU(13).
-
Calicele centrale şi periferice: depinde de operator pentru a diferenţia dilatarea calicelor periferice (minore) de cele centrale (majore)(7).
-
DTU-P3. La fel ca în clasificarea SFU, reprezintă subţierea minimă a parenchimului medular (de exemplu, 6 mm) şi subţierea severă a parenchimului cortical (de exemplu, 2 mm) cu rinichi hidronefrotici asemănători chistului de acelaşi grad. Definiţia largă a DTU-P3 nu reuşeşte să demonstreze cu acurateţe severitatea hidronefrozei şi, prin urmare, induce în eroare privind necesitatea tratamentului prompt. Nu sugerează cine are nevoie de tratament chirurgical şi cine poate fi urmărit conservator. Primul caz (medulara subţire) poate fi urmărit în siguranţă non-operator, în timp ce al doilea (cortex subţire) necesită în mod clar o intervenţie chirurgicală. Această definiţie largă face prognosticul dificil de prezis în cazurile de JUPHN(7).
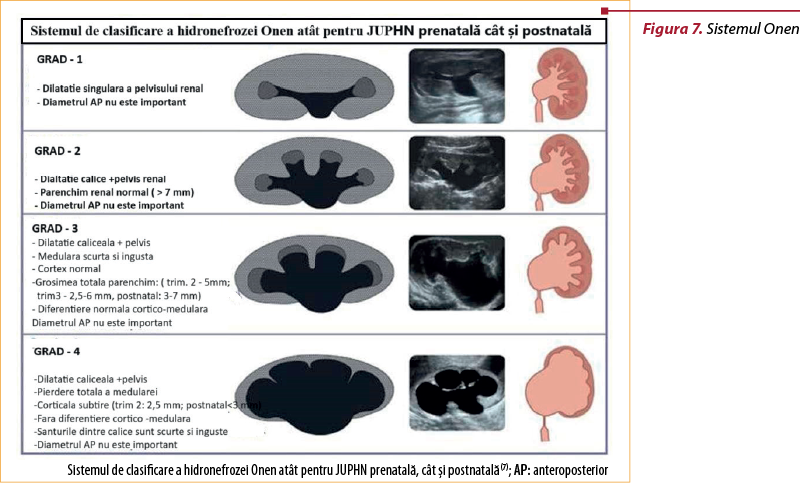
E) Sistemul de clasificare Onen
Acest sistem de clasificare a fost dezvoltat atât pentru JUPHN prenatală, cât şi postnatală. Este adecvat şi aplicabil atât pentru făt, cât şi pentru copii, standardizând limbajul ecografiştilor, clinicienilor, metoda de evaluare şi măsurarea rinichilor. Sistemul de notare Onen este terminologic simplu şi clar. Prin urmare, toate disciplinele, inclusiv radiologie, perinatologie, nefrologie pediatrică şi urologie pediatrică, îl pot utiliza cu uşurinţă nu numai pentru practica clinică, ci şi pentru cercetările viitoare(7).
Protocolul de tratament şi urmărire pentru JUPHN bazat pe sistemul de notare Onen(7):
-
Cazurile de JUPHN Onen-1 nu necesită evaluare invazivă şi nici tratament chirurgical sau antibiotic datorită naturii lor benigne; tot ce au nevoie este urmărirea doar cu ultrasunete. Este suficientă o ecografie urinară detaliată la 1-3-6 luni postnatal, un an şi doi ani. Dacă Onen-1 nu creşte sau nu se rezolvă, urmărirea poate fi întreruptă(7).
-
Cazurile Onen-2 JUPHN nu necesită evaluare invazivă şi nici antibiotic datorită naturii lor benigne; tot ce au nevoie este urmărirea doar cu ultrasunete. Cu toate acestea, aproximativ 10% dintre aceşti sugari se vor agrava şi vor avea nevoie de pieloplastie în timpul urmăririi. Prin urmare, aceste cazuri ar putea fi urmărite cu ultrasunete mai îndeaproape, comparativ cu cele de hidronefroză Onen-1. Este suficientă o ecografie urinară detaliată la 1-3-6 luni postnatal şi la fiecare şase luni până la vârsta de 3 ani. Dacă Onen-2 scade la Onen-1 sau se rezolvă, urmărirea poate fi întreruptă. Dacă Onen-2 persistă, o ecografie poate fi efectuată anual până la vârsta de 5 ani şi apoi urmărirea poate fi întreruptă prin informarea pacienţilor despre simptome precum durerea sau ITU(7).
-
Pacienţii cu JUPHN Onen-3 (medulă subţire, parenchim renal de 3-7 mm) au nevoie de o urmărire atentă, inclusiv scanare renală, deoarece aproximativ o treime dintre aceşti copii au nevoie de pieloplastie în timpul urmăririi. Este rezonabilă o ecografie urinară detaliată în prima lună postnatal, la fiecare trei luni până la vârsta de 2 ani şi la fiecare şase luni până la vârsta de 3 ani. Dacă Onen-3 asimptomatic persistă până la vârsta de 3 ani, cu funcţie renală normală, există două opţiuni de discutat cu familia; 1) se continuă urmărirea invazivă până la vârsta adultă, 2) pieloplastie, cu mare succes, prevenirea urmăririi invazive de lungă durată şi antibioprofilaxia. Dacă Onen-3 este diagnosticat, se recomandă o scanare renală. Dacă funcţia şi aspectul (la ecografie) ale rinichiului ipsilateral, precum şi ale rinichiului contralateral sunt normale, se continuă urmărirea, cu repetarea ecografiei la trei luni. Dacă Onen-3 scade sau se stabilizează, se urmăreşte pacientul la trei luni; dacă Onen-3 se înrăutăţeşte, se recomandă o a doua scanare renală pentru aprecierea funcţiei renale. Dacă funcţia este sub 35 sau scade cu mai mult de 10 unităţi, se recomandă pieloplastia(7).
-
Pacienţii cu JUPHN Onen-4 (cortex subţire, parenchim renal <3 mm, fără diferenţiere corticomedulară) au nevoie de corecţie chirurgicală după o perioadă scurtă de urmărire (1-3 luni). Corecţia chirurgicală promptă, în timp util, promite o îmbunătăţire a deprecierii funcţiei renale(7).
Autor pentru corespondenţă: Iuliana Picioreanu E-mail: ipicioreanu@gmail.com
CONFLICT DE INTERESE: niciunul declarat.
SUPORT FINANCIAR: niciunul declarat.
Acest articol este accesibil online, fără taxă, fiind publicat sub licenţa CC-BY.

Bibliografie
-
Murugapoopathy V, Gupta IR. A Primer on Congenital Anomalies of the Kidneys and Urinary Tracts (CAKUT). Clin J Am Soc Nephrol. 2020;15:723–31.
-
Isert S, Müller D, Thumfart J. Factors Associated With the Development of Chronic Kidney Disease in Children With Congenital Anomalies of the Kidney and Urinary Tract. Front Pediatr. 2020;8:298.
-
Oliveira EA, Oliveira MCL, Mak RH. Evaluation and management of hydronephrosis in the neonate. Curr Opin Pediatr. 2016;28:195-201.
-
Bessa J de, Rodrigues CM, Chammas MC, et al. Diagnostic accuracy of Onen’s Alternative Grading System combined with Doppler evaluation of ureteral jets as an alternative in the diagnosis of obstructive hydronephrosis in children. PeerJ. 2018;6:e4791.
-
Yalçınkaya F, Özçakar ZB. Management of antenatal hydronephrosis. Pediatr Nephrol. 2020;35:2231-9.
-
Nguyen HT, Benson CB, Bromley B, et al. Multidisciplinary consensus on the classification of prenatal and postnatal urinary tract dilation (UTD classification system). J Pediatr Urol. 2014;10:982-98.
-
Onen A. Grading of Hydronephrosis, An Ongoing Challenge. Front Pediatr. 2020;8:458.
-
Vize PD, Woolf AS, Bard JBL (Eds.). The Kidney: From Normal Development to Congenital Disease, 1st Edition. Academic Press, 2003.
-
Li Z-Y, Chen Y-M, Qiu L-Q, et al. Prevalence, types, and malformations in congenital anomalies of the kidney and urinary tract in newborns, A retrospective hospital-based study. Ital J Pediatr. 2019;45:50.
-
Ministerul Sănătăţii - MS. Protocolul privind metodologia efectuării consultaţiei prenatale şi postnatale documentate în carnetul gravidei. https://lege5.ro/gratuit/ha4dgnruga2a/protocolul-privind-metodologia-efectuarii-consultatiei-prenatale-si-postnatale-documentate-in-carnetul-gravidei-din-23082021, 2021. (https://lege5.ro/gratuit/ha4dgnruga2a/protocolul-privind-metodologia-efectuarii-consultatiei-prenatale-si-postnatale-documentate-in-carnetul-gravidei-din-23082021).
-
Taghavi K, Sharpe C, Stringer MD. Fetal megacystis, A systematic review. J Pediatr Urol. 2017;13:7-15.
-
Melo FF, Mak RH, Simões E Silva AC, et al. Evaluation of Urinary Tract Dilation Classification System for Prediction of Long-Term Outcomes in Isolated Antenatal Hydronephrosis, A Cohort Study. J Urol. 2021;206:1022-30.
-
Pelliccia P, Sferrazza Papa S, Cavallo F, et al. Prenatal and postnatal urinary tract dilation, Advantages of a standardized ultrasound definition and classification. J Ultrasound. 2019;22:5-12.
-
Bell D, Jin T. Urinary tract dilatation classification. In: Radiopaedia.org: Radiopaedia.org, 2005.
-
Gosling JA, Harris PF, Humpherson JR, Whitmore I, Willan PLT (Eds.). Human Anatomy, Color Atlas and Textbook: With STUDENT CONSULT Online Access, 5th Edition. Elsevier, 2008.
Articole din ediţiile anterioare
Diabetul gestaţional - efectele asupra mamei și copilului
Diabetul gestațional afectează 3-9% din sarcini. Implicațiile acestuia pentru viitorul mamei și al copilului sunt uriașe, întrucât crește riscul c...
Evaluarea clinică şi managementul cefaleei pacientului pediatric
Cefaleea este una din patologiile frecvent întâlnite în practica medicală şi unul din simptomele obişnuite de prezentare a pacienţilor pediatric...
Endometrioza – importanţa diagnosticului precoce
Endometrioza este o boală complexă, benignă, care afectează femeile de vârstă reproductivă.
Dermatita atopică
Dermatita atopică este o boală inflamatorie cutanată cronică, asociată cu prurit intens, care apare cel mai frecvent la copii. În principal, factor...