Osteoporosis remains a public health issue due to the predisposition of the affected bone to fracture. At present, it is one of the leading causes of morbidity and mortality among the elderly worldwide. We intend to present a different aspect of osteoporosis types and their clinical evaluation based on biochemical markers, a useful tool for healthcare practitioners involved in the management of this pathology. This article presents more than osteoporosis in menopause. This short review of osteoporosis presents osteoporosis during pregnancy, osteoporosis and immobilization, drug-induced osteoporosis and osteoporosis in rheumatic diseases.
O incursiune în diferitele tipuri de osteoporoză şi scorurile utilizate pentru calcularea riscului de fractură
A glimpse of different types of osteoporosis and the scores used for fracture risk calculation
First published: 30 noiembrie 2021
Editorial Group: MEDICHUB MEDIA
DOI: 10.26416/Med.144.6.2021.2023
Abstract
Rezumat
Osteoporoza rămâne o problemă de sănătate publică, din cauza predispoziţiei osului afectat la fractură. Aceasta este în prezent una dintre principalele cauze de morbiditate şi mortalitate în rândul vârstnicilor din întreaga lume. Dorim să prezentăm diferite aspecte ale tipurilor de osteoporoză şi evaluarea clinică a acesteia pe baza markerilor biochimici, un instrument util pentru practicienii din domeniul sănătăţii implicaţi în managementul acestei patologii. Articolul prezintă mai mult decât osteoporoza în menopauză. Această recenzie scurtă despre osteoporoză prezintă osteoporoza în timpul sarcinii, osteoporoza şi imobilizarea, osteoporoza indusă de medicamente şi osteoporoza în bolile reumatismale.
Introducere
Osteoporoza este o boală sistemică, fiind caracterizată prin scăderea masei osoase pe unitatea de volum, compromiţând rezistenţa osului. Osteoporoza rămâne o problemă de sănătate publică, din cauza predispoziţiei osului afectat de a se fractura, cu consecinţe sociale şi medicale, şi poate contribui la reducerea speranţei de viaţă(1). Aceasta este în prezent una dintre principalele cauze indirecte de morbiditate şi mortalitate în rândul vârstnicilor din întreaga lume, ducând la scăderea calităţii vieţii(2).
În osteoporoză, oasele au o structură histologică normală; totuşi, masa tisulară este scăzută, ceea ce face ca oasele să fie mai puţin rezistente şi, prin urmare, predispuse la fracturi, chiar şi după traumatisme minore. Fracturile capului şi gâtului femurului, fracturile canalului radiocarpian şi fracturile prin compresie ale vertebrelor sunt leziuni ce afectează şi imobilizează frecvent pacienţii în vârstă în scaune cu rotile(3). Persoanele cu fracturi au un risc mai mare de deces, nu direct din cauza fracturii, ci a complicaţiilor spitalizării, imobilizării, riscului crescut de pneumonie, tromboză pulmonară şi embolie. Din cauza complexităţii extreme a diagnosticului, dorim să prezentăm diferite aspecte ale tipurilor de osteoporoză şi evaluarea clinică a acestora prin intermediul markerilor biochimici, un instrument util pentru practicienii din domeniul sănătăţii implicaţi în managementul acestei patologii, medici de familie, ginecologi, medici de recuperare medicală şi endocrinologi.
Aspecte importante ale diferitelor tipuri de osteoporoză
Osteoporoza poate fi cauzată fie de o creştere a resorbţiei osoase, fie de o scădere a ratei de formare a osului. Acest dezechilibru al activităţii celulelor osteoblastice şi osteoclastice apare în principal prin alterarea mecanismelor de reglare, în primul rând prin intervenţia factorilor hormonali(2). În funcţie de modul în care este afectat osul, osteoporoza este împărţită în două tipuri.
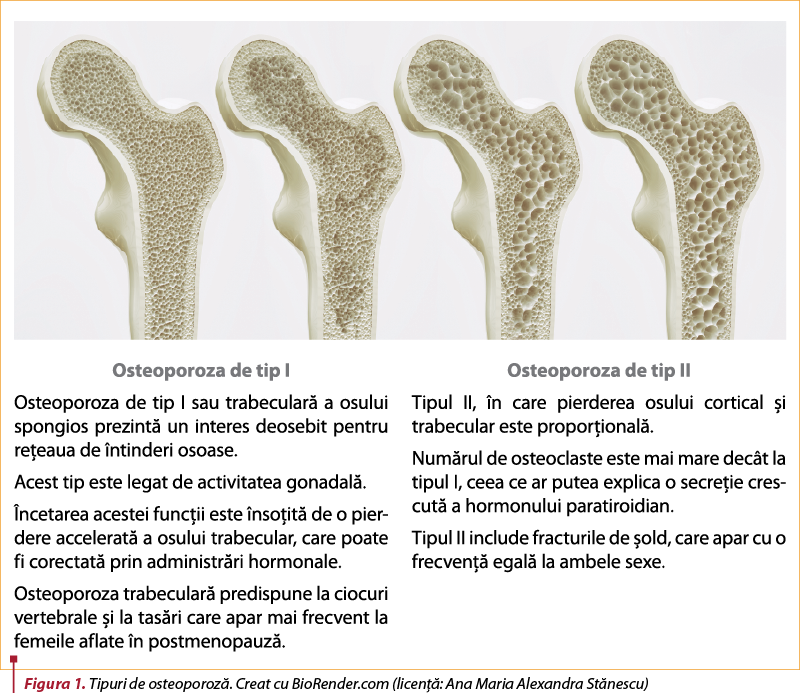
Osteoporoza de tip I sau trabeculară a osului spongios prezintă un interes deosebit privind reţeaua de canaliculi osoşi. Acest tip este legat de activitatea gonadală. Încetarea acestei funcţii este însoţită de o pierdere accelerată a osului trabecular, care poate fi corectată prin administrări hormonale(4). Osteoporoza trabeculară predispune la ciocuri vertebrale şi tasări ce apar mai frecvent la femeile aflate în postmenopauză.
Osteoporoza de tip II – pierderea osului cortical şi trabecular este proporţională. În cadrul acestui tip, numărul de osteoclaste este mai mare decât la tipul I, ceea ce ar putea explica o secreţie crescută a hormonului paratiroidian. Tipul II include fracturile de şold, ce apar cu o frecvenţă egală la ambele sexe.
Din punct de vedere etiologic, osteoporoza poate fi primară sau secundară. Formele primare, care nu recunosc o cauză definitivă, includ cea mai comună formă a involuţiei. Formele juvenile şi idiopatice prezente la adulţii tineri fac, de asemenea, parte din această categorie.
În formele secundare, osteoporoza este o manifestare a unei boli care poate fi foarte variată ca etiologie. Poate fi însoţită de osteoporoza din unele afecţiuni endocrine (hipercorticism, hipotiroidism, hipogonadism, diabet de tip 1, acromegalie etc.), afecţiuni digestive (criză biliară primitivă, malabsorbţie etc.), medicamente din terapii cronice (glucocorticoizi, hormoni tiroidieni etc.), heparină, anticonvulsivante, metotrexat, boli reumatismale (artrită reumatoidă, spondilită anchilozantă etc.), factori nutriţionali (aport scăzut de calciu, alimentaţie vegetariană, malnutriţie, scorbut etc.), alte cauze (fumat, alcoolism, imobilizare, hipoponderalitate etc.).
Diferenţele dintre tipurile de osteoporoză de tip I şi de tip II sunt prezentate în figura 1.
Osteoporoza din postmenopauză şi de involuţie
În jurul vârstei de 50 de ani, începe pierderea osoasă fiziologică, femeile pierzând aproximativ 35-40% din osul cortical şi aproximativ 55-60% din osul trabecular, iar bărbaţii, cu aproximativ o treime mai puţin. Se estimează că o persoană în jurul vârstei de 80 de ani are aproximativ jumătate din cantitatea de os pe care o avea la 30-35 de ani. Osteoporoza la menopauză interesează în special osul trabecular, în timp ce osteoporoza la vârstnici este atât corticală, cât şi trabeculară(5).
Osteoporoza de vârstă apare prin scăderea activităţii osteoblastelor şi mai puţin prin creşterea numărului de osteoclaste(6). Calcitonina, inhibitorul major al resorbţiei osteoclastice, prezintă o scădere a nivelului său bazal odată cu vârsta, indiferent de sex(7). În acest context, dezechilibrul dintre funcţiile celor două tipuri de celule favorizează pierderea osoasă(6,8).
Organismul vârstnicilor are un comportament particular în ceea ce priveşte metabolismul vitaminei D – şi anume, conversia formei inactive (25-hidroxivitamina D) în forma activă (1,25-dihidroxivitamina D)(9) are loc în mod normal la nivelul rinichilor, sub influenţa hormonului paratiroidian, în timp ce la vârstnici enzima responsabilă de această conversie scade odată cu vârsta (sau scade reactivitatea la acţiunea hormonului), determinând creşteri progresive ale hormonului paratiroidian, fenomen care accelerează resorbţia osoasă. Se adaugă, de asemenea, limitarea efortului fizic, cu repercusiuni asupra masei musculare şi osoase, o dietă săracă în proteine şi fosfor, dar şi restricţia calorică la cei care urmează diete(6). În acest context, suplimentarea cu calciu ar trebui să crească de la 1 la 1,5 g/zi la vârstnici.
Osteoporoza nutriţională este cauzată de aportul deficitar de calciu, fosfor, proteine şi vitamine şi de consumul cronic de alcool(10) (prin malnutriţie şi influenţele pe care le are asupra tractului digestiv – gastrită atrofică, scăderea absorbţiei intestinale a calciului). Sunt cunoscute homeostazia calciului şi stările fiziologice din sarcină şi alăptare(11), situaţii în care necesarul de calciu se dublează sau chiar se triplează şi scade masa osoasă, cu apariţia osteoporozei de sarcină, tranzitorie.
Osteoporoza prin imobilizare se caracterizează printr-o scădere profundă şi rapidă a masei osoase locale sau generale. Imobilizarea completă după o perioadă de şase luni produce o pierdere de o treime din masa osoasă preexistentă, crescând semnificativ calciul, şi duce la pierderea semnificativă a osului trabecular(12).
Osteoporoza indusă de medicamente apare după cure de lungă durată cu anumite medicamente(13). Printre acestea, heparina induce pierderea osoasă din cauza influenţelor negative pe care le are medicamentul asupra metabolismului mucopolizaharidelor din colagen, ce devine impropriu pentru fixarea calciului(14).
Atunci când sunt utilizate în cure de lungă durată, alte medicamente cu potenţial osteoporotic sunt fenitoina, barbituricele, metalele grele, hidroxidul de aluminiu şi metotrexatul(15) (prin efectul său citotoxic şi de calciu).
Osteogeneza imperfectă. Acest grup include suferinţele caracterizate de o imposibilitate (genetică) de a forma un colagen normal calitativ şi cantitativ. Cele mai multe defecte au fost găsite în colagenul de tip I(16). Susceptibilitatea sau multe fracturi cu deformări osoase ghidează diagnosticul, în special atunci când apar la tineri(17).
Osteoporoza este secundară altor boli. Orice suferinţă cronică de consum provoacă osteoporoză prin imobilizare şi malnutriţie. Dacă pacientul urmează terapie cu cortizon, acesta este un factor agravant(18). De asemenea, printre aceste boli se numără insuficienţa renală cronică, mielomul multiplu, limfomul malign Hodgkin, leucemia limfocitară cronică, sindromul Cushing şi hiperparatiroidismul(19).
Osteoporoza şi infecţia cu virusul imunodeficienţei umane (HIV). Mulţi factori contribuie la creşterea riscului de fractură la pacienţii cu HIV, inclusiv factorii de risc tradiţionali şi factorii HIV intrinseci(20). Factorii asociaţi clasic cu masa osoasă scăzută şi fracturi, cum ar fi vârsta, fractura anterioară, căderile, indicele de masă corporală scăzut, abuzul de alcool şi fumatul, sunt adesea prezenţi în patologia pacienţilor cu HIV(21). Unii factori de risc, cum ar fi deficienţa de vitamina D(9) şi diabetul, sunt mai des întâlniţi la aceşti indivizi şi, de asemenea, pot contribui la apariţia osteoporozei. Bărbaţii care trăiesc cu HIV au adesea niveluri scăzute de testosteron seric, iar pacienţii HIV-pozitivi au o rezistenţă mai mare la insulină. Riscul de a dezvolta diabet la pacienţii seropozitivi este de 1,4 ori mai mare decât la populaţia generală(22). Alte comorbidităţi contribuie la acestea, prin creşterea riscului de fractură la pacienţii cu HIV. Funcţia musculară afectată este o descoperire foarte frecventă în HIV şi poate ajuta la creşterea riscului de căderi şi fracturi(23). Studiul multicentric de cohortă SIDA (MACS) a raportat o scădere accelerată a forţei musculare şi a mersului la subiecţii HIV-pozitivi după vârsta de 50 de ani, comparativ cu subiecţii HIV-negativi(24).
Numărul scăzut de limfocite CD4 a fost asociat în mod constant cu un risc crescut de osteoporoză şi fracturi. Pacienţii cu mai puţin de 200 de limfocite CD4/mm3 au un risc de fractură mai mare decât indivizii cu un număr mai mare de limfocite CD4(25). Coinfecţia HIV cu hepatita B sau C creşte şi riscul de fractură. La persoanele cu HIV care sunt coinfectate cu virusul hepatitei C(26), riscul de fracturi este de două ori mai mare decât la persoanele infectate numai cu HIV. Coinfecţia cu virusul hepatitei B creşte şi riscul de fractură la pacienţii HIV-pozitivi; în plus, tratamentul cu antiretrovirale(27) şi/sau interferon alfa este asociat cu o masă osoasă scăzută şi cu o frecvenţă crescută a fracturilor(28).
Osteoporoza din boli reumatice. Acestea implică factori multipli: activitate inflamatorie prelungită, tratament cu corticosteroizi şi alte medicamente osteopenice, imobilizare, deficit de vitamina D, asocierea insuficienţei renale şi amenoree la femeile cu lupus eritematos sistemic(29,30).
Evaluarea riscului de fractură (scor FRAX®) şi markeri biochimici ai metabolismului osos
Scorul de evaluare a riscului de fractură este un scor simplu, bazat pe calcularea riscului de fractură în următorii zece ani, recomandat de Organizaţia Mondială a Sănătăţii(31). Acest scor calculează riscul de fractură pentru următorii zece ani ai unei persoane ţinând cont doar de factorii clinici de risc sau în combinaţie cu densitatea minerală osoasă a colului femural (DMO) (g/cm2). Factorii clinici de risc sunt vârsta, sexul, greutatea, prezenţa fracturilor de fragilitate după 45-50 de ani(32), statutul de fumător, consumul de alcool, antecedentele familiale de fracturi, imobilizarea, tratamentul cu hormoni glucocorticoizi, poliartrita reumatoidă şi osteoporoza secundară. Dacă se adaugă valoarea DMO(33) măsurată la şold, predicţia pentru riscul de fractură creşte.
Este important de menţionat că scorul FRAX® subestimează riscul de fractură viitoare, deoarece raportează riscul doar pentru fracturile de şold şi fracturile majore, care cuprind aproximativ jumătate din toate fracturile de fragilitate(31). În plus, riscul de subestimare a FRAX® la pacienţii cu fracturi multiple legate de osteoporoză, fracturi recente şi DMO la nivelul coloanei lombare este mult mai mic decât DMO a colului femural, la cei cu osteoporoză secundară şi cei cu risc crescut de cădere.
Căderile sunt cauza principală a majorităţii fracturilor la adulţii în vârstă(34,35). Pentru persoanele cu antecedente de cădere, scorul de risc de fractură Garvan, deşi bazat pe date mult mai puţine decât FRAX®(36), poate fi utilizat pentru a obţine o perspectivă asupra riscului de fractură viitoare(35).
Diagnosticul clinic al osteoporozei este adesea tardiv, iar din acest motiv este necesară utilizarea metodelor paraclinice de explorare pentru a evidenţia pierderea osoasă şi a permite diagnosticul diferenţial cu alte cauze de resorbţie osoasă(37).
Figura 2 prezintă markeri biochimici ai resorbţiei osoase în osteoporoză.
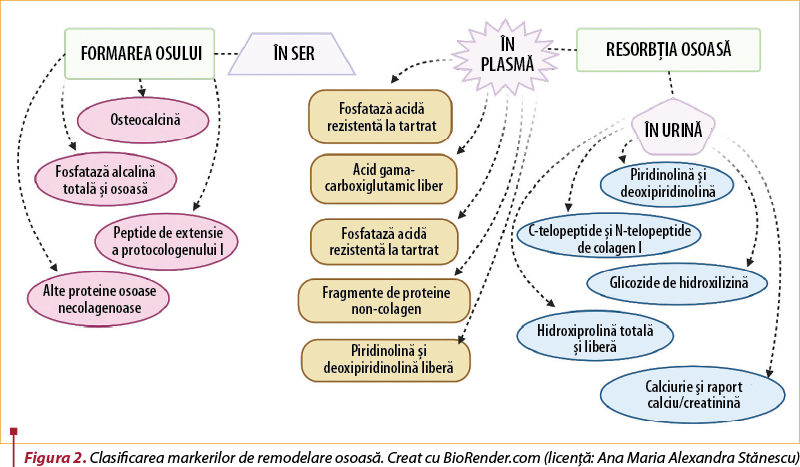
Deşi markerii biochimici ai resorbţiei osoase au un rol limitat în identificarea pacienţilor cu osteoporoză, aceştia au un potenţial real în evaluarea pacienţilor cu risc crescut de pierdere osoasă accelerată („fast bone losers”)(38).
Viteza formării sau resorbţiei osoase poate fi evaluată prin măsurarea activităţii enzimatice legate de celulele responsabile de formarea osului (osteoblaste), resorbţia osoasă (osteoclaste)(39) sau prin măsurarea unui constituent al matricei osoase extracelulare care este eliberat în circulaţie în timpul formării şi resorbţiei osoase. Aceşti markeri diferă prin sensibilitate şi specificitate(40) şi sunt esenţiali în supravegherea terapeutică a osteoporozei: markerii resorbţiei osoase scad după 4-6 săptămâni de tratament, iar cei de formare după 2-3 luni, în timp ce modificările DMO (DXA) apar după un an de tratament(41,42).
Concluzii
Există mai multe etiologii ale osteoporozei. Practicienii trebuie să fie familiarizaţi cu diferitele etiologii ale acesteia, deoarece osteoporoza creşte riscul de fractură osoasă.
Conflict of interests: The authors declare no conflict of interests.
Bibliografie
- Granacher U, Gollhofer A, Hortobágyi T, Kressig RW, Muehlbauer T. The importance of trunk muscle strength for balance, functional performance, and fall prevention in seniors: a systematic review. Sports Med. 2013 Jul;43(7):627-641.
- Liu J, Curtis EM, Cooper C, Harvey NC. State of the art in osteoporosis risk assessment and treatment. J Endocrinol Invest. 2019 Oct;42(10):1149-1164. doi: 10.1007/s40618-019-01041-6.
- Heijink A, Vanhees M, van den Ende K, van den Bekerom MP, van Riet RP, Van Dijk CN, Eygendaal D. Biomechanical considerations in the pathogenesis of osteoarthritis of the elbow. Knee Surg Sports Traumatol Arthrosc. 2016 Jul;24(7):2313-8. doi: 10.1007/s00167-015-3518-7.
- Raehtz S, Bierhalter H, Schoenherr D, Parameswaran N, McCabe LR. Estrogen Deficiency Exacerbates Type 1 Diabetes-Induced Bone TNF-α Expression and Osteoporosis in Female Mice. Endocrinology. 2017 Jul 1;158(7):2086-2101. doi: 10.1210/en.2016-1821.
- Bijelic R, Milicevic S, Balaban J. Risk Factors for Osteoporosis in Postmenopausal Women. Med Arch. 2017 Feb;71(1):25-28. doi: 10.5455/medarh.2017.71.25-28.
- Ensrud KE, Crandall CJ. Osteoporosis. Ann Intern Med. 2017 Aug 1;167(3):ITC17-ITC32. doi: 10.7326/AITC201708010. Erratum in: Ann Intern Med. 2017 Oct 3;167(7):528.
- Musumeci G, Castrogiovanni P, Trovato FM, Weinberg AM, Al-Wasiyah MK, Alqahtani MH, Mobasheri A. Biomarkers of Chondrocyte Apoptosis and Autophagy in Osteoarthritis. International Journal of Molecular Sciences. 2015; 16(9):20560-20575. https://doi.org/10.3390/ijms160920560G.
- Geenen R, Overman CL, Christensen R, Åsenlöf P, Capela S, Huisinga KL, Husebø MEP, Köke AJA, Paskins Z, Pitsillidou IA, Savel C, Austin J, Hassett AL, Severijns G, Stoffer-Marx M, Vlaeyen JWS, Fernández-de-Las-Peñas C, Ryan SJ, Bergman S. EULAR recommendations for the health professional’s approach to pain management in inflammatory arthritis and osteoarthritis. Ann Rheum Dis. 2018 Jun;77(6):797-807. doi: 10.1136/annrheumdis-2017-212662.
- Wimalawansa SJ, Razzaque MS, Al-Daghri NM. Calcium and vitamin D in human health: Hype or real? J Steroid Biochem Mol Biol. 2018 Jun;180:4-14. doi: 10.1016/j.jsbmb.2017.12.009.
- Chen YW, Ramsook AH, Coxson HO, Bon J, Reid WD. Prevalence and Risk Factors for Osteoporosis in Individuals With COPD: A Systematic Review and Meta-analysis. Chest. 2019 Dec;156(6):1092-1110. doi: 10.1016/j.chest.2019.06.036.
- Armas LA, Recker RR. Pathophysiology of osteoporosis: new mechanistic insights. Endocrinol Metab Clin North Am. 2012 Sep;41(3):475-86. doi: 10.1016/j.ecl.2012.04.006.
- Bowden Davies KA, Pickles S, Sprung VS, Kemp GJ, Alam U, Moore DR, Tahrani AA, Cuthbertson DJ. Reduced physical activity in young and older adults: metabolic and musculoskeletal implications. Ther Adv Endocrinol Metab. 2019 Nov 19;10:2042018819888824. doi: 10.1177/2042018819888824.
- Evenepoel P, Cunningham J, Ferrari S, Haarhaus M, Javaid MK, Lafage-Proust MH, Prieto-Alhambra D, Torres PU, Cannata-Andia J; European Renal Osteodystrophy (EUROD) workgroup, an initiative of the CKD-MBD working group of the ERA-EDTA, and the committee of Scientific Advisors and National Societies of the IOF. European Consensus Statement on the diagnosis and management of osteoporosis in chronic kidney disease stages G4-G5D. Nephrol Dial Transplant. 2021 Jan 1;36(1):42-59. doi: 10.1093/ndt/gfaa192.
- Dardonville Q, Salguiero E, Rousseau V, Chebane L, Faillie JL, Gautier S, Montastruc JL, Carvajal A, Bagheri H. Drug-induced osteoporosis/osteomalacia: analysis in the French and Spanish pharmacovigilance databases. Eur J Clin Pharmacol. 2019 Dec;75(12):1705-1711. doi: 10.1007/s00228-019-02743-9.
- Nguyen KD, Bagheri B, Bagheri H. Drug-induced bone loss: a major safety concern in Europe. Expert Opin Drug Saf. 2018 Oct;17(10):1005-1014. doi: 10.1080/14740338.2018.1524868.
- Palomo T, Vilaça T, Lazaretti-Castro M. Osteogenesis imperfecta: diagnosis and treatment. Curr Opin Endocrinol Diabetes Obes. 2017 Dec;24(6):381-388. doi: 10.1097/MED.0000000000000367.
- Rossi V, Lee B, Marom R. Osteogenesis imperfecta: advancements in genetics and treatment. Curr Opin Pediatr. 2019 Dec;31(6):708-715. doi: 10.1097/MOP.0000000000000813.
- Kanis JA, Cooper C, Rizzoli R, Reginster JY; Scientific Advisory Board of the European Society for Clinical and Economic Aspects of Osteoporosis (ESCEO) and the Committees of Scientific Advisors and National Societies of the International Osteoporosis Foundation (IOF). Correction to: European guidance for the diagnosis and management of osteoporosis in postmenopausal women. Osteoporos Int. 2020 Jan;31(1):209. doi: 10.1007/s00198-019-05184-3. Erratum for: Osteoporos Int. 2019 Jan;30(1):3-44.
- Conley RB, Adib G, Adler RA, Åkesson KE, Alexander IM, Amenta KC, et al. Secondary Fracture Prevention: Consensus Clinical Recommendations from a Multistakeholder Coalition. J Bone Miner Res. 2020 Jan;35(1):36-52. doi: 10.1002/jbmr.3877.
- Lara BMC, Pádua CM, Mendicino CCP, Rocha GM. Osteopenia and osteoporosis among treatment-experienced people living with HIV. Braz J Infect Dis. 2020 Jul-Aug;24(4):288-295. doi: 10.1016/j.bjid.2020.05.008.
- Starup-Linde J, Rosendahl SB, Storgaard M, Langdahl B. Management of Osteoporosis in Patients Living With HIV – A Systematic Review and Meta-analysis. J Acquir Immune Defic Syndr. 2020 Jan 1;83(1):1-8. doi: 10.1097/QAI.0000000000002207.
- Weitzmann MN. Bone and the Immune System. Toxicol Pathol. 2017 Oct;45(7):911-924. doi: 10.1177/0192623317735316.
- Mirza FS, Luthra P, Chirch L. Endocrinological aspects of HIV infection. J Endocrinol Invest. 2018 Aug;41(8):881-899. doi: 10.1007/s40618-017-0812-x.
- Studer RK, Negrete H, Craven PA, DeRubertis FR. Protein kinase C signals thromboxane induced increases in fibronectin synthesis and TGF-beta bioactivity in mesangial cells. Kidney Int. 1995 Aug;48(2):422-30. doi: 10.1038/ki.1995.310.
- Premaor MO, Compston JE. People living with HIV and fracture risk. Osteoporos Int. 2020 Sep;31(9):1633-1644. doi: 10.1007/s00198-020-05350-y.
- Compston J. HIV infection and bone disease. J Intern Med. 2016 Oct;280(4):350-8. doi: 10.1111/joim.12520.
- Delpino MV, Quarleri J. Influence of HIV Infection and Antiretroviral Therapy on Bone Homeostasis. Front Endocrinol (Lausanne). 2020 Sep 2;11:502. doi: 10.3389/fendo.2020.00502.
- Engel T, Raffenberg M, Marzolini C, Cavassini M, Kovari H, Hasse B, Tarr PE. HIV and Aging – Perhaps Not as Dramatic as We Feared? Gerontology. 2018;64(5):446-456. doi: 10.1159/000489172.
- Adami G, Fassio A, Rossini M, Caimmi C, Giollo A, Orsolini G, Viapiana O, Gatti D. Osteoporosis in Rheumatic Diseases. Int J Mol Sci. 2019 Nov 22;20(23):5867. doi: 10.3390/ijms20235867.
- Bruyère O, Honvo G, Veronese N, Arden NK , Branco J, et al. An updated algorithm recommendation for the management of knee osteoarthritis from the European Society for Clinical and Economic Aspects of Osteoporosis, Osteoarthritis and Musculoskeletal Diseases (ESCEO). Seminars in Arthritis and Rheumatism. 2019;49(3):337-350. doi: 10.1016/j.semarthrit.2019.04.008.
- Matsumoto H, Tanimura C, Kushida D, Osaka H, Kawabata Y, Hagino H. FRAX score and recent fall history predict the incidence for sarcopenia in community-dwelling older adults: a prospective cohort study. Osteoporos Int. 2020 Oct;31(10):1985-1994. doi: 10.1007/s00198-020-05447-4.
- Link TM, Kazakia G. Update on Imaging-Based Measurement of Bone Mineral Density and Quality. Curr Rheumatol Rep. 2020 Apr 9;22(5):13. doi: 10.1007/s11926-020-00892-w.
- Kendler DL, Compston J, Carey JJ, Wu CH, Ibrahim A, Lewiecki EM. Repeating Measurement of Bone Mineral Density when Monitoring with Dual-energy X-ray Absorptiometry: 2019 ISCD Official Position. J Clin Densitom. 2019 Oct-Dec;22(4):489-500. doi: 10.1016/j.jocd.2019.07.010.
- Camacho PM, Petak SM, Binkley N, Diab DL, Eldeiry LS, Farooki A, et al. American Association of Clinical Endocrinologists/American College of Endocrinology Clinical practice guidelines for the diagnosis and treatment of postmenopausal osteoporosis – 2020 update executive summary. Endocr Pract. 2020 May;26(5):564-570. doi: 10.4158/GL-2020-0524.
- Watts NB. Postmenopausal Osteoporosis: A Clinical Review. J Womens Health (Larchmt). 2018 Sep;27(9):1093-1096. doi: 10.1089/jwh.2017.6706.
- Martineau P, Leslie WD. The utility and limitations of using trabecular bone score with FRAX. Curr Opin Rheumatol. 2018 Jul;30(4):412-419. doi: 10.1097/BOR.0000000000000504.
- Ibáñez L, Rouleau M, Wakkach A, Blin-Wakkach C. Gut microbiome and bone. Joint Bone Spine. 2019 Jan;86(1):43-47. doi: 10.1016/j.jbspin.2018.02.008.
- Greenblatt MB, Tsai JN, Wein MN. Bone Turnover Markers in the Diagnosis and Monitoring of Metabolic Bone Disease. Clin Chem. 2017 Feb;63(2):464-474. doi: 10.1373/clinchem.2016.259085.
- Uda Y, Azab E, Sun N, Shi C, Pajevic PD. Osteocyte Mechanobiology. Curr Osteoporos Rep. 2017 Aug;15(4):318-325. doi: 10.1007/s11914-017-0373-0.
- Mintzer S, Constantino T, Gidal B, Bhargava P, Grinnell T, Blum D. Markers of bone and lipid metabolism with eslicarbazepine acetate monotherapy. Epilepsy Res. 2019 Dec;158:106216. doi: 10.1016/j.eplepsyres.2019.106216.
- Palareti G, Legnani C, Cosmi B, Antonucci E, Erba N, Poli D, Testa S, Tosetto A; DULCIS (D-dimer-ULtrasonography in Combination Italian Study) Investigators (See Appendix); DULCIS (D-dimer-ULtrasonography in Combination Italian Study) Investigators. Comparison between different D-Dimer cutoff values to assess the individual risk of recurrent venous thromboembolism: analysis of results obtained in the DULCIS study. Int J Lab Hematol. 2016 Feb;38(1):42-9. doi: 10.1111/ijlh.12426.
- Laroche M, Baradat C, Ruyssen-Witrand A, Degboe Y. Variability of Denosumab densitometric response in postmenopausal osteoporosis. Rheumatol Int. 2018 Mar;38(3):461-466. doi: 10.1007/s00296-018-3929-0.
Articole din ediţiile anterioare
Aspecte ale infecţiei cu noul coronavirus la femeile gravide
Sarcina şi naşterea nu cresc, în general, riscul de infectare cu SARS-CoV-2, dar se pare că favorizează evoluţia către formele severe. Medicul de f...
Efectele suplimentării cu micronutrienţi în perioada de sarcină
Comportamentul alimentar inadecvat antrenează un aport de micronutrienţi mai mic decât valorile recomandate, în rândul femeilor de vârstă reproduct...
Corelaţii ale metabolismului lipidic cu remodelarea osoasă
Introducere. Osteoporoza şi dislipidemia reprezintă o patologie medicală cronică, iar relaţia dintre acestea se bazează pe factori de risc şi me...
Hipertensiunea arterială iatrogenă
Numeroşi agenţi terapeutici sau substanţe chimice pot determina o creştere tranzitorie sau persistentă a tensiunii arteriale (TA) sau pot in...