Ever since his birth, the newborn is subjected to painful procedures, starting with administrating vitamin K and normal vaccines and ending with different screening tests performed prior to discharge. In addition, infants hospitalized in neonatal intensive care units may be exposed to painful procedures (arterial, vein or lumbar puncture, intramuscular injections, peripheral or central venous catheterization, endotracheal intubation etc.), many of them being carried out in emergency. In the case of a small preterm, 27 gestation weeks or smaller, even a simple diaper change or a usual clinical examination can trigger pain sensation.
Managementul durerii la nou-născut
Pain management in newborns
First published: 15 martie 2017
Editorial Group: MEDICHUB MEDIA
DOI: 10.26416/Peri.1.1.2017.476
Abstract
Rezumat
Încă de la naştere, nou-născutul este supus unor proceduri dureroase, începând cu administrarea vitaminei K şi a vaccinurilor uzuale şi terminând cu diferite teste de screening efectuate anterior externării. În plus, nou-născuţii internaţi în secţiile de terapie intensivă neonatală pot fi expuşi unor proceduri dureroase suplimentare (puncţie arterială, venoasă sau lombară, injecţii intramusculare, cateterizare venoasă periferică sau centrală, intubaţie endotraheală etc.), multe din acestea fiind efectuate în urgenţă. În cazul prematurilor cu vârstă de gestaţie mică, de 27 de săptămâni sau mai mici, chiar schimbarea scutecului sau un simplu examen clinic obişnuit poate declanşa senzaţia de durere.
Introducere
Progresele efectuate în ultimii ani au stabilit că nou-născutul poate experimenta durere acută sau cronică, iar managementul corect are beneficii atât pe termen scurt, cât şi pe termen lung(1).
Atât nou-născutul la termen, cât şi prematurul pot experimenta durere şi au dreptul la terapie analgezică eficientă, în condiţii de siguranţă(2). Din acest motiv, prevenirea durerii la nou-născut este un deziderat nu numai al celor care îngrijesc nou-născuţii, dar şi al părinţilor(3).
Nou-născutul nu poate verbaliza durerea şi, ca urmare, depinde de alţii să recunoască, să evalueze şi să gestioneze durerea, cu atât mai mult cu cât, faţă de adult, afişează o hipersensibilitate la stimuli senzoriali şi este mai predispus la durere şi la consecinţele sale.
În ultimele decenii, managementul durerii la nou-născut a cunoscut numeroase schimbări, care au debutat cu respingerea considerentelor anterioare, de până în anii ’80(4), care susţineau că nou-născutul nu poate experimenta nocicepţia acută şi cronică la fel ca adultul, datorită imaturităţii sistemului nervos periferic şi central, concepţii clasice care împiedicau luarea unei decizii terapeutice analgezice.
În plus, lipsa studiilor la momentul respectiv în ceea ce priveşte dependenţa şi posibilele efecte adverse ale opioidelor, precum şi lipsa datelor farmacologice şi farmacocinetice au condus la tratamentul insuficient intra- şi perioperator.
Odată cu publicarea studiilor care au arătat că există modificări cuantificabile ale markerilor biochimici şi fiziologici ca urmare a stimulilor dureroşi chiar şi la prematuri, de multe ori mai mari decât la adult(5,6), aceste concepţii greşite au început să fie corectate.
Aproximativ 10-15% din totalul nou-născuţilor maturi şi marea majoritate a prematurilor sunt spitalizaţi în secţiile de terapie intensivă neonatală, reprezentând categoria de nou-născuţi cu cel mai mare risc de a prezenta ulterior anomalii de dezvoltare neurologică(7). Printre consecinţe se numără sensibilitate modificată, cu prelungirea durerii până în perioada adolescenţei, anomalii neuroanatomice permanente şi anomalii comportamentale, emoţionale şi deficit de învăţare(8).
Definiţii utilizate uzual
- Durere: o senzaţie şi experienţă neplăcută, somatică sau viscerală, asociată cu leziuni tisulare reale sau potenţiale. De asemenea, incapacitatea de a comunica verbal sau non-verbal durerea nu neagă existenţa acesteia.
- Stres: o tulburare a echilibrului dinamic între un nou-născut şi mediul său, având ca rezultat un răspuns fiziologic al nou-născutului.
- Stresul sau răspunsul la durere: răspunsul fiziologic al individului la durere sau la stres, caracterizat în principal prin schimbări în patru domenii - endocrino-metabolic, autonom, imunologic şi/sau comportamental.
- Analgezie: absenţa sau reducerea intensităţii durerii, în prezenţa unor stimuli care ar fi în mod normal dureroşi.
- Controlul durerii: reducerea intensităţii şi/sau duratei durerii.
- Anestezie: imobilizarea şi supresia răspunsului autonom la nocicepţie.
- Sedare: status medical controlat, de deprimare a stării de conştienţă, cu sau fără pierderea reflexelor aeriene protective, având ca urmare pierderea abilităţii de a răspunde la stimuli dureroşi(1,9).
Nou-născuţii internaţi în secţiile de terapie intensivă neonatală pot fi expuşi procedurilor dureroase, ce pot ajunge la un număr de 15-20 pe zi, cum ar fi puncţia arterială şi venoasă, puncţia lombară, injecţii intramusculare, cateterizare venoasă periferică sau centrală, intubaţia endotraheală etc., multe din acestea fiind efectuate în urgenţă(10,11) - tabelul 1. Prematurii cu greutate la naştere extrem de mică sau foarte mică sunt manipulaţi de 150 de ori pe zi şi au mai puţin de 10 minute de odihnă neîntreruptă.
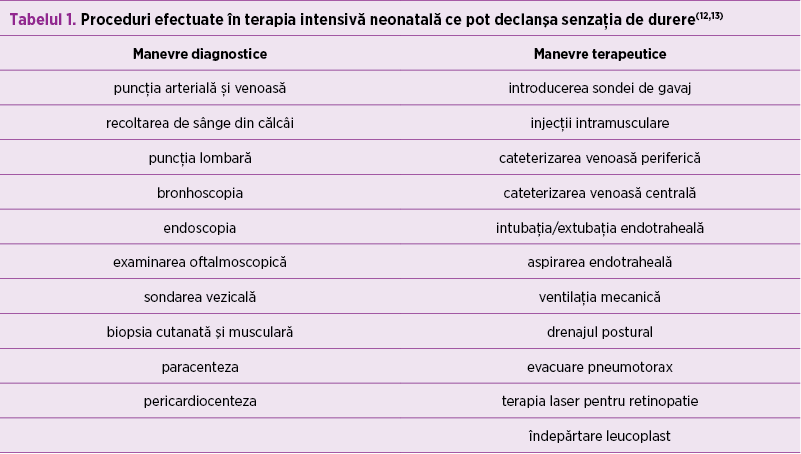
Alte surse de durere la nou-născut sunt reprezentate de zonele de hiperalgezie şi inflamaţie din jurul leziunilor tisulare, de escoriaţiile cauzate de senzorii pentru determinarea transcutanată a saturaţiei în oxigen, de electrozii de monitorizare şi de agenţi dezinfectanţi cu acţiune locală. La prematurii sub 27 de săptămâni, chiar schimbarea scutecului sau o manevră de consultaţie obişnuită poate declanşa senzaţia de durere(14).
Răspunsul la durere
Răspunsul imediat la durere este diferit de la un nou-născut la altul, prematurii fiind mai conştienţi de stimularea dureroasă comparativ cu nou-născutul la termen. Un nou-născut sănătos răspunde energic la o stimulare dureroasă, în timp ce nou-născutul bolnav poate să nu prezinte niciun fel de reacţie. Prematurii răspund la durere printr-o reacţie fiziologică şi comportamentală foarte evidentă şi printr-o cascadă de manifestări hormonale şi metabolice, a cărei repetare ar putea avea efecte destabilizatoare atât pe termen scurt, cât şi lung(15).
Modificările comportamentale la durere includ(16):
- Modificări ale expresiei faciale: grimasă, bătăi ale aripioarelor nazale, tremurături ale bărbiei, adâncirea şanţului nazo-labial, mişcări linguale atipice, încruntare.
- Mişcări ale corpului: arcuirea spatelui, hipotonia cefei, încleştarea degetelor, hipotonie/tremurături la nivelul membrelor, zvârcolire; mişcări active în vederea încercării de a se retrage din faţa stimulului.
Modificări fiziologice la durere
Stimulul dureros activează mecanismele de compensare la nivelul sistemului nervos autonom, care are ca răspuns modificarea frecvenţei cardiace şi a celei respiratorii, a tensiunii arteriale, a saturaţiei în oxigen, accelerarea metabolismului celular cu necesar crescut de oxigen, reducerea volumului tidal, diaforeză şi dilatarea pupilelor(17).
Modificări neuroendocrine la durere(16,18):
- Paloare, eritem tegumentar, midriază, înghiţire repetată.
- Reducerea autoreglării cerebrovasculare, cu creşterea presiunii intracraniene, cu risc de apariţie a hemoragiilor intraventriculare.
- Creşterea eliberării de: cortizol, adrenalină, noradrenalină, glucagon, GH, renină, angiotensină, aldosteron şi ADH.
Evaluarea durerii la nou-născut - al cincilea semn vital
Evaluarea durerii la nou-născut este complicată de incapacitatea acestuia de a verbaliza durerea. Există numeroase scale şi scoruri de evaluare a durerii la nou-născut, bazate pe diferiţi indicatori contextuali (vârsta de gestaţie, statusul somn/veghe), răspunsul comportamental, răspunsul fiziologic sau combinaţii ale saturaţiei în oxigen, TA şi expresia facială.
Din cauza greutăţilor de comunicare ale nou-născutului, este necesară diferenţierea între durere şi agitaţie, pentru că fiecare dintre ele trebuie abordată şi tratată separat.
Expresiile faciale reprezintă indicatorii cei mai specifici şi mai sensibili ai durerii şi sunt incluşi în majoritatea scalelor şi scorurilor de evaluare a durerii neonatale. Următoarele scale şi scoruri au fost supuse evaluării comportamentale şi s-au dovedit a fi măsuri valide, fiabile şi fezabile de evaluare a durerii neonatale (tabelul 2).
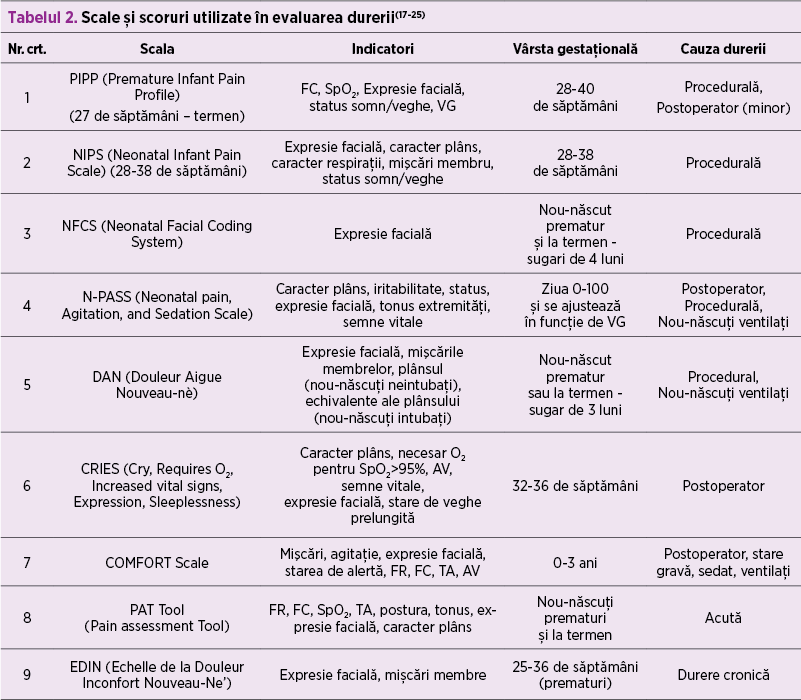
Pentru durerea acută (procedurală, postoperatorie):
- Premature Infant Pain Profile (PIPP)(19)
- Pentru sugari - Neonatale Pain Scale (NIPS)(20)
- Douleur Aigue du Nouveau-Né (DAN)(21)
- Plâns, Necesită oxigen, Semne vitale crescute, Expresie, lipsa Somnului (CRIES)(22)
- Durere neonatală, Agitaţie şi Scor de Sedare (N-pass)(23)
- Instrument de evaluare a durerii (PAT)(24).
Pentru durere cronică:
- Durere neonatală, Agitaţie şi Scor de Sedare (N-pass)(23)
- Echelle douleur Inconfort Nouveau-Né (EDIN)(25).
Furnizorii de servicii de sănătate ar trebui să se orienteze după ghidurile instituţiei. Fiecare instituţie ar trebui să selecteze un instrument, să educe personalul pentru a asigura măsurarea constantă şi gestionarea optimă şi documentată a durerii.
Managementul durerii
Obiective:
- Minimizarea stresului.
- Reducerea numărului de proceduri dureroase şi stimuli care nu sunt necesare.
- Prevenirea injuriei SNC.
- Minimizarea eliberării mediatorilor durerii la nivel tisular.
- Refacerea răspunsului la stres.
- Prevenirea/reducerea durerii acute prin furnizarea de analgezice ca prevenţie pentru orice procedură dureroasă anticipată, ce include o combinaţie de metode non-farmacologice şi farmacologice.
- Monitorizarea răspunsurilor pacientului la analgezice utilizând scale şi scoruri de evaluare validate şi furnizarea analgeziei suplimentare în caz de necesitate.
Măsuri non-farmacologice
Următoarele abordări nefarmacologice pot reduce în mod eficient durerea şi disconfortul din măsurile de îngrijire de rutină şi proceduri minore (de exemplu, toc bastonul) atât la prematuri, cât şi la nou-născuţi la termen(26).
În anumite situaţii, aceste combinaţii pot elimina utilizarea farmacologică sau pot ajuta la reducerea dozei sau a frecvenţei dozelor necesare şi, în consecinţă, pot diminua efectele secundare(27,28).
a. Alăptare/administrarea laptelui de mamă/supt non-nutritiv.
b. Terapie prin muzică.
c. Înfăşarea, menţinerea situaţiei satisfăcătoare a corpului cu ajutorul pernuţelor, al Kangaroo-care.
d. Procedurile invazive se efectuează doar cu personal pregătit.
e. Mărirea perioadelor de pauză între procedurile dureroase.
În fiecare secţie de neonatologie ar trebui respectat un protocol de stimulare minimă care să ţină cont de următoarele elemente(37):
- Scăderea numărului de stimuli luminoşi şi auditivi.
- Utilizarea monitorizării permanente cu ajutorul aparaturii, în loc de auscultarea cordului.
- Trebuie menţinută o poziţionare corectă a nou-născutului, care să îi permită să respire bine; trebuie mutat doar dacă desaturează.
- Numărul de manevre invazive trebuie redus la minimum, fiind necesară gruparea recoltărilor de sânge pentru investigaţii.
- Se preferă montarea unui cateter arterial ombilical la nou-născuţii care vor necesita evaluări dese ale gazelor sanguine.
Măsuri farmacologice
Farmacocinetica şi farmacodinamica sunt diferite la nou-născut, mai ales la prematuri, comparativ cu celelalte grupe de vârstă. Trebuie avut în vedere că - la fel ca în cazul miorelaxantelor - medicaţia sedativ-hipnotică nu este şi analgezică.
Măsurile farmacologice variază în funcţie de severitatea durerii, de la analgezie locală la analgezie sistemică.
1. Administrarea orală de sucroză 24% sau glucoză 33%(35). Efectele calmante ale sucrozei s-au dovedit a fi datorate gustului dulce şi nu depind de volum, având în vedere că volume mici de 0,2 ml de sucroză au fost la fel de eficiente ca un volum mai mare de până la 1 ml. Instalarea efectului apare la două minute după administrare şi persistă pentru aproximativ cinci până la opt minute(29), fiind dependent de contactul cu limba, şi nu de ingestia prin tubul nazogastric(12). Nu a fost stabilită o doză optimă pentru administrare, motiv pentru care informaţiile din studii variază de la 0,05-0,5 ml/doză de soluţie de sucroză 24%(30).
2. Analgezie locală - cremă EMLA 5% (liodcaină 2,5%, pilocarpină 2,5%).
Este utilizată în abordurile vasculare sau în cazul puncţiei lombare şi se aplică cu 20-30 de minute anterior procedurii. Are însă ca efect secundar apariţia leziunilor ca urmare a aplicării frecvente, precum şi un risc de methemoglobinemie, din cauza faptului că prin metabolizarea pilocarpinei se produc substanţe oxidante, nou-născuţii fiind expuşi riscului de methemoglobinemie deoarece au niveluri scăzute de methemoglobin-reductază şi hemoglobina fetală este mai uşor oxidată la methemoglobină(31).
3. Analgezie regională
Analgezia regională: spinală, epidurală, bloc nervos specific (lidocaină, bupivacaine, ropivacaină). Reduce necesarul de analgezice sistemice. Postoperator: gastroschizis, omfalocel, hernie diafragmatică etc. Acest tip de intervenţie include analgezia spinală şi epidurală, iar substanţele administrate sunt anestezice locale. Au ca avantaj major reducerea necesarului de analgezice sistemice(32).
4. Analgezie sistemică
a. Non-opioide
Acetaminofenul (paracetamolul) poate fi utilizat pentru gestionarea durerii procedurale sau postoperatorii uşoare până la moderate, dar este ineficient în cazul recoltării sângelui capilar (călcâi). Dozele recomandate sunt de 10-15 mg/kg pe cale orală sau 20-25 mg/kg intrarectal, administrate la fiecare 6-8 ore, iar pentru utilizarea intravenosă, o doză de încărcare de 20 mg/kg, urmată de 10 mg/kg la fiecare 6-8 ore(33,34).
b. AINS
Sunt utilizate mai rar în cazul nou-născuţilor, din cauza efectelor adverse bine cunoscute (toxicitate renală, hemoragie digestivă), fiind rezervate închiderii canalului arterial persistent(36).
c. Opiode: morfina, fentanyl, sufentanil
Opiozii sunt indicaţi în cazul nou-născuţilor, însă necesită monitorizarea efectelor adverse, respectiv creşterea frecvenţei cardiace, barieră hematoencefalică imatură, timp de înjumătăţire mare.
Efectele adverse ale analgezicelor de tip narcotic, demne de luat în considerare, sunt: depresia respiratorie, hipotensiune arterială, complianţă scăzută a cutiei toracice, scăderea volumului tidal, retenţie urinară, convulsii, bradicardie, constipaţie. Ca urmare, utilizarea de rutină a morfinei la nou-născuţii prematuri nu este indicată, fiind însă recomandată postoperator sau în timpul manevrelor invazive(38).
Dintre sedativele non-barbiturice este preferat midazolamul, derivat sintetic de benzodiazepine, cu acţiune rapidă şi durată scurtă de acţiune. Diazepamul nu este recomandat ca sedativ la nou-născut, din cauza timpului de înjumătăţire crescut şi a benzil-alcoolului aflat în componenta sa. Poate induce icter, depresie respiratorie, hipotensiune sau agitaţie(37).
Concluzii
Durerea poate fi evaluată din primele faze ale vieţii şi, în ciuda numeroaselor studii publicate privind modificările complexe comportamentale, fiziologice şi biochimice ale nou-născuţilor şi a rezultatelor clinice negative pe termen scurt şi lung ale expunerii repetitive la durere, utilizarea clinică a măsurilor de evaluare şi de control al durerii la nou-născuţi rămân sporadice şi suboptime.
În momentul de faţă, în neonatologie, alegerea medicaţiei pentru minimizarea durerii (intensitate, durată), precum şi asistarea nou-născutului în încercarea sa de a face faţă durerii se fac utilizând scale şi scoruri validate, ţinând cont şi de protocolul pe care fiecare secţie îl are.
În cele din urmă, indiferent de vârstă, pacientul are dreptul la analgezie, şi acest drept ar trebui să fie recunoscut şi garantat chiar şi atunci când nevoia de analgezie nu poate fi exprimată verbal de către pacient, iar cei implicaţi în îngrijirea nou-născuţilor (personal medical, părinţi) trebuie să ţină cont de faptul că pacientul pediatric experimentează durerea la fel ca adultul.
Bibliografie
2. Finnström O, Schollin J. Lakartidningen. Newborn infants do feel pain! Technique and environment in connection with specimen collection can be improved. 1998 Dec 9; 95(50):5718-20.
3. Franck LS, Cox S, Allen A, Winter I. Parental concern and distress about infant pain. Arch Dis Child Fetal Neonatal Ed. 2004; 89:F71–F75.
4. Anand KJ, Hickey PR. Pain and its effects in the human neonate and fetus. N Engl J Med 1987 Nov 19; 317(21):1321-9.
5. Mancuso T, Burns J. Ethical concerns in the management of pain in the neonate. Paediatr Anaesth.2009; 19:953–7. [PubMed]
6. Peters JW, Schouw R, Anand KJ, van Dijk M, Duivenvoorden HJ, Tibboel D. Does neonatal surgery lead to increased pain sensitivity in later childhood? Pain. 2005; 114:444–54. [PubMed]
7. Anand KJ, Scalzo FM. Can adverse neonatal experiences alter brain development and subsequent behavior? Biol Neonate. 2000; 77:69–82.
8. Grunau, RE (2013) Neonatal Pain in Very Preterm Infants: Long-Term Effects on Brain, Neurodevelopment and Pain Reactivity. Rambam Maimonides Medical Journal, 4(4), e0025.
9. Caraceni A, Cherny N, Fainsinger R et al. The Steering Committee of the EAPC Research Network. Pain measurement tools and methods in clinical research in palliative care: recommendations of an expert working group of the European Association of Palliative Care. J Pain Symptom Manage 2002; 23: 239–255.
10. Carbajal R, Rousset A, Danan C, et al. Epidemiology and treatment of painful procedures in neonates in intensive care units. JAMA 2008; 300:60.
11. Simons SH, van Dijk M, Anand KS, et al. Do we still hurt newborn babies? A prospective study of procedural pain and analgesia in neonates. Arch Pediatr Adolesc Med 2003; 157:1058.
12. Krishnan, L. (2013). Pain Relief in Neonates. Journal of Neonatal Surgery, 2(2), 19.
13. Witt, N., Coynor, S., Edwards, C., & Bradshaw, H. (2016). A Guide to Pain Assessment and Management in the Neonate. Current Emergency and Hospital Medicine Reports, 4, 1–10.
14. Johnston C, Barrington KJ, Taddio A, Carbajal R, Filion F. Pain in Canadian NICUs: have we improved over the past 12 years? Clin J Pain 2011 Mar; 27(3):225-32.
15. Bartocci M, Bergqvist LL, Lagercrantz H, Anand KJ. Pain activates cortical areas in the preterm newborn brain. Pain. 2006; 122:109–17.
16. Bellieni, C.V. Pain Assessment in Human Fetus and Infants, AAPS J (2012) 14: 456.
17. Lawrence J, Alcock D, McGrath P et al. The development of a tool to assess neonatal pain. Neonatal Netw, 1993; 12:59-66.
18. Sweet S, McGrath PJ. Physiological measures of pain. Prog Pain Res Meas, 1998; 10:59-81.
19. Stevens B, Johnston C, Petryshen P, Taddio A. Premature Infant Pain Profile: development and initial validation. Clin J Pain 1996 Mar; 12(1):13-22.
20. Lawrence J, Alcock D, McGrath P, Kay J, Mac Murray SB, Dulberg C. The development of a tool to assess neonatal pain. Neonatal Netw 1993 Sep; 12(6):59-66.
21. Carbajal R, Paupe A, Hoenn E, Lenclen R, Olivier-Martin M. [APN: evaluation behavioral scale of acute pain in newborn infants]. Arch Pediatr 1997 Jul; 4(7):623-8.
22. Krechel SW, Bildner J. CRIES: a new neonatal postoperative pain measurement score. Initial testing of validity and reliability. Paediatr Anaesth 1995; 5(1):53-61.
23. Hummel P, Puchalski M, Creech SD, Weiss MG. Clinical reliability and validity of the N-PASS: neonatal pain, agitation and sedation scale with prolonged pain. J Perinatol 2008 Jan; 28(1):55-60.
24. Spence K, Gillies D, Harrison D, Johnston L, Nagy S. A reliable pain assessment tool for clinical assessment in the neonatal intensive care unit. J Obstet Gynecol Neonatal Nurs 2005 Jan; 34(1):80-6.
25. Debillon T, Zupan V, Ravault N, Magny JF, Dehan M. Development and initial validation of the EDIN scale, a new tool for assessing prolonged pain in preterm infants. Arch Dis Child Fetal Neonatal Ed 2001 Jul; 85(1):F36-F41.
26. Sharek PJ, Powers R, Koehn A, Anand KJ. Evaluation and development of potentially better practices to improve pain management of neonates. Pediatrics 2006; 118 Suppl 2:S78.
27. Bellieni CV, Cordelli DM, Marchi S, et al. Sensorial saturation for neonatal analgesia. Clin J Pain 2007; 23:219.
28. Golianu B, Krane E, Seybold J, et al. Non-pharmacological techniques for pain management in neonates. Semin Perinatol 2007; 31:318.
29. Blass E M, Shah A. Pain-reducing properties of sucrose in human newborns. Chem Senses.1995; 20:29–35.
30. Heaton PA, Fernando AM, Herd D. Oral sucrose for procedural pain in infants. Lancet 2011; 377:25; author reply 27.
31. S. Lillieborg, I. Otterbom, K. Ahlen, and C. Long. Topical anaesthesia in neonates, infants and children. Br. J. Anaesth. (2004) 92 (3): 450-451.
32. Lönnqvist PA. Regional anaesthesia and analgesia in the neonate. Best Pract Res Clin Anaesthesiol. 2010; 24:309–21.
33. Allegaert K, Palmer GM, Anderson BJ. The pharmacokinetics of intravenous paracetamol in neonates: size matters most. Arch Dis Child 2011; 96:575–80.
34. Pacifici, G. M., & Allegaert, K. (2015). Clinical Pharmacology of Paracetamol in Neonates: A Review. Current Therapeutic Research, Clinical and Experimental, 77, 24–30.
35. Harrison D, Stevens B, Bueno M, Yamada J, Adams-Webber T, Beyene J, Ohlsson A. Efficacy of sweet solutions for analgesia in infants between 1 and 12 months of age: a systematic review. Arch Dis Child 2010; 95:406–13.
36. Aranda JV(1), Beharry KD, Valencia GB. Nonsteroidal anti-inflammatory drugs (NSAIDs) in the newborn - which ones? J Matern Fetal Neonatal Med. 2009; 22 Suppl 3:21-2.
37. American Academy of Pediatrics Committee on Fetus and Newborn; American Academy of Pediatrics Section on Surgery; Canadian Paeditric Society Fetus and Newborn Committee, Batton DG, Barrington KJ, Wallman C. Prevention and management of pain in the neonate: an update. Pediatrics. 2006 Nov; 118(5):2231-41.
38. Bellu R, de Waal K, Zanini R. Opioids for neonates receiving mechanical ventilation: a systematic review and meta-analysis. Arch Dis Child Fetal Neonatal Ed 2010; 95:F241–51.
Articole din ediţiile anterioare
Care este comportamentul româncelor privind fumatul şi consumul de alcool în timpul sarcinii?
Deşi este arhicunoscut faptul că fumatul şi alcoolul au doar efecte nocive asupra sănătăţii, aceste obiceiuri afectează un procent important al pop...
Hernie congenitală diafragmatică pe partea dreaptă - prezentare de caz
Hernia diafragmatică congenitală este o patologie ce constă în existenţa unui defect la nivelul diafragmului abdominal, din pricina căruia are loc ...
Sindrom de colestază neonatală la un prematur cu greutate foarte mică la naştere (VLBW) – prezentare de caz
Sindromul de colestază neonatală reprezintă o patologie importantă (cu o incidenţă de 1/2500 de nou-născuţi vii), care ridică multe probleme de dia...
Corioamniotita – naşterea prematură şi dezvoltarea nou-născutului
Corioamniotita este o complicaţie importantă a sarcinii, fiind asociată cu consecinţe materne, perinatale, dar şi pe termen lung. Efectele asupra m...