Anemia, as a multifactorial syndrome, is often registered in farm animals' pathology, especially with nutritional origin and less often with different other causes (systemic or organ diseases). It is defined as a decreasing in the number of red blood cells (erythrocytes), the hematocrit and the hemoglobin concentration, respectively. The physiopathological and, respectively, the clinical consequences are directly corelated with the severity of the anemia and the responsible mechanism, expressed by pallor of the mucous membranes, weakness, tachycardia and/or tachypnea and, indirectly, by the reduction of productive and reproductive indices. Nutritional/deficiency anemias are widespread in intensive breeding, with economic repercussions not to be neglected, and the knowledge and application of curative-prophylactic principles at the ages of maximum vulnerability considerably reduce the incidence and the unfavorable economic impact.
Anemiile la suine
Anemia in pigs
First published: 30 septembrie 2023
Editorial Group: MEDICHUB MEDIA
DOI: 10.26416/PV.41.3.2023.8680
Abstract
Rezumat
Anemia, ca sindrom plurifactorial, este frecvent întâlnită în patologia animalelor de rentă, în special cu origine nutriţională şi mai rar cu diverse alte cauze (afecţiuni sistemice sau de organ). Este definită ca o scădere a numărului de globule roşii (hematii), a hematocritului şi, respectiv, a concentraţiei hemoglobinei. Consecinţele fiziopatologice şi clinice sunt în strânsă concordanţă cu severitatea anemiei şi mecanismul inductor, traduse prin paloarea mucoaselor, slăbiciune, tahicardie şi/sau tahipnee şi, indirect, prin reducerea indicilor productivi şi reproductivi. Anemiile nutriţionale/carenţiale sunt frecvent întâlnite în creşterea intensivă, având repercusiuni economice deloc de neglijat, iar cunoaşterea şi aplicarea principiilor curativo-profilactice la vârstele de maximă vulnerabilitate reduc considerabil incidenţa şi impactul economic defavorabil.
În patologia veterinară, sunt unanim acceptate şi recunoscute sistemele de clasificare a anemiei pe baza: proprietăţilor fizice (dimensiunea eritrocitelor şi concentraţia hemoglobinei), a răspunsului măduvei osoase (regenerativ/neregenerativ) sau pe baza proceselor patologice (eritropoieză defectuoasă, hemoragie şi hemoliză).
În patologia suinelor, anemia poate recunoaşte o multitudine de cauze, clasificarea fiind recomandată a fi sistematizată după mecanismul inductor: eritropoieză defectuoasă, hemoliză, posthemoragică, carenţială, bacteriană, toxică etc.
Anemiile prin eritropoieză defectuoasă sunt întâlnite în boli cronice (debilitante), deficienţe nutriţionale/carenţiale (fier, cupru, vitamina B12), infecţii virale specifice (PRRSV, circovirus porcin 2). Cele hemolitice pot fi de tip autoimun (izoeritroliză neonatală), vasculite, sindromul de coagulare vasculară diseminată sau parazitoze endoglobulare (Mycoplasma suis, Eperythrozoon suis).
Anemiile posthemoragice sunt frecvente în cazul enteropatiilor hemoragice (gastroenterita transmisibilă, dizenterie), al ulcerelor gastrice, sindroamelor hemoragice intestinale (volvulus), parazitismului extern: infestaţii cu păduchi (Haematopinus suis), intern: viermi (Trichuris suis, Strongyloides ransomi, Fasciola hepatica, Macracanthorhynchus hirudinaceus), în tulburări de coagulabilitate etc.
În categoria anemiilor carenţiale sau toxice, cele mai frecvente cauze sunt reprezentate de deficitul de fier (anemia feriprivă), cupru (anemia cupriprivă), vitamina B12 (cobaltoprivă), acid folic, vitamina B6, vitamina E, vitamina K sau intervenţia nocivă a aflatoxinelor, tricotecenilor (stachybotriotoxine), zearalenonei sau anticoagulantelor (warfarină, bromadiolon etc.).
Cele bacteriene sunt determinate mai frecvent de acţiunea micoplasmelor (Mycoplasma suis), salmonelelor (Salmonella spp.), Lawsonia intracellularis etc.
La adulţi, anemiile hemolitice toxice-nutriţionale recunosc o incidenţă apreciabilă, mai ales în sistemul gospodăresc de creştere. Anemia din intoxicaţia cu varză şi cu ceapă este cea mai frecventă cauză a anemiei hemolitice la suine.
În cazul intoxicaţiei cu varză, aceasta apare după consumul îndelungat (2-4 săptămâni) al unor cantităţi mari de frunze şi colete de varză. Coordonatele patogenetice sunt în strânsă corelaţie cu faptul că varza (Brassica oleracea) conţine, pe lângă mari cantităţi de tiocianaţi, nitraţi şi glicozizi cianogenetici, şi o cantitatea apreciabilă de metil-sulfoxid cisteină, aminoacid cu acţiune intens hemolizantă.
Clinic, exprimările sunt dominate de slăbire, hipogalaxie, mucoase palide pe un fond icteric sau subicteric, urină de culoare brun-negricioasă/brun-verzuie, din cauza hemoglobinuriei şi coluriei. În suspiciunea diagnostică se au în vedere datele din ancheta nutriţională, anemia (macrocitară hipocromă cu tendinţă regenerativă) cu hemoglobinurie şi icter.
În cazurile de intoxicaţie cu ceapă (cu incidenţă mai redusă), aceste modificări se înregistrează după consumul acesteia timp de 5-7 zile. Ceapa (Allium cepa) conţine o fracţiune hemolitică (metapropildisulfid), un antioxidant care inhibă de fapt G6PDH, determinând hemoliză cu formare de corpi Heinz. Exprimarea clinică este dominată de constipaţie alternând cu diaree, tahicardie, polipnee, mucoase aparent palide, subicterice sau icterice, poliurie, urină de culoare roşie-brună, iar fecalele conţin resturi de ceapă. Respiraţia, urina şi fecalele au un miros aliaceu caracteristic. Orientările de diagnostic vizează tulburările digestive asociate semnelor hemolizei, halena cu miros aliaceu specific şi rezultatele examenului hematologic. Însă cele mai frecvente anemii la suine sunt de ordin carenţial, recunoscând o incidenţă crescută atât în sistemul intensiv, cât şi în cel extensiv de creştere.
În etiologia acestor anemii carenţiale (prin carenţă/deficit) practic pot fi implicaţi toţi factorii plastici şi catalitici din eritropoieză (proteină, fier, cupru, acid folic, ciancobalamină).
Deficitul de proteină poate fi unul global sau parţial (deficitul de aminoacizi, necesari atât sintezei hemului, cât şi sintezei globinei). Aportul necorespunzător de cobalamină, respectiv vitamina B12, determină reducerea eritropoiezei (şi apariţia de metamielocite gigante în măduva osoasă hematogenă, precum şi reticulocitoză). Piridoxina (vitamina B6) este necesară pentru utilizarea fierului în sinteza hemoglobinei, iar deficitul acesteia, de asemenea, va avea consecinţe detrimentale în eritropoieză.
Deficitul în acid folic va fi urmat de insuficienţa eritropoiezei (întrucât acidul folic interferează din punct de vedere metabolic cu alte elemente, în special ciancobalamina şi acidul ascorbic).
Carenţele minerale, singulare sau asociate, mai ales de fier, cobalt şi cupru, sunt cauze recunoscute ale anemiilor, în principal ale celor hipocrome(4,7,9,16,17,20).
În anemia cupriprivă, din cauza faptului că acest element deficitar, de altfel necesar integrării fierului în hemoglobină (intră în compoziţia enzimei ceruloplasmina), dar şi mobilizării lui din depozit şi absorbţiei lui de la nivel intestinal, eritropoieza va fi deficitară, iar consecinţele vor fi pe măsură. Cea mai întâlnită anemie carenţială la purcei este anemia feriprivă (prin deficit de fier).
Deficitul de fier este înregistrat cel mai frecvent la tineret (sugari). Este cunoscut faptul că fierul este esenţial în eritropoieză, întrucât intră în compoziţia hemului. Afecţiunea este întâlnită şi la animalele infestate cu paraziţi hematofagi sau cu pierdere cronică (redusă cantitativ) de sânge. Cei mai vulnerabili sunt sugarii, din cauza deficitului/carenţei în fier, cu consecinţe morfologice şi funcţionale multiple, constituind o cauză serioasă a pierderilor productive/economice pentru fermier.
Din punct de vedere etiopatogenetic, anemia feriprivă la purcei poate apărea consecutiv acţiunii factorilor determinaţi şi/sau favorizanţi.
Cauza principală este deficitul nutriţional de fier, conducând la o reducere a disponibilităţii în hematopoieză/hemoglobinogeneză şi, implicit, la o reducere numerică şi funcţională a hematiilor, cu consecinţele fiziopatologice aferente.
Principala consecinţă funcţională este hipoxia tisulară (deficit de oxigenare tisulară).
Este cunoscut faptul că, din săptămâna a treia, necesarul de fier este de 300-400 mg, iar la până la 40% dintre purcei li se asigură niveluri suboptime de fier (până la înţărcare, până la 35% din aceştia suferă consecinţele deficitului de fier).
Studii recente la nivel european au evidenţiat faptul că peste 46% din purcei prezintă o anemie subclinică latentă, iar peste 16% sunt anemici.
În medii naturale, purceii obţin fierul din sol, dar în fermele comerciale sursa naturală de fier este limitată la aportul nutriţional.
Nici colostrul şi nici laptele nu asigură/nu acoperă necesarul zilnic de 7-16 mg/zi (un litru de lapte de scroafă conţine aproximativ 1,5 mg de fier), oferind doar 10-20% din necesarul zilnic de fier al sugarului.
Purceii din rasele cu înaltă productivitate, respectiv din cele cu creştere rapidă, sunt expuşi unui risc şi mai mare de apariţie şi dezvoltare a anemiei.
Şi purceii mai mici (cei slăbiţi), de asemenea, prezintă o vulnerabilitate mai mare de a dezvolta anemie feriprivă, pentru că necesită o perioadă şi mai mare de alăptare.
În cazul scroafelor cu mulţi purcei, acest risc devine şi mai mare, întrucât rezervele fetale şi cantitatea de lapte şi de fier este mai mică pentru fiecare sugar.
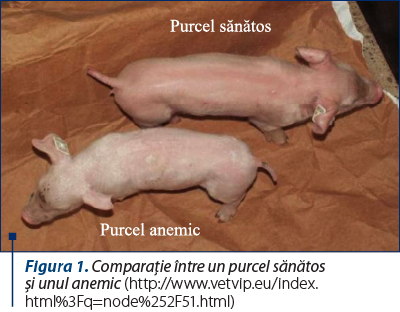
Dominantele clinice cu valoare diagnostică la purceii cu anemie carenţială (feriprivă) sunt starea de slăbiciune, cu hiporeflectivitate, hiporeactivitate şi somnolenţă, asociată cu spor ponderal redus, paloarea mucoaselor aparente şi a pielii depigmentate, dispnee, intoleranţă la efort, tahipnee şi tahicardie.
Deoarece acest tip de anemie este asociat şi cu un risc mai mare de infecţii, purceii afectaţi sunt susceptibili de a dezvolta episoade diareice.
Infecţiile respiratorii pot fi, de asemenea, o problemă din cauza capacităţii reduse de transport al oxigenului la nivel sânguin, fiind descrisă o vulnerabilitate crescută la contractarea şi dezvoltarea afecţiunilor respiratorii.
Consideraţiile anatomopatologice impun precizarea faptului că, în aceste situaţii, cazurile severe, urmate de mortalitate rapidă, permit identificarea la necropsie a edemului pulmonar, a edemelor articulare şi musculare, a dilataţiei cardiace/cardiomiopatiei dilatative (consecutiv creşterii minut-volumului şi efortului miocardic crescut), cu paloarea seroaselor şi a organelor parenchimatoase.
În ce priveşte suspicionarea şi confirmarea diagnosticului, se au în vedere următoarele elemente(4,8,14,20,22):
- purceii sugari sunt anemici la valori ale hemoglobinei sub 10-11 g/dl;
- cei cu valori ale hemoglobinei sub 11 g/dl sunt consideraţi subanemici (cu anemie subclinică);
- purceii cu hemoglobina sub 9 g/dl sunt consideraţi anemici (cu exprimări clinice caracteristice);
- la cei care nu au primit suplimente cu fier până în ziua a şasea, hemoglobina poate scădea la 7 g/dl.
- Impactul comercial pentru practica veterinară cotidiană şi pentru crescătorul de suine are în vedere următoarele consideraţii practice:
- abordarea curativo-profilactică a carenţei în fier (cu multiple consecinţe patogenetice) este de importanţă covârşitoare în creşterea şi dezvoltarea tineretului suin, respectiv în obţinerea indicilor productivi caracteristici rasei/liniei;
- purceii anemici vor avea o dezvoltare întârziată şi o creştere în greutate modestă, devenind susceptibili/vulnerabili în faţa agenţilor etiologici biotici şi abiotici;
- în evaluările de efectiv/fişele de evaluare a expoataţiilor de suine, programul profilactic de suplimentare cu preparate pe bază de fier trebuie să figureze în lista de verificare.
- Prevenirea şi tratamentul anemiei feriprive la purcei au în vedere următoarele recomandări(2,5,7,10,11,14,15,22):
- în scop preventiv (pentru a împiedica apariţia deficitului de fier) şi pentru a împiedica pierderile productive/de dezvoltare consecutivă importante, se recomandă suplimentarea în primele trei zile de la naştere;
- constituţional, purceii la naştere au o cantitate foarte mică de fier (aproximativ 50 mg), epuizându-se după trei zile – considerent important de luat în calcul pentru crescător/fermier, întrucât 40% din purcei sunt născuţi cu deficit latent sau acut de fier, devenind o componentă curativo-profilactică obligatorie pentru sistemele moderne de creştere şi exploatare a suinelor.
Varianta optimă reiese din faptul că, practic, concentraţia în fier a colostrului şi a laptelui nu poate fi îmbunătăţită prin suplimentarea hranei scroafelor. Totodată, se impune precizarea că scroafele de reproducţie – cele tinere şi cele mai în vârstă – prezintă un risc mai mare de a dezvolta un deficit de fier la fătare.
Fermierii/crescătorii pot suplimenta acest necesar în fier prin două modalităţi: oral/injectabil.
Varianta suplimentării orale este posibilă (existând forme disponibile în acest sens), dar este mai puţin eficientă în prevenirea deficitului de fier la purcei. Când se apelează la suplimentele orale, se ia în calcul faptul că o singură administrare nu este suficientă, necesitând câteva doze în primele două săptămâni de viaţă. Calea orală poate fi folosită prin încorporarea suplimentului în apă sau furaj, dar cu incertitudinea aportului corespunzător (inclusiv prin omogenizarea/dizolvarea incompletă/incorectă). Un alt inconvenient este dat de imaturitatea mucoasei intestinale şi de absorbţia digestivă limitată a fierului (în primele zile de viaţă).
Este unanim acceptată teoria variantei suplimentării injectabile a fierului la purcei, la vârsta maximei susceptibilităţi şi vulnerabilităţi. Datele ştiinţifice susţin argumentat că aceasta este modalitatea cea mai eficientă de a preveni şi de a trata anemiile prin carenţă de fier la purcei.
În practica veterinară curentă sunt disponibile numeroase formule/preparate injectabile pe bază de fier recomandate atât în scop curativ, cât şi profilactic pentru anemia feriprivă a purceilor: fierd extran (0,5-1 ml profilactic şi 1 ml curativ), Dextrafer (0,5-0,75 ml profilactic, respectiv 0,75-1 ml curativ) etc., la vârsta de 2-4 zile de la naştere(1,5,18,21,23).
Neajunsul aparent de reacţie la locul de injectare poate fi limitat prin administrarea până în ziua a treia de viaţă a acestor preparate (când rezerva de antioxidanţi din colostru şi lapte este suficientă pentru a contracara potenţialele neajunsuri).
Există preparate complexe – de tip gleptoferron – care previn anemia feriprivă şi, prin conţinutul în toltrazuril (coccidiostatic), limitează şi riscul coccidiozei (principala cauză a diareei la purcei).
Beneficiul cel mai mare al tratamentului profilactic este că avem siguranţa respectării necesarului dozei corespunzătoare.
Sunt descrise în patologia suinelor şi numeroase cauze şi tipuri de anemie hemolitică dobândită sau congenitală.
La nou-născuţi este descrisă boala hemolitică neonatală, întâlnită la purcei (dar şi la căţei, mânji şi viţei). În acest context etiopatogenetic, are loc izoimunizarea maternă faţă de antigeni eritrocitari „străini”. Aceste condiţii pot fi întâlnite în cursul gestaţiei, după vaccinarea cu vaccinuri tisulare homologe sau cu vaccinuri conţinând resturi de eritrocite, sau după transfuzii. În acelaşi context, şi hemoragiile feto-materne (cu diferite cauze) duc la izoimunizarea faţă de sistemul de grupă sanguină a fetusului. Transferul anticorpilor izoimuni are loc prin colostru, provocând hemoliza intravasculară la nou-născut.
De asemenea, anemia hemolitică autoimună (sferocitoza) este cauza acţiunii factorilor hemolitici mai mult decât a particularităţii morfologice anormale sau a tulburării în formarea eritrocitelor la nivelul măduvei osoase.
Anemia este mai accentuată în fazele primare, iar în cadrul modificărilor hematologice, sferocitoza constituie tabloul predominant. Adiţional se înregistrează hemoglobinurie (din cauza fragilităţii marcante a sferocitelor), sferocitele sunt înlocuite de macrocite policromatofile, VEM şi CHEM fiind indicatorii care pot măsura intensitatea eliberării de eritrocite imature în sânge ca răspuns la anemie. Modificările celulare pe frotiu sunt de tip normocitar-normocrom.
Pe frotiul de sânge periferic, la purceii cu anemie severă se pot observa eritroblaşti, reticulocitoză şi sferocitoză. Reticulocitoza tranzitorie observată nu este legată totdeauna de severitatea anemiei. Uneori se observă o creştere persistentă a numărului de hematii, ce poate fi asociată cu un prognostic favorabil.
Anemiile hemolitice pot fi întâlnite şi prin modificarea antigenităţii eritrocitelor proprii, după tratamente cu antibiotice, chinină, clorpromazină etc., dar şi după unele boli virale, când are loc fixarea unor particule de membrană eritrocitară, fapt ce generează complexe imunologice noi, fenomene de eritroliză şi anemie hemolitică.
Anemii hemolitice toxice pot fi induse de diferite toxine bacteriene (alfa-toxina produsă de Staphylococcus pyogenes în procesele gangrenoase) sau de substanţe toxice (plumb, compuşi fenolici, benzen).
De asemenea, frecvente sunt şi anemiile hemolitice infecţioase şi parazitare (hemobartonelloză, leptospiroză, anaplasmoză, babesioze, Mycoplasma suis, Eperythrozoon suis).
Mecanismele patogenetice sunt extrem de diferite şi de ordin particular.
În leptospiroză se produce eliberarea de hemolizine în urma lizei leptospirelor prin acţiunea anticorpilor serici şi a complementului, cu sensibilizarea eritrocitelor (care apoi sunt distruse de anticorpi şi complement, ca în anemia autoimună). Paraclinic se înregistrează anemie severă, scăderea hemoglobinei serice, a VSH‑ului şi leucocitoză, iar pe frotiul de sânge se observă anizocitoză, poikilocitoză, policromazie, eritrocite cu punctaţii bazofile, rar eritroblaşti.
În infecţiile streptococice, mecanismul de acţiune se bazează pe acţiunea specifică a streptococilor beta-hemolitici (ce produc hemoliză completă) şi a celor alfa-hemolitici (ce produc hemoliză incompletă).
Şi în infecţiile stafilococice sunt produse şi eliberate substanţe (toxice) cu însuşiri enzimatice (hemolizine, fibrolizine, hialuronidaze, fermenţi proteolitici şi o coagulază), care explică manifestările clinice extrem de complexe ce se constată în stafilococii, printre care anemia hemolitică.
Şi anumite structuri virale pot fi implicate direct în inducerea anemiei la suine. De exemplu, circovirusul porcin 2, respectiv virusul sindromului reproductiv şi respirator porcin (PRRS), mecanismul exact al anemiei nefiind identificat, însă a fost demonstrat că virusul (direct sau indirect) perturbă eritropoieza (Halbur et al., 2002).
În categoria anemiilor hemolitice congenitale, anemia prin deficit de piruvatkinază este dominată de prezenţa de eritrocite macrocitare hipocrome, prin reticulocitoză marcantă, cu rezistenţă osmotică crescută. Clinic, pacienţii exprimă aparent o stare generală nemodificată, inclusiv privind sporul de creştere, caracteristică stărilor cronice, dar prezintă o toleranţă la efort fizic diminuată, paloare anemică sau icterică-subicterică persistentă în timp şi splenomegalie.
Şi eritropoieza defectuoasă este o cauză importantă a anemiei porcinelor şi se poate dezvolta din cauza deficienţelor nutriţionale, a bolilor cronice sau a agenţilor infecţioşi.
În diverse afecţiuni de organ (organopatii) se pot întâlni numeroase astfel de anemii prin eritropoieză redusă, între care boli de organ şi de ţesuturi (nefritele cronice interstiţiale cu uremie cronică); hipotiroidismul; neoplaziile (limfosarcomatoza); hipoadrenocorticismul, enteropatii parazitare (trichostrongilidoze), diferite stări medulotoxice (boala de iradiaţie, toxicitatea estrogenilor, unele micotoxicoze). În mod particular, în nefropatiile cronice uremice are loc un deficit de eritropoietină, cu supresia consecutivă a activităţii eritropoietice a serului, precum şi reducerea metabolismului eritrocitelor; anemia este normocromă şi normocitară.
Şi în unele intoxicaţii cu medicamente se pot produce anemii de grade şi intensităţi diferite, în special în cazul celor induse de cloramfenicol, clorpromazină, sulfamide, bromuri, barbiturice, fenilhidantoine, succinimide, diazepam, carbamazepină etc.(3,12)



Conflict de interese: niciunul declarat
Suport financiar: niciunul declarat
Acest articol este accesibil online, fără taxă, fiind publicat sub licenţa CC-BY.

Bibliografie
- Antileo R, Figueroa J, Valenzuela C. Characterization of a novel encapsulated oral iron supplement to prevent iron deficiency anemia in neonatal piglets. Journal of Animal Science. 2016;94(Suppl_3):157-160.
- Bhattarai S, Framstad T, Nielsen JP. Iron treatment of pregnant sows in a Danish herd without iron deficiency anemia did not improve sow and piglet hematology or stillbirth rate. Acta Veterinaria Scandinavica. 2019;61(1):1-9.
- Codreanu MD. Terapeutica veterinară. Editura Printech, 2019.
- Codreanu MD. Patologie şi clinică medicală. Editura Printech, Bucureşti, 2022.
- Constantinescu V. Managementul bolilor suinelor. Editura Printech, Bucureşti, 2022.
- da Costa TD, Texeira AO, Moreira LM, et al. Evaluation of iron dextran application programs to prevent iron deficiency anemia in piglets. Revista Brasileira de Saúde e Produção Animal. 2023;24:20220013.
- Haoxuan D, Yu X, Feng J. Iron homeostasis disorder in piglet intestine. Metallomics. 2020;12(10):1494-1507.
- Godyń D, Pieszka M, Lipiński P, Starzyński R. Diagnostics of iron deficiency anaemia in piglets in the early postnatal period – a review. Animal Science Papers & Reports. 2016;34:307-318.
- Jończy A, Mazgaj R, Starzyński RR, et al. Relationship between down-regulation of copper-related genes and decreased ferroportin protein level in the duodenum of iron-deficient piglets. Nutrients. 2020;13(1):104.
- Jae Cheol K, Wilcock P, Bedford MR. Iron status of piglets and impact of phytase superdosing on iron physiology: A review. Animal Feed Science and Technology. 2018;235:8-14.
- Leyshon BJ, Radlowski EC, Mudd AT, Steelman AJ, Johnson RW. Postnatal Iron Deficiency Alters Brain Development in Piglets. J Nutr. 2016;146(7):1420-1427.
- McClorry S, Ji P, Parenti MG, Slupsky CM. Antibiotics augment the impact of iron deficiency on metabolism in a piglet model. J Nutr Biochem. 2023;119:109405.
- Perng V, Li C, Klocke CR, et al. Iron Deficiency and Iron Excess Differently Affect Dendritic Architecture of Pyramidal Neurons in the Hippocampus of Piglets. J Nutr. 2021;151(1):235-244.
- Perri A, Friendship R, Harding J, O’Sullivan Terri. An investigation of iron deficiency and anemia in piglets and the effect of iron status at weaning on post-weaning performance. Journal of Swine Health and Production. 2016;24(1):10-20.
- Pu Y, Li S, Xiong H, Zhang X, Wang Y, Du H. Iron Promotes Intestinal Development in Neonatal Piglets. Nutrients. 2018;10(6):726.
- Rydal MP, Bhattarai S, Nielsen JP. An experimental model for iron deficiency anemia in sows and offspring induced by blood removal during gestation. Animals. 2021;11(10):2848.
- Rytych JL, Elmore MR, Burton MD, et al. Early life iron deficiency impairs spatial cognition in neonatal piglets. J Nutr. 2012;142(11):2050-2056.
- Sawhney S, Bhattacharya D, Ponraj P, et al. Control of iron deficiency anaemia in piglets through 2-7-10-15 module of oral iron supplementation. Explor Anim Med Res. 2022;12(2):187-194.
- Staroń R, Lipiński P, Lenartowicz M, et al. Dietary hemoglobin rescues young piglets from severe iron deficiency anemia: Duodenal expression profile of genes involved in heme iron absorption. PLoS One. 2017;12(7):e0181117.
- Svoboda M, Drabek J. Iron deficiency in suckling piglets: etiology, clinical aspects and diagnosis. Folia Vet. 2005;49:104-111.
- Svoboda M, Vaňhara J, Berlinská J. Parenteral iron administration in suckling piglets-a review. Acta Veterinaria Brno. 2017;86(3):249-261.
- Szabo P, Bilkei G. Iron deficiency in outdoor pig production. Journal of Veterinary Medicine Series A. 2002;49(7):390-391.
- Szudzik M, Starzyński RR, Jończy A, Mazgaj R, Lenartowicz M, Lipiński P. Iron Supplementation in Suckling Piglets: An Ostensibly Easy Therapy of Neonatal Iron Deficiency Anemia [published correction appears in Pharmaceuticals (Basel). 2019 Jan 29;12(1):]. Pharmaceuticals (Basel). 2018;11(4):128.
Articole din ediţiile anterioare
Implicaţiile stresului de transport asupra bunăstării şi sănătăţii suinelor
În practica medicală veterinară şi în creşterea semiintensivă/intensivă a animalelor de interes economic, grija pentru bunăstarea acestora este ese...