Urinary tract infection (UTI) is an important issue in pediatric ambulatory practice which causes stress to the child, worries the parents and can lead to permanent kidney damage. Diagnosing UTI in infancy can be realy difficult due to nonspecific symptoms at this age. Family doctors must know that young children presenting with an occult cause of febrile illness may have acute pyelonephritis. In ambulatory practice, if the child is under two years old, it is quite difficult to obtain an uncontaminated urine sample for analysis and culture. Prompt diagnosis and effective treatment of a febrile UTI may prevent acute and long-term complications. Collaboration between family doctors and pediatric nephrologist is essential for an appropriate follow-up of those at high risk of recurrence and/or renal scarring. This article reviews recent evidence regarding the diagnosis, treatment, evaluation and monitoring of children with UTI.
Infecţia tractului urinar la copil
Urinary tract infection in children
First published: 03 ianuarie 2016
Editorial Group: MEDICHUB MEDIA
Abstract
Rezumat
Infecția tractului urinar la vârsta pediatrică este o patologie importantă, care poate avea impact negativ pe termen lung asupra funcționalității renale, producând disconfort atât copilului, cât și familiei. Din cauza manifestărilor clinice nespecifice la sugar și copilul mic, pentru a diagnostica un episod de infecție urinară trebuie să existe un grad înalt de suspiciune din partea clinicianului. Infecția urinară la sugar și copilul mic este de cele mai multe ori o pielonefrită acută care se poate manifesta clinic la debut doar cu stare febrilă. Recoltarea unei probe de urină la copilul sub 2 ani poate fi o adevărată provocare în condiții de ambulatoriu, deoarece pot să apară multe rezultate fals pozitive. Diagnosticarea corectă și urmărirea copilului după un episod de infecție urinară condiționează evoluția și prevenirea complicațiilor acute și mai ales ale celor cu impact pe termen lung. Colaborarea medicului de familie cu pediatrul nefrolog este esențială pentru evaluarea corectă a acestor copii și prevenirea complicațiilor precoce și tardive. Acest articol prezintă ultimele actualizări legate de diagnosticul, tratamentul, evaluarea și monitorizarea copiilor diagnosticați cu infecție de tract urinar.
Importanța problemei
Infecţia tractului urinar (ITU) la vârsta pediatrică reprezintă o patologie importantă atât ca frecvență, ocupând locul al treilea în cadrul infecțiilor la copil, după cele de tract respirator și digestiv(1), cât mai ales din cauza dificultăților de diagnostic în practica medicului de familie.
Simptomatologia la vârstele mici este adesea înșelătoare și nespecifică, fiind o adevărată provocare pentru clinicianul din ambulatoriu, care, neavizat, poate trece superficial peste acest diagnostic(2). Conform unor studii epidemiologice, multe dintre infecțiile urinare, mai ales la sugar, rămân nediagnosticate(3) și au consecințe nefaste pe termen lung de tipul cicatricelor renale (10-15% dintre ITU febrile) și insuficienței renale cronice care necesită dializă și transplant(4).
Există încă destule controverse legate de criteriile de diagnostic, recomandările de evaluare imagistică și de antibioterapie profilactică(5).
Clasificare și definire de termeni
Există cinci sisteme de clasificare larg utilizate; pentru abordarea episodului acut, localizarea și severitatea infecției sunt primordial de apreciat(1,6,7,8).
1. Localizarea - infecții urinare joase (cistite, uretrite), cu simptomatologie sugestivă, întâlnite mai ales la copilul mare, și infecții urinare înalte (pielonefrite), cu afectarea pelvisului și a parenchimului renal, mai severe, exprimate clinic cu simptomatologie nespecifică, mai ales la sugar și copilul mic (de la tulburări de apetit și falimentul creșterii până la sepsis).
2. Episodul de infecție urinară poate fi:
- Prima infecție - poate semnala o anomalie anatomică care trebuie investigată.
-
Infecții de tract urinar recurente - pot fi reinfecții sau recăderi(9):
- reinfecție - fiecare episod poate fi cauzat de un alt microorganism (pot fi serotipuri diferite de E. coli);
-
recăderi;
- • infecții nerezolvate, din cauza terapiei inițiale neadecvate (doze neadaptate, absorbție intestinală deficitară, asociere de germeni), care nu reușește să elimine germenii din tractul urinar;
- • infecții persistente datorate existenței anomaliilor anatomice (litiază renală, abces renal, diverticuli uretrali, fistule vezico-intestinale/rectale/vaginale etc.) care favorizează persistența focarului microbian (obișnuit, se izolează același agent microbian, la scurt timp după rezolvarea episodului inițial).
3. Severitatea unui episod de ITU - se apreciază în funcție de vârsta pacientului, localizarea infecției, expresia clinică și complianța la tratament; luând în considerare acești parametri, se decid spitalizarea și calea de administrare a medicației.
4. Simptomatologia
- Bacteriuria asimptomatică este depistată în cursul investigațiilor de screening, la copii aparent sănătoși, în special fetițe de vârstă școlară. Reprezintă colonizarea tractului urinar cu serotipuri nevirulente sau rezistența înnăscută a gazdei la infecțiile cu uropatogeni. Nu se recomandă tratament cu antibiotic, doar monitorizare.
- Bacteriuria simptomatică - exprimare variabilă, cu semne sugestive ce permit diagnosticarea facilă (copilul mare, verbal, frecvent ITU joase), sau simptomatologie nespecifică (sugar și copilul mic, ITU înalte), care face dificilă diagnosticarea infecției dacă nu există un grad înalt de suspiciune din partea clinicianului.
5. ITU complicate (la nou-născut și sugarul mic, pielonefrite, substrat malformativ, ITU atipice) sau necomplicate (cistitele simple și uretritele).
Epidemiologie
Incidența infecției de tract urinar în copilărie nu este pe deplin cunoscută, existând variații mari în diverse studii epidemiologice. Există o afectare mai frecventă a sexului feminin față de cel masculin, cu excepția perioadei de nou-născut și sugar mic, când băieții au o susceptibilitate mai crescută pentru infecții(8).
Studii efectuate în Suedia arată că cel puțin 3% dintre fete și 1% dintre băieți au o ITU simptomatică până la vârsta de 11 ani, în timp ce altele (Marea Britanie) sugerează că 8% dintre fete și 2% dintre băieți au cel puțin un episod de infecție urinară până la vârsta de 7 ani(10).
Într-un studiu efectuat în 2007, Shaikh et al. raportează o prevalență de 7% a infecției urinare la sugarii care se prezintă cu febră fără semne de focar(11).
Etiopatogenie
Tractul urinar, exceptând porțiunea terminală a uretrei, este steril. Colonizarea cu uropatogeni se produce mai rar prin diseminare hematogenă (sepsis, vârstă mică, tarați) și cel mai frecvent prin ascensiunea germenilor din zona perineală.
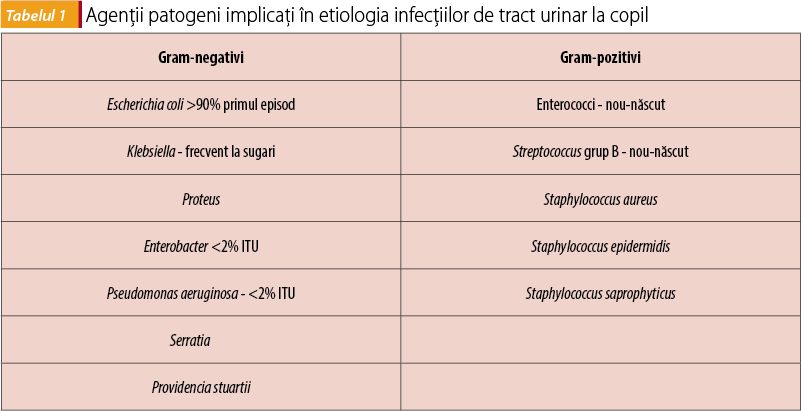
Deși ITU pot fi determinate de orice agent patogen care colonizează tractul urinar (ex: fungi, paraziți și virusuri), agenții cauzali cei mai frecvenți sunt bacteriile de origine enterică. Escherichia coli este implicată în etiologia a 80-90% din cazuri de ITU la copil, Klebsiella ocupă locul al doilea, mai frecventă la sugari, speciile de Proteus sunt izolate în aproximativ 30% din cazurile de cistită la copil(8). În cazul infecțiilor urinare care apar pe un substrat malformativ, sunt implicați agenți patogeni multidrog rezistenți (non-E. coli, ca unele specii de enterococi și Pseudomonas aeruginosa) sau asocieri de germeni(12). Adenovirusurile determină cistite hemoragice, iar infecțiile cu Candida apar obișnuit la gazde imunocompromise(3) (tabelul 1).
Există numeroase mecanisme de apărare împotriva infecțiilor urinare, printre acestea menționăm: efectul de spălare a tractului urinar prin fluxul de urină constant antegrad de la rinichi la vezica urinară și eliminarea completă și ritmică a acesteia prin uretră (previne aderența și proliferarea bacteriilor la nivelul tractului urinar), caracteristici antimicrobiene specifice ale urinei (pH-ul urinar scăzut, celulele polimorfonucleare, glicoproteina Tamm-Horsfall care inhibă aderența bacteriană la mucoasa epiteliului urinar), colonizarea regiunii perineale și periuretrale cu floră bacteriană saprofită (efect de barieră împotriva ascensionării uropatogenilor)(12).
Infectarea căilor urinare, cu implicarea deseori și a parenchimului renal, ține de o serie de condiții favorizante dependente atât de gazdă, cât și de virulența agentului patogen.
1. Factori dependenți de organismul-gazdă
- Rolul factorilor genetici - predispoziția pentru infecții de tract urinar
Severitatea unui episod de infecție urinară și recurența acesteia sunt dependente și de mecanisme de apărare înnăscute ale gazdei(13).
Copiii predispuși la infecții urinare (mai ales recurențe) au deficiențe ale mecanismelor de apărare, permițând aderența și adezivitatea uropatogenilor la nivelul mucoasei tractului urinar, cu declanșarea în cascadă a fenomenelor inflamatorii. Aceste mecanisme de apărare sunt codificate genetic și există variații individuale în ceea ce privește gradul de expresie al receptorilor uroepiteliali, capabili să recunoască agentul patogen și să activeze celulele cu eliberarea de mediatori ai inflamației (citokine proinflamatorii, fracții ale complementului, molecule de adeziune)(14).
Această reacție inflamatorie destinată clearance-ului bacterian poate determina leziuni la nivelul căilor urinare și al parenchimului renal. Variabilitatea răspunsului inflamator se traduce prin grade diferite de manifestare clinică, de la bacteriuria asimptomatică (receptorii de suprafață sunt blocați și nu se declanșează cascada inflamatorie) la pielonefrită, infecții recurente și cicatrice renale.
- Deficiențe de apărare nespecifice, deficit local de IgA secretor (alimentația la sân în primul an de viață poate fi considerată un factor de protecție).
- Boli metabolice: diabetul zaharat.
- Anomalii funcționale ale tractului urinar: tulburări funcționale ale vezicii urinare care nu permit golirea completă, tulburări sfincteriene (vezica neurogenă, instabilitatea vezicală), comportamentul retențional (în special la fetițe, care nu pot elimina în condiții improprii).
- Anomalii anatomice: refluxul vezico-ureteral (RVU), malformații (valve de uretră posterioară, diverticuli vezicali, stenoza joncțiunii pielo-ureterale, ureterocel, fistule vezico-intestinale/rectale/vaginale), anomalii ale sistemului pielocaliceal, litiaza renală etc.
- Perturbarea florei saprofite (cu rol de barieră) prin cure repetate de antibiotice are drept consecințe multiplicarea germenilor patogeni atât în colon, cât și în zona periuretrală.
- Igiena perineală deficitară, mai ales la fetițe, permite ascensiunea germenilor din tractul digestiv prin contaminarea cu fecale a zonei periuretrale.
- Constipaţia cronică.
- Manevre urologice - cateterizarea uretrală repetată.
- Sexul feminin este mai predispus la infecții de tract urinar - uretra scurtă, meatul urinar în vecinătatea orificiului anal, infecții de tipul vulvo-vaginitei, infestările parazitare care antrenează prurit anal (oxiuroza). Prima infecție urinară la vârsta adolescenței poate fi un marker al debutului vieții sexuale.
- La sexul masculin, circumcizia e asociată cu un risc mai mic de infecții urinare, mai ales în primul an de viață(15,16).
2. Factori care țin de virulența agentului patogen: atașarea E. coli de receptorii căilor urinare se realizează prin intermediul unor prelungiri denumite fimbrii. Cele mai cunoscute sunt fimbriile P. Ele recunosc antigenele de grup sanguin de tip P de la nivelul tractului urinar. Mai intervin: antigenele K (capsulare), cu rol de protecție împotriva fagocitozei germenilor, antigenele O, hemolizina, aerobactimul, enterobactimul, ureaza și proteaza produse de Proteus (ureaza scindează ureea, având ca rezultat creșterea concentrației de NH4 în urină, cu alcalinizarea acesteia)(8).
Diagnostic
Diagnosticul infecției de tract urinar la copil presupune parcurgerea următoarelor etape: suspiciunea clinică, colectarea unei probe de urină și analiza acesteia, investigații necesare precizării sediului ITU și complicațiilor asociate (laborator, imagistică)(17,18,19).
Anamneza bolnavului poate furniza elemente importante pentru orientarea diagnostică:
- creștere deficitară;
- episoade febrile anterioare de etiologie incertă;
- pierderea controlului sfincterian (enurezis);
- anomalii ale jetului urinar;
- ITU în antecedente sau uropatie cunoscută;
- antecedente heredocolaterale de RVU/alte anomalii genito-urinare;
- anomalii ale aparatului urinar decelate intrauterin (morfologie fetală).
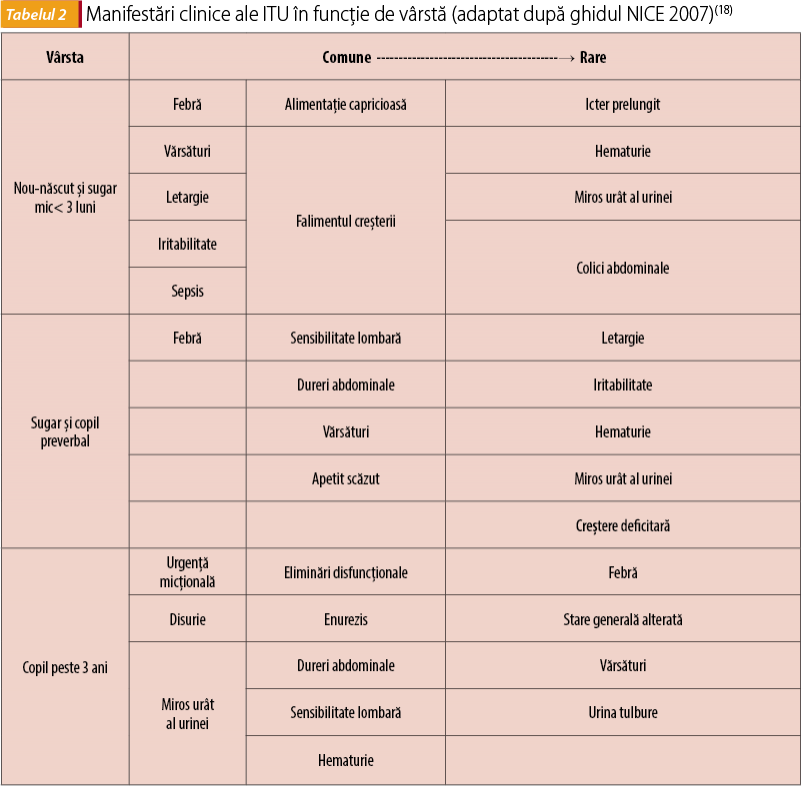
Manifestări clinice în funcție de vârstă (tabelul 2)
1. Nou-născut și sugar mic - simptomatologie nespecifică, polimorfă. Tabloul clinic cuprinde o paletă de simptome de gravitate variabilă, de la febră izolată până la sepsis.
- febră izolată (>24-48 de ore);
- simptomatologie digestivă: vărsături, diaree, apetit capricios;
- iritabilitate/letargie, convulsii;
- stare generală alterată;
- falimentul creșterii;
- icter prelungit la nou-născut;
- sepsis.
2. Sugar peste 3 luni și copil mic (1-3 ani) - frecvent simptomatologie nespecifică, cu grade variate de severitate, traduse prin:
- sindrom febril prelungit;
- febră >39°C (24-48 de ore) fără semne de focar;
- falimentul creșterii în condițiile unei îngrijiri corecte;
- diaree trenantă;
- stare septică.
Rareori simptome specifice, remarcate de către părinți: agitație/plâns în timpul micțiunii, miros urât al urinei, lizereu roșiatic pe scutec, oligurie.
3. Copilul mare, verbal - simptomatologie specifică asemănătoare celei de la adult, cu tabloul clasic de cistită sau pielonefrită.
Examenul clinic este esențial în orientarea diagnostică și stabilirea severității bolii:
- Măsurarea temperaturii, a pulsului și a tensiunii arteriale.
- Aprecierea stării de hidratare.
- Analiza curbei de creștere.
- Palparea abdomenului - mase tumorale/durere, examinarea sensibilității punctelor ureterale.
- Examinarea regiunii genitale pentru a căuta anomalii anatomice (fimoză, coalescență labială, secreții genitale, vulvo-vaginită);
- Examinarea regiunii sacrate - semne de mielodisplazie ocultă (pigmentare mediană, pilozitate localizată, fosetă suprasacrată, sinus pilonidal) - asocieri cu vezica neurogenă.
- Căutarea altor surse de febră.
Aprecierea severității bolii - criterii de spitalizare:
- terenul: vârsta <3 luni, uropatie cunoscută, imunodeprimat;
- stare generală alterată (posibil sepsis): hiper-/hipotermie, letargie/iritabilitate/convulsii, geamăt, tulburări hemodinamice (paloare/cianoză/marmorat, timp de recolorare capilar peste 3 sec.), deshidratat, icter;
- pionefroză/abces renal - rinichi voluminos, dureros spontan sau la palpare;
- evoluție nefavorabilă cu terapia inițiată în ambulatoriu;
- nu tolerează medicația administrată p.o.;
- dificil/imposibil de urmărit în ambulatoriu.
Diagnosticul de laborator
Orice suspiciune clinică de infecție a tractului urinar trebuie investigată prin teste de laborator menite să confirme infecția, să îi precizeze sediul și să identifice agentul etiologic.
1. Există teste de screening (bandelete reactive) care pot depista prezența leucocitelor și a nitriților în urină, având valoare predictivă negativă de 97%, orientând rapid clinicianul și evitând excesul de investigații. Testul screening negativ infirmă diagnosticul de ITU și nu mai este necesară urocultura. Face excepție sugarul cu vârsta mai mică de 3 luni(20,21,22).
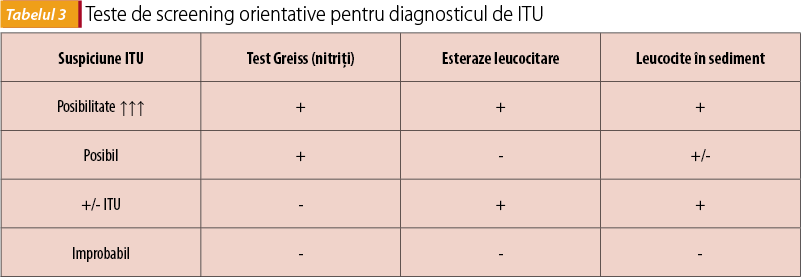
Examenul sumar de urină poate aduce informații utile în ceea ce privește prezența piuriei (>10 leucocite pe câmp în sedimentului urinar centrifugat), proteinuriei, hematuriei, bacteriuriei, care pot crește probabilitatea diagnosticului de ITU (tabelul 3).
- prezența esterazelor leucocitare se corelează cu piuria (>10-20 leucocite/mmc în sedimentul urinar);
- absența piuriei în condițiile unei uroculturi pozitive poate semnifica bacteriurie asimptomatică;
- piuria poate să apară și în alte circumstanțe: apendicită acută, deshidratare, post-traumatic, glomerulonefrite, vaginite, uretrite, litiază renală etc.;
- test Greiss fals negativ - nitriții sunt produși de conversia nitraților din urină prin acțiunea bacteriilor gram-negative (BGN); pot să existe rezultate fals negative în ITU cu coci gram-pozitivi;
- un test screening pozitiv este obligatoriu urmat de urocultură(10).
2. Teste diagnostice - examenul citobacteriologic al urinei (ECBU) sau urocultura (izolarea agentului etiologic și efectuarea antibiogramei) reprezintă gold standard pentru diagnosticul de ITU.
Pentru a putea interpreta corect rezultatele unei uroculturi, recoltarea corectă este esențială, fiind condiția primordială pentru a evita excesul de diagnostic și terapia inutilă cu antibiotic. Există mai multe metode de recoltare a unei probe de urină, eligibile în funcție de vârsta copilului, gravitatea bolii și experiența serviciului medical. Recoltarea corectă a unei probe de urină la sugar și la copilul mic, în condiții de ambulatoriu, poate fi o adevărată provocare.
- Metodele neinvazive:
recoltarea urinei din jetul urinar mijlociu este posibilă doar la copilul mare, care are control sfincterian și poate colabora;
recoltarea în pungi colectoare sterile este singura metodă accesibilă în condiții de ambulatoriu la sugar și la copilul mic. Chiar dacă se respectă condițiile de recoltare (igienă riguroasă, schimbarea colectorului steril la maximum 30 de minute dacă sugarul nu a emis urină, transportul la laborator al probei colectate în maximum 30 de minute și însămânțarea probei în maximum două ore de la recoltare), în 85% din cazuri rezultatele sunt fals pozitive, motiv pentru care ghidurile americane nu recomandă această metodă de recoltare a urinei. Obținerea unei uroculturi negative prin această metodă poate însă exclude diagnosticul de ITU (valoare predictiv negativă foarte bună)(23,24,25).
- Metodele invazive sunt puncția suprapubiană ghidată ecografic și cateterismul (sondajul) vezical cu sondă Nélaton sterilă. Aceste metode sunt accesibile doar în condiții de spitalizare. În ghidurile internaționale există încă divergențe privind recomandările. Astfel, ghidurile americane le consideră metode de elecție pentru recoltarea urinei la sugar și copilul mic (sub 2 ani), în timp ce unele ghiduri europene recomandă utilizarea metodelor invazive doar atunci când nu există posibilitatea de recoltare a unei probe de urină prin metode neinvazive (Ghid NICE, 2007).
Interpretarea uroculturii se face în funcție de metoda de recoltare utilizată:
-
Criteriile Kass de interpretare a uroculturii își mențin valabilitatea dacă recoltarea s-a efectuat prin metode neinvazive:
- peste 100.000 de colonii/ml de urină = bacteriurie semnificativă = urocultură pozitivă;
- sub 10.000 de colonii/ml de urină - urocultură negativă (absența infecției urinare);
- între 10.000 și 100.000 colonii/ml de urină - zona discutabilă, necesită repetarea examenului sau poate fi interpretată ca pozitivă în anumite condiții: „infecție urinară «decapitată» (recoltarea urinei după inițierea tratamentului cu antibiotic), prezența unor simptome clinice sugestive (febră, disurie, polakiurie, dureri lombare etc.), bacteriurie acută intermitentă, prezența unui microorganism dificil de cultivat pe medii obișnuite, posibilitatea inactivării bacteriene la recoltare (utilizarea soluțiilor antiseptice pentru toaleta locală înaintea efectuării uroculturii), urina diluată (diureză abundentă, flux rapid al urinei), izolarea - în cursul unei recidive a infecției urinare a unui agent urobacterian identic cu cel inițial”(1,12).
Din cauza ratei mari de uroculturi fals pozitive la sugar și copilul mic, orice cultură pozitivă obținută prin colectarea cu ajutorul pungilor sterile trebuie verificată prin altă metodă de colectare a urinei înainte de inițierea tratamentului(26).
Pe de altă parte, trei uroculturi pozitive cu același germene cresc probabilitatea de diagnostic pozitiv de ITU, din acest motiv, dacă condițiile clinice permit, este recomandabilă amânarea inițierii oricărui antibiotic până se recoltează minimum două probe de urină pentru urocultură(8).
n În cazul utilizării metodelor invazive, dacă recoltarea se face prin aspirație suprapubiană, orice creștere de germeni este interpretată ca urocultură pozitivă. Atunci când recoltarea s-a efectuat prin sondaj vezical, se consideră urocultură pozitivă dacă există peste 10.000 UFC/ml urină și urocultură negativă sub 1.000 UFC/ml urină(19,10).
Afirmarea diagnosticului de ITU presupune asocierea criteriului bacteriuriei semnificative (urocultura pozitivă) cu cel al piuriei. Doar urocultura pozitivă fără piurie poate sugera bacteriuria asimptomatică, în timp ce prezența doar a piuriei izolate nu semnifică automat ITU(23).
Bilanțul biologic standard în condițiile suspectării unei ITU înalte include:
- hemoleucogramă cu formula leucocitară;
- sindrom inflamator: VSH, CRP, procalcitonina (reflectă răspunsul inflamator sistemic la agresiunea endotoxinelor bacteriene, crește în infecții severe, util în diagnosticul pielonefritei și al leziunilor renale)(27,28);
- ionograma sangvină, bilanțul funcțional renal (uree, creatinină);
- hemocultura în condițiile în care se suspectează un sepsis.
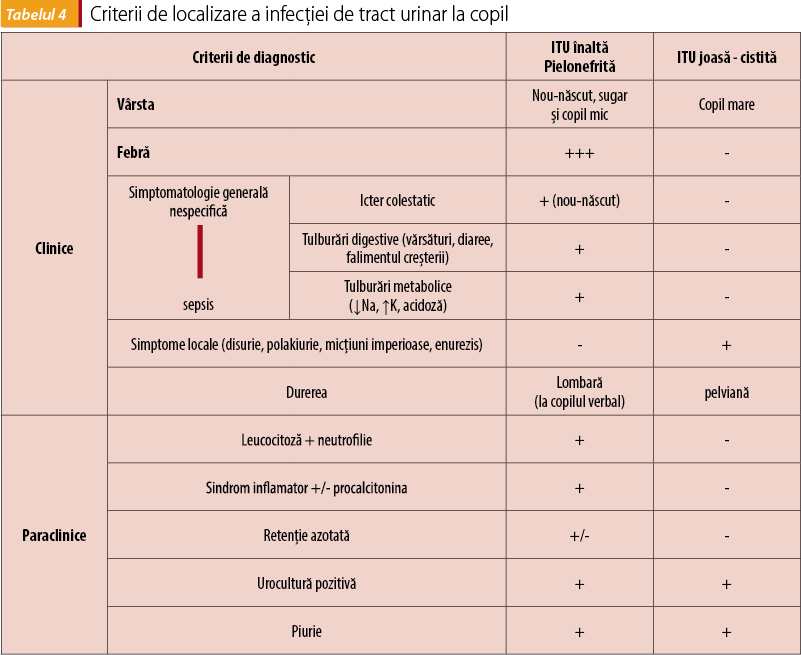
3. Evaluarea sediului și severității ITU - criterii de localizare a infecției urinare. Deoarece simptomatologia unei infecții urinare la copil nu este întotdeauna sugestivă, uneori este dificil de diferențiat între ITU „joasă” sau „înaltă”. Deoarece copiii sub 5 ani sunt o categorie vulnerabilă, cu risc crescut de a dezvolta leziuni ale parenchimului renal secundar unei ITU, în practică se recomandă să considerăm și să tratăm infecția tractului urinar ca și cum ne-am afla în prezența unei forme „înalte” sau „complicate”(12).
Există câteva criterii de diferențiere în tabelul 4.
4. Investigațiile imagistice se efectuează în scopul descoperirii unui eventual substrat malformativ care a favorizat apariția ITU pentru aprecierea severității bolii și a leziunilor renale.
-
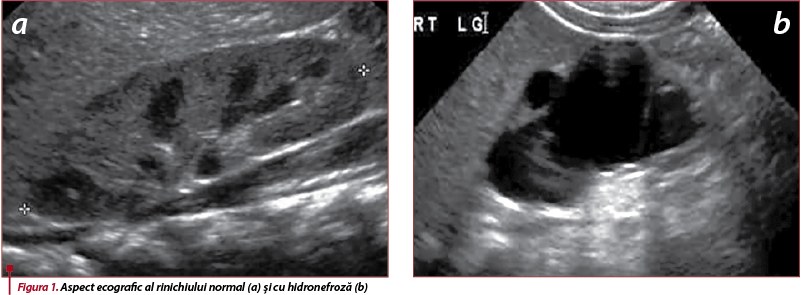
Ecografia renală
- detectează anomalii renale și vezicale, dimensiunile rinichilor, ale corticalei renale, hidronefroza (figura 1);
- este un instrument diagnostic valoros, permițând excluderea unui RVU de grad IV sau V, a abcesului renal etc.(29);
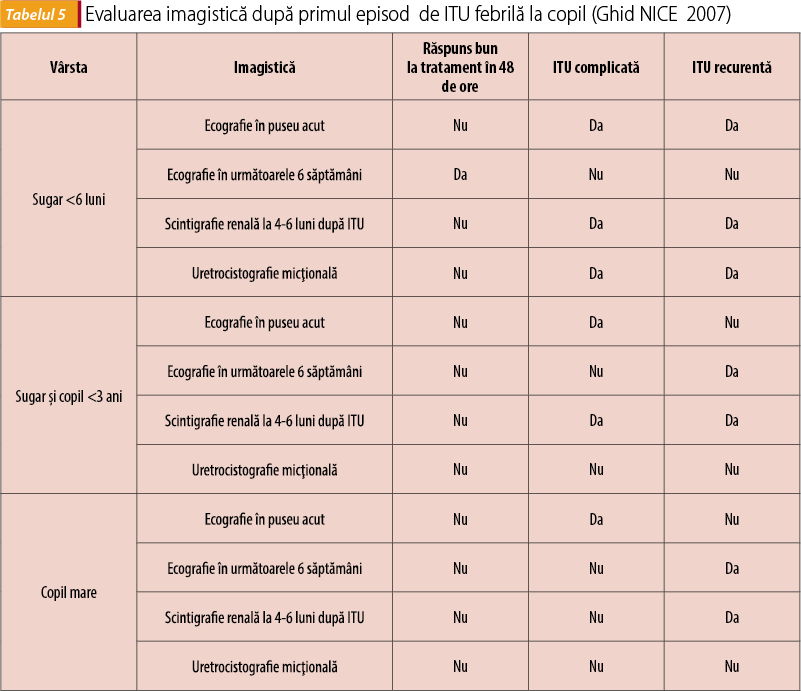
- se recomandă în toate cazurile după primul episod de infecție de tract urinar (în anumite situații se efectuază în puseul acut, tabelul 5), excepție face primul episod de cistită la fetițe;
- ecografia renală efectuată antenatal poate detecta diferite grade de hidronefroză la făt și este necesară reevaluarea ecografică precoce postnatal sau la vârsta de 4-6 săptămâni, în funcție de situație. Dacă persistă hidronefroza, oportunitatea evaluării imagistice suplimentare pentru depistarea RVU (conform studiilor, se poate asocia în 12% dintre cazuri) este în prezent controversată(30).
-
Uretrocistografia micțională (cistografia retrogradă)
- este investigația de elecție pentru diagnosticarea refluxului vezico-ureteral (RVU);
- fiind o investigație invazivă, este necesar consimțământul informat al tutorilor legali ai copilului;
- se recomandă după primul episod de ITU înaltă, dacă ecografia decelează anomalii (hidronefroză, cicatrice renale sau alte anomalii anatomice), dacă există istoric familial de RVU, anomalii ale jetului urinar sau după al doilea episod de ITU înaltă la sugar și copilul mic (tabelul 5)(18,23);
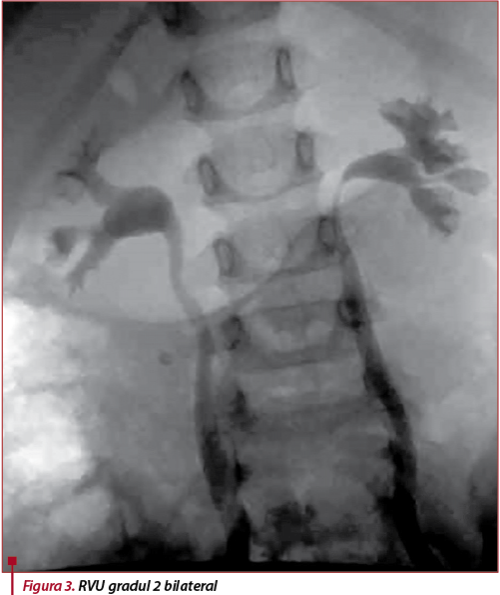
- există grade diferite de RVU (figurile 2 și 3), doar în cazurile severe (gradul IV sau V) este necesară profilaxia recidivelor de infecție urinară și corecție chirurgicală(17).
- Scintigrafia renală cu 99mTc DMSA (acid dimercaptosuccinic) reprezintă gold standardul pentru detectarea cicatricelor renale, permițând evaluarea parenchimului renal(31). Prezența unui defect de fixare parenchimatoasă sugerează pielonefrită, dar nu poate diferenția o formă acută de una cronică, motiv pentru care momentul investigației trebuie ales la un interval mai lung (câteva luni) de la producerea infecției (figura 4). Scintigrama radioizotopică cu Tc99–DTPA (acidul dietilentriaminpentaacetic), substanță care se regăsește în urina primară, furnizează date asupra perfuziei renale, filtrării glomerulare și a funcției de excreție, cu avantajul de a furniza informații separate despre funcționalitatea fiecărui rinichi(32,33,34,35).
- Alte investigaţii imagistice: IRM, CT scan se utilizează în formele complicate sau în cadrul bilanțului preoperator pentru cura chirurgicală a malformațiilor renale. Tomografia computerizată furnizează informații exacte despre anomaliile renourinare și caracterizează organele adiacente și structurile vasculare. Este examenul de elecție pentru diagnosticul „maselor renale”(35). Rezonanța magnetică nucleară furnizează date precise asupra prezenței, poziției și orientării rinichilor. Se utilizează rar în ITU, în special când infecția se asociază cu mase intrarenale, agenezie sau ectopie renală(35).
Tratament
Abordarea terapeutică a copiilor cu infecție de tract urinar se face ținând cont de vârsta copilului, severitatea infecției și patologia asociată. Inițierea terapiei cu antibiotice se recomandă cât mai precoce, după prelevarea corectă a cel puțin unui eșantion de urină pentru examen citobacteriologic.
Alegerea antibioticului se face inițial empiric, ținând cont de vârstă, contexul clinic și sensibilitatea teoretică a germenilor, conform datelor regionale privind rezistența la antibiotice a uropatogenilor comuni(36).
Studii numeroase din ultima decadă au arătat că există o rezistență în creștere la antibiotice. Încă din 2006(37), s-a constatat că E. coli are o rezistență considerabilă la antibioticele b-lactamice (37,7%) și trimetoprim-sulfametoxazol (21,3%), motiv pentru care aceste antibiotice nu sunt recomandate de primă intenție în ITU severe. În ultimii ani, sistemele de supraveghere europene (ECDC) raportează o situație îngrijorătoare: creșterea procentului de tulpini E. coli producătoare de betalactamaze cu spectru extins (BLSE). În România, în 2013, rezistența tulpinilor de E. coli la cefalosporinele de generația a III-a era între 10% şi 25% și rezistența combinată la cefalosporine, fluorochinolone și aminoglicozide se situa între 5% şi 10%. Există un trend ascendent al acestui fenomen, amplificat de utilizarea în exces a antibioticelor în România (ne situăm printre cei mai mari consumatori de antibiotice din Europa, alături de Franța și Grecia)(38,39).
Numeroase studii clinice randomizate conduse în ultimii ani au arătat că, în tratamentul pielonefritei acute, administrarea antibioticului pe cale orală are eficiență similară celei parenterale, în ceea ce privește ameliorarea clinică și prevenirea cicatricelor renale; recomandările trebuie să țină cont de: vârstă, severitatea bolii și toleranță(40,41).
1. Principii de tratament în pielonefrita acută:
- Spitalizarea se recomandă pentru: nou-născut și sugarul sub 3 luni, sugar sau copil cu semne clinice severe, uropatie cunoscută. În celelalte cazuri se poate trata și urmări copilul în ambulatoriu.
- Terapia de atac se administrează inițial parenteral (i.v.), pentru 2-4 zile (48 de ore de apirexie). Se utilizează cefalosporine de generația a III-a: ceftriaxone (peste vârsta de o lună) sau cefotaxime (primă alegere la nou-născut).
-
Aminoglicozidele se recomandă în patru situații(17):
- în asociere cu cefalosporinele de generația a III-a în pielonefritele severe, la sugarul sub 3 luni, la imunodeprimați, în caz de uropatie subiacentă cunoscută sau sepsis;
- în monoterapie, în caz de alergie la antibiotice betalactamice, la pacienți cu funcție renală normală;
- în monoterapie, în cazul unor sușe de E. coli rezistente la cefalosporine;
- în infecția cu Enterococ se asociază cu amoxicilina/ ampicilina.
- Tratamentul de atac se continuă cu antibiotic administrat oral (p.o.) până la 10-14 zile, utilizând cefixime sau cotrimoxazol (după vârsta de o lună), adaptat în funcție de rezultatul antibiogramei.
- Ciprofloxacina (eficiență crescută pe majoritatea uropatogenilor) rămâne o terapie de rezervă recomandată în cazul infecției cu germeni multidrogrezistenți și Pseudomonas(42,41).
2. Tratamentul ITU joase (cistitei) - se recomandă alegerea unui antibiotic cu o concentrație bună în urină (nitrofurantoin, cotrimoxazole sau cefalosporine), administrat pe cale orală, pentru o perioadă de 3-5 zile (regimurile scurte au eficiență similară cu regimul terapeutic de 7-10 zile)(43,42,39).
Tratamentul cu antibiotic trebuie asociat cu administrare abundentă de lichide, igienă locală și tratamentul condițiilor medicale asociate care predispun la recidivă (constipația, oxiuroza, vezica instabilă etc.)(8,23,18).
Monitorizarea sugarului și a copilului după un prim episod de ITU
Cu terapie adecvată, răspunsul la tratament apare obișnuit în 24-48 de ore: urina devine sterilă după 24 de ore, leucocituria dispare în 3-4 zile și în 90% dintre cazuri copilul devine afebril în 24-48 de ore. La copiii cu stare febrilă prelungită trebuie suspectată infecția cu un germene rezistent la tratamentul inițiat sau prezența unei uropatii congenitale(7).
Repetarea uroculturii în timpul sau la finele tratamentului se recomandă doar în caz de evoluție nefavorabilă sau dacă antibiograma confirmă prezența unui germene rezistent la terapia inițiată(17,23).
Urmărirea copilului în primele 72 de ore este deosebit de importantă, mai ales dacă s-a decis tratarea acestuia în ambulatoriu, instruirea familiei și evaluarea zilnică permit aprecierea corectă a evoluției și depistarea precoce a complicațiilor acute: sepsis, deshidratare, abces renal sau pionefroză.
Chiar după primul episod de ITU sunt importante cercetarea substratului pe care a survenit infecția, identificarea factorilor de risc menționați anterior și corectarea acestora în măsura în care este posibil: evitarea constipației, igiena perineală riguroasă, echilibrarea florei intestinale (probiotice, simbiotice), evitarea abuzului de antibiotice, educarea sfincteriană diurnă la vârsta potrivită (18 luni), tratamentul vezicii instabile (clorhidrat de oxibutinină), corecția chirurgicală a malformațiilor aparatului urinar atunci când se impune.
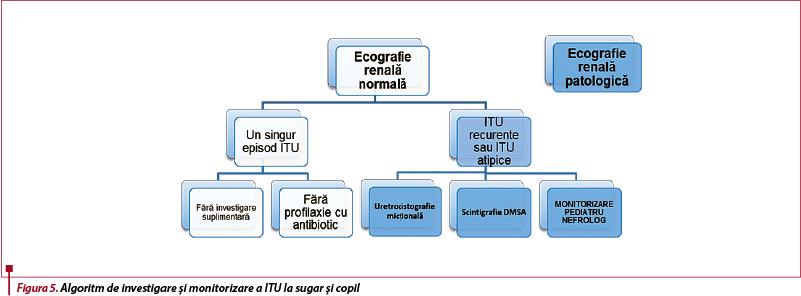
Investigarea imagistică suplimentară este necesară dacă apar recurențe ale infecțiilor urinare (posibile în 30% dintre cazuri)(17), în ITU complicate sau atipice, în cazurile în care au fost depistate anomalii ecografice (tabelul 5).
Riscul de recurență după un prim episod de pielonefrită acută este de 30%(17), motiv pentru care este important ca familia copilului să fie informată pentru a putea sesiza imediat semnele sugestive de infecție urinară, impunându-se recoltarea unei probe de urină în orice episod febril care survine în evoluția acestor copii.
Monitorizarea sugarului și a copilului după un prim episod de ITU febrilă permite atât depistarea, cât și prevenirea complicațiilor tardive. Conform unei metaanalize efectuate de către Shaikh et al. în 2010, în aproximativ 10-15% din cazuri, un prim episod de pielonefrită acută conduce la cicatrice renale(4), care pot determina în timp afectarea funcției renale, hipertensiune arterială, pre-eclampsie și uneori insuficiență renală cronică(45).
Incidența reală a bolii cronice renale în faza terminală, secundară ITU din copilărie, rămâne necunoscută, dar e posibil să fie destul de rară și continuă să fie un subiect controversat(46).
O metaanaliză efectuată de Shaikh et al. în 2014 cuantifică următorii factori de risc asociați cu apariția cicatricelor renale secundare infecției urinare (în ordine descrescătoare în ceea ce privește importanța): RVU grad IV sau V, anomalii la examenul ecografic renal, RVU grad III, proteina C reactivă peste 40 mg/L, temperatura de cel puțin 39°C, infecția cu alt microorganism decât E. coli, polimorfonucleare peste 60% și RVU grad I sau II. Ceilalți factori investigați, vârstă, sex, durata episodului febril, nu s-au asociat semnificativ cu apariția cicatricelor renale(45,46).
În ultimii ani, eficiența și necesitatea profilaxiei cu antibiotice după un episod de ITU este în continuă dezbatere. Din ce în ce mai multe studii au dovedit că există beneficii minore în ceea ce privește riscul recurențelor și prevenția apariției cicatricelor renale(47).
Dimpotrivă, recomandările clasice, prin utilizarea în exces a antibioticelor, au permis selectarea de microorganisme rezistente și la dezechilibrarea microbiotei intestinale. Din aceste motive, în prezent, se recomandă profilaxie antimicrobiană doar în următoarele cazuri: reflux vezico-ureteral de gradul IV sau V(7), alte uropatii malformative până la corecția chirurgicală, cistitele recidivante la fetițe (cotrimoxazol timp de 3 luni dacă episoadele sunt frecvente)(17).
Concluzii
- Pentru a diagnostica un episod de ITU la sugar și la copilul mic, trebuie să existe un grad înalt de suspiciune, impunându-se recoltarea unei probe de urină în orice stare febrilă fără semne de focar care apare la copilul sub 2 ani.
- Identificarea și tratarea condițiilor favorizante asociate unui episod de ITU sunt condiții esențiale pentru evoluția favorabilă a acestor copii.
- Diagnosticul și tratamentul prompt al unei ITU febrile reduc riscul de cicatrice renale și sechele pe termen lung.
- Recoltarea urinei în pungi colectoare sterile este o metodă accesibilă și larg utilizată în practica din ambulatoriu. Această metodă este utilă doar atunci când rezultatele uroculturii sunt negative. Deoarece are un potențial foarte ridicat (85%) de rezultate fals pozitive, nu este o metodă sigură pentru a afirma diagnosticul de ITU la sugar și copilul mic. Orice urocultură pozitivă obținută prin această metodă trebuie confirmată prin utilizarea altor metode de recoltare, pentru a evita excesul de diagnostic și terapie antimicrobiană.
- După un prim episod de ITU, comunicarea eficientă și instruirea atentă a familiei copilului sunt esențiale pentru diagnosticarea precoce și tratamentul prompt al unei recurențe. Se recomandă recoltarea unei probe de urină pentru examen biochimic și urocultură în cazul oricărui episod febril ce apare la un copil cu istoric de ITU.
- Nu se recomandă supravegherea prin uroculturi secvențiale periodice după primul episod de ITU.
- Nu se mai recomandă uretrocistografia micțională de rutină după un prim episod de ITU la sugar și copilul mic.
- Profilaxia cu antibiotice nu trebuie recomandată de rutină după primul episod de ITU febrilă la copilul între 2 luni și 2 ani.
- Colaborarea medicului de familie cu pediatrul nefrolog este esențială în îngrijirea corectă a acestor copii.
Bibliografie
2. Tullus K. Difficulties in diagnosing urinary tract infections in small children. Pediatr. Nephrol. 2011;26(11):1923–1926.
3. J.J. Zorc, Darcie A. Kiddoo, Kathy N. Shaw Diagnosis and Management of Pediatric Urinary Tract Infections, Clin Microbiol Rev. 2005; 18(2): 417–422.
4. Shaikh N, Ewing AL, Bhatnagar S, Hoberman A. Risk of renal scarring in children with a first urinary tract infection: a systematic review. Pediatrics. 2010;126(6):1084-1091.
5. Bauer, Ross et al, New Developments in the Diagnosis and Management of Pediatric UTIs, Urologic Clinics, 2008, 35 (1):47 – 58.
6. Tekgül S, Riedmiller H., Dogan H.S. et al., European Society of Paediatric Urology, European Guidelines on Paediatric Urology, Urinary Tract Infections in Children, (2013):31-44.
7. Stein R, Dogan HS, Hoebeke P, Kočvara R, Nijman RJ, Radmayr C, Tekgül S, Urinary tract infections in children: EAU/ESPU guidelines. Eur Urol. 2015;67(3):546-58.
8. Brumariu O., Munteanu M., Gavrilovici C., Infecţia tractului urinar. În Ciofu E., Ciofu C., Pediatria - tratat, ediţia I, București, 2001, cap. 11: 711- 718.
9. M. E. Jantunen, H. Saxe E. Salo, A. Siitonen, Recurrent Urinary Tract Infections in Infancy: Relapses or Reinfections? The Journal of Infectious Diseases 2002;185:375–9.
10. Maria Bitsori, E. Galanakis, Pediatric Urinary Tract Infections, Diagnosis and Treatment Expert Rev Anti Infect Ther. 2012;10(10):1153-1164.
11. Shaikh N, Morone NE, Lopez J, et al. Does this child have a urinary tract infection? JAMA. 2007;298(24):2895-2904.
12. V. Popescu, Infecţiile tractului urinar la copil, Rev. Română de Pediatrie, 2007, LVI, (3):267-281.
13. Mak RH, Kuo HJ., Pathogenesis of urinary tract infection: an update, Curr Opin Pediatr. 2006;18(2):148-52.
14. Zaffanello M, Malerba G, Cataldi L, Antoniazzi F, Franchini M, Monti E, et al. Genetic risk for recurrent urinary tract infections in humans: a systematic review. J Biomed Biotechnol. 2010:321082, doi:10.1155/2010/321082.
15. Schoen EJ, Colby CJ, Ray GT. Newborn circumcision decreases incidence and costs of urinary tract infections during the first year of life. Pediatrics. 2000, 105(4 Pt 1):789-93.
16. Shaikh N, Morone NE, Bost JE, Farrell MH. Prevalence of urinary tract infection in childhood: a meta-analysis. Pediatr Infect Dis J. 2008 Apr. 27(4):302-8.
17. Bellaiche M. Pediatrie, Ed Vernazobes Grego, Paris (2013); Infection urinaire: 303-310.
18. National Collaborating Centre for Women’s and Children’s Health. NICE (2007) Urinary tract infection in children: diagnosis, treatment and long term management. www.nice.org.uk/nicemedia/pdf/GG54fullguideline.pdf
19. AAP American Academy of Pediatrics. Committee on Quality Improvement. Subcommittee on Urinary Tract Infection. Practice parameter: the diagnosis, treatment, and evaluation of the initial urinary tract infection in febrile infants and young children, 1999, Pediatrics 103:843–852.
20. Whiting P, Westwood M, Watt I, Cooper J, Kleijnen J. Rapid tests and urine sampling techniques for the diagnosis of urinary tract infection (UTI) in children under five years: a systematic review. BMC Pediatr. 2005;5(1):4.
21. Laidman J. Dipstick Test Effective Initial Screen for UTI in Infants. Medscape Medical News. May, 2014.
22. Glissmeyer EW, Korgenski EK, Wilkes J, et al. Dipstick screening for urinary tract infection in febrile infants.Pediatrics. 2014, 133(5):e1121-7.
23. [Guideline] Subcommittee on Urinary Tract Infection; Steering Committee on Quality Improvement and Management. Urinary Tract Infection: Clinical Practice Guideline for the Diagnosis and Management of the Initial UTI in Febrile Infants and Children 2 to 24 Months. Pediatrics. 2011.
24. Al-Orifi F, McGillivray D, Tange S, Kramer MS. Urine culture from bag specimens in young children: are the risks too high? JPediatr. 2000;137(2):221–226.
25. Li PS, Ma LC, Wong SN. Is bag urine culture useful in monitoring urinary tract infection in infants? J Paediatr Child Health. 2002;38(4):377–381.
26. Etoubleau C, Reveret M, Brouet D, et al. Moving from bag to catheter for urine collection in non-toilet-trained children suspected of having urinary tract infection: a paired comparison of urine cultures. J Pediatr. 2009;154(6):803-806.
27. Nikfar R, Khotaee G, Ataee N, Shams S. Usefulness of procalcitonin rapid test for the diagnosis of acute pyelonephritis in children in the emergency department. Pediatr Int. 2010;52(2):196-8.
28. Bressan S, Andreola B, Zucchetta P, Montini G, Burei M, Perilongo G, et al. Procalcitonin as a predictor of renal scarring in infants and young children. Pediatr Nephrol. 2009, 24(6):1199-204.
29. A. Nickavara, B. Safaeianb, M. Biglari abharic Radiologic and clinical evaluation of children with first febrile urinary tract infection, International Journal of Pediatrics and Adolescent Medicine. 2015; 2(1):24–28.
30. Estrada CR, Peters CA, Retik AB, Nguyen HT. Vesicoureteral reflux and urinary tract infection in children with a history of prenatal hydronephrosis-should voiding cystourethrography be performed in cases of postnatally persistent grade II hydronephrosis? J Urol. 2009,181(2):801-6.
31. Paterson A – Urinary tract infection: an update on imaging strategies. Eur Radiol, 2004, 14 (Suppl 4):89 – 100.
32. Ahmed M, Eggleston D, Kapur G, Jain A, Valentini RP, Mattoo TK. Dimercaptosuccinic acid (DMSA) renal scan in the evaluation of hypertension in children. Pediatr Nephrol. 2008; 23:435–438.
33. Herz D, Merguerian P, McQuiston L, Danielson C, Gheen M, Brenfleck L. 5-year prospective results of dimercapto-succinic acid imaging in children with febrile urinary tract infection: proof that the top-down approach works. J Urol. 2010;184:1703–1709.
34. European Association of Urology. Guidelines on Urological Infections. Arnhem, The Netherlands; 2009.
35. European radiology and nuclear medicine URCoRatEC. Radiation Protection 118: Referral guidelines for imaging. http://www.radioprotection.org.
36. Chakupurakal R, Ahmed M, Sobithadevi DN, Chinnappan S, Reynolds T. Urinary tract pathogens and resistance pattern. J Clin Pathol. 2010;63:652–654.
37. Zhanel GG, Hisanaga TL, Laing NM, DeCorby MR, Nichol KA, Weshnoweski B, Johnson J, Noreddin A, Low DE, Karlowsky JA, Hoban DJ. Antibiotic resistance in Escherichia coli outpatient urinary isolates: final results from the North American Urinary Tract Infection Collaborative Alliance (NAUTICA) Int J Antimicrob Agents. 2006;27:468–475.
38. Summary of the latest data on antibiotic resistance in EU: 2014 - http://ecdc.europa.eu/en/eaad/Documents/antibiotics-resistance-EU-data-2014.pdf.
39. Saadeh SA, Mattoo TK. Managing urinary tract infections. Pediatr. Nephrol. (2011) 26(11), 1967–1976.
40. Montini G, Toffolo A, Zucchetta P et al. Antibiotic treatment for pyelonephritis in children: multicentre randomised controlled noninferiority trial. BMJ (2007) 335(7616), 386.
41. Hodson EM, Willis NS, Craig JC. Antibiotics for acute pyelonephritis in children. Cochrane Database Syst. Rev. 4, CD003772 (2007).
42. Beetz R, Westenfelder M. Antimicrobial therapy of urinary tract infections in children. Int. J. Antimicrob. Agents (2011), 38 (Suppl.):42–50.
43. Michael M, Hodson EM, Craig JC, Martin S, Moyer VA. Short versus standard duration oral antibiotic therapy for acute urinary tract infection in children. Cochrane Database Syst. Rev. 1, CD003966 (2003).
44. Saadeh SA, Mattoo TK. Managing urinary tract infections. Pediatr. Nephrol. (2011), 26(11): 1967–1976.
45. Shaikh N, Craig JC, Rovers MM, et al. Identification of Children and Adolescents at Risk for Renal Scarring After a First Urinary Tract Infection: A Meta-analysis with Individual Patient Data. JAMA Pediatr. 2014, 168(10):884-885.
46. Round J, Fitzgerald AC, Hulme C, Lakhanpaul M, Tullus K. Urinary tract infections in children and the risk of ESRF. Acta Paediatr. 2012;101(3):278-282.
47. Hayashi Y, Kojima Y, Kamisawa H, et al. Is antibiotic prophylaxis effective in preventing urinary tract infections in patients with vesicoureteral reflux? Expert Rev Anti Infect Ther 2010;8:51-8.
Articole din ediţiile anterioare
Cum influenţează „Dr. Google” deciziile noastre medicale?
În contextul proliferării accesului la informaţii medicale online prin intermediul motoarelor de căutare precum Google, acest studiu îşi propune să...
Sunt psihiatrii o specie pe cale de dispariţie? Observaţii privind provocările interne și externe ale profesiei
Pe baza preocupărilor recent exprimate în legătură cu o criză în psihiatrie, sunt identificate și discutate șase provocări pentru profesia noastră....
Evaluarea unui suflu cardiac la copil
Suflul sistolic este un simptom frecvent întâlnit în perioada copilăriei, peste 50% din copii prezentând la un moment dat un suflu cardiac(1). Majo...
Importanţa diagnosticului precoce în bolile inflamatorii reumatice
În România, mai mult de 600.000 de pacienţi (3% din populaţie), din care 2.000 de copii, suferă de boli reumatice inflamatorii precum artrita re...