Hypersensitivity reactions (HSRs) to chemotherapeutic agents have a steadily increasing incidence, with a major impact on oncological diseases outcome, inducing the discontinuity of an effective therapy. The most commonly involved agents are platinum salts and taxanes, which can cause HSRs with different degrees of severity. Given the risk of defining some adverse reactions as HSRs, it is recommended to use a well-structured allergy assessment protocol in which in vivo and in vitro specific tests have proven their utility. There is, however, a limitation of the skin tests, due to the risk of an irritant reaction even at low concentrations, despite the establishment of certain concentrations considered non-irritating for skin testing. The management of HSRs to chemotherapeutic agents provides two major options depending on the severity of the reaction and risk: resuming treatment with a modified protocol (perfusion rate, premedication, etc.) or replacement of the culprit agent. In the absence of a therapeutic alternative, the desensitisation procedure allows maintaining the therapy in safety, improving the oncological prognosis. Desensitization has been shown to be an effective therapeutic tool in chemotherapy hypersensitivity, with more and more studies presenting rapid desensitization protocols, by steps, on the basis of escalating low doses until the full therapeutic dose is reached in few hours.
The EAACI Position Paper on Allergo-Oncology provides an update in the field and demonstrates the usefulness of the allergic approach in patients with HSRs to oncological drugs.
Reacţii de hipersensibilitate la agenţi chimioterapici: săruri de platină și taxani
Hypersensitivity reactions to chemotherapeutic agents: platinum salts and taxanes
First published: 16 noiembrie 2017
Editorial Group: MEDICHUB MEDIA
DOI: 10.26416/Aler.1.1.2017.1241
Abstract
Rezumat
Reacțiile de hipersensibilitate (RHS) la agenți chimioterapici au o incidență în continuă creștere, cu un impact major în evoluția afecțiunilor oncologice, prin inducerea discontinuității unei terapii eficiente. Compușii cel mai frecvent implicați sunt sărurile de platină și taxanii, care pot determina RHS cu grade variate de severitate. Având în vedere riscul de catalogare a unor reacții adverse drept RHS, este recomandată folosirea unui protocol bine structurat de evaluare alergologică, în care testele specifice in vivo și in vitro și-au dovedit utilitatea. Există totuși o limitare privind testele cutanate, având în vedere riscul unei reacții iritative chiar la concentrații mici, în ciuda stabilirii anumitor concentrații considerate neiritative pentru testarea cutanată.
Managementul RHS la chimioterapice oferă două opțiuni majore, în funcție de severitatea reacției și dec risc: reluarea tratamentului cu un protocol modificat (ritmul perfuziei, premedicație etc.) sau înlocuirea agentului cauzal. În cazul lipsei unei alternative terapeutice, procedeul de desensibilizare permite continuarea terapiei în siguranță, îmbunătățind prognosticul oncologic. Desensibilizarea s-a dovedit un instrument terapeutic eficient în hipersensibilitatea la chimioterapice, tot mai multe studii prezentând protocoale de desensibilizare rapidă, în trepte, care au la bază escaladarea dozelor mici până la atingerea dozei totale terapeutice în câteva ore. EAACI Position Paper privind Alergo-Oncologia aduce cele mai recente informații în domeniu și demonstrează utilitatea demersului alergologic la pacienții cu RHS la medicația oncologică.
Introducere
Chimioterapicele anticanceroase, cunoscute și ca citotoxice, antitumorale, antineoplazice, citostatice etc., sunt medicamente destinate distrugerii selective a celulelor canceroase, perturbând procesele metabolice care stau la baza multiplicării acestora. În funcție de mecanismul de acțiune, citostaticele sunt împărțite în mai multe grupe: agenți alchilanți (de exemplu, ciclofosfamida, săruri de platină), antimetaboliți (de exemplu, metotrexat, 5-fluorouracil, capecitabină), antibiotice antitumorale și inhibitori de topoizomerază (de exemplu, doxorubicină, bleomicină), agenți cu acțiune pe microtubulii fusului de diviziune (de exemplu, taxani, alcaloizii de Vinca), terapii moleculare „țintite“ (de exemplu, crizotinib, lapatinib, sorafenib), anticorpi monoclonali (de exemplu, bevacizumab, cetuximab, rituximab), alte chimioterapice (de exemplu, L-asparaginaza, lenalidomida, thalidomida, interferonul alfa) și agenți hormonali (de exemplu, antiestrogeni, inhibitori de aromatază, antiandrogeni).
Orice agent chimioterapic poate genera o reacție de hipersensibilitate (RHS), cel mai frecvent implicate fiind sărurile de platină, taxanii, antraciclinele și anticorpii monoclonali(1).
Sărurile de platină și taxanii – date generale
Sărurile de platină sunt agenți alchilanți, care, prin intermediul ionului de metal greu, platina, determină în mod direct și indirect alterarea ADN-ului și a sintezei citoplasmatice de proteine. Reprezentații lor sunt: cisplatinul, carboplatinul și oxaliplatinul. Sunt folosite frecvent în special în cancerele ginecologice și cele colorectale.
Incidența RHS la sărurile de platină variază între 12% și 17%(2). Peste 50% dintre reacțiile la carboplatin și oxaliplatin sunt moderat-severe(3). Unele combinații au asociat o creștere a ratei de RHS, acestea fiind mai frecvente în cazul asocierii carboplatin-paclitaxel (18,8%) față de carboplatin-doxorubicină (5,5%)(4).
Taxanii sunt agenți citotoxici care acționează asupra fusului de diviziune și blochează depolimerizarea microtubulilor, împiedicând astfel diviziunea celulară(5). Din acest grup fac parte paclitaxelul, docetaxelul și nab-paclitaxelul. Aceștia sunt esențiali în tratamentul tumorilor (metastatice sau cu invazie locală) de sân, pulmon, prostată, ovare sau gastrice.
Incidența RHS la taxani variază între 8% și 50%(4). Aceasta poate fi redusă chiar sub 10%, cu premedicație adecvată(6).
RHS – factori de risc
În privința factorilor de risc, conform unui studiu recent(3), prevalența atopiei și a antecedentelor personale de RHS postmedicamentoase nu este semnificativ mai mare față de populația generală; aceste date nu sunt însă susținute și de alte cercetări(4).
Sexul feminin și numărul perfuziilor anterioare au fost considerați factori de risc pentru sărurile de platină(7). Cel mai frecvent, debutul primelor RHS apare după o medie de 6-10 cure de tratament cu săruri de platină(7). De asemenea, s-a constatat un risc de RHS la carboplatin de 47% dacă intervalul între curele de tratament era peste 24 luni și de 6,5%, dacă acest interval era sub 12 luni(4). Pentru taxani s-au evidențiat drept factori de risc istoricul de reacții tegumentare ușoare în timpul primelor administrări, prezența unor afecțiuni respiratorii, obezitatea și statusul postmenopauză(4).
RHS – clasificare
Terapia oncologică poate induce RHS imediate (survenite în timpul terapiei parenterale și până la 48 de ore de la administrare) sau RHS tardive (după 48 de ore)(8).
În cazul sărurilor de platină, cele mai multe RHS apar după curele 6-10 de tratament(7), ceea ce ar putea susține mecanismul de tip IgE-mediat(9).
În cazul taxanilor, reacțiile pot apărea de la prima sau de la a doua cură de tratament. Deși au fost raportate cazuri de reacții IgE-mediate la paclitaxel(3), se consideră că mecanismul principal implicat în RHS induse de taxani este degranularea mastocitelor și a bazofilelor(10). În unele cazuri, responsabil de RHS este considerat un excipient al citotoxicului. Din cauza proprietăților hidrofobe, taxanii necesită folosirea unui solvent pentru a facilita administrarea parenterală (Cremophor EL – ulei de ricin polioxietilat non-ionic pentru paclitaxel și surfactant polisorbat 80 non-ionic pentru docetaxel)(5). Solventul pentru paclitaxel poate avea un rol crucial în aceste RHS, cel pentru docetaxel fiind mai puțin incriminat în aceste reacții. Totuși folosirea anumitor generice de docetaxel (care conțin cantități variabile de etanol și polisorbat 80) poate crește riscul inductor al RHS(5).
RHS – manifestări clinice
RHS pot varia ca severitate de la cele ușoare, limitate la nivel cutanat, până la cele severe, care pot pune viața în pericol. Citotoxicele pot declanșa manifestări cutanate (rash, erupții morbiliforme, urticarie, prurit palmar, prurit generalizat, edem facial și al mâinilor), febră, colici abdominale, diaree, durere lombară, dar și manifestări mai severe, precum bronhospasm, tahicardie, hipotensiune sau hipertensiune arterială, durere toracică(11).
Reacțiile de toxicitate cutanată datorate taxanilor trebuie diferențiate de RHS induse de aceștia. Cea mai caracteristică formă de prezentare a unei astfel de reacții toxice cutanate constă din placarde intertriginoase inflamatoare, localizate axilar, inghinal și la nivelul pliului gâtului (în special în cazul docetaxelului)(5). Asociat, pot exista reacții veziculoase, necrotice și chiar ulcerații cronice. Alte manifestări cutanate induse de taxani pot fi: sindromul PATEO (Periarticular Thenar Erythema and Onycholysis – eritem tenar periarticular și onicoliză); leziuni care implică suprafețele extensoare ale brațelor și zonele laterale ale coapselor și ale genunchilor, în cazul paclitaxelului(12), fototoxicitate, dermatită postiradiere, eritrodiestezia fixă, accentuarea keratozei actinice(13). Rareori au fost descrise pentru taxani eritem polimorf, necroliză epidermică toxică (TEN – Toxic Epidermal Necrolysis) și sindrom Stevens-Johnson. Simptome atipice, precum durerea lombară, au fost asociate cu taxanii(1). Febra sau frisonul din timpul administrării citotoxicelor pot anunța posibile reacții anafilactice la următoarele administrări(8).
RHS – evaluare
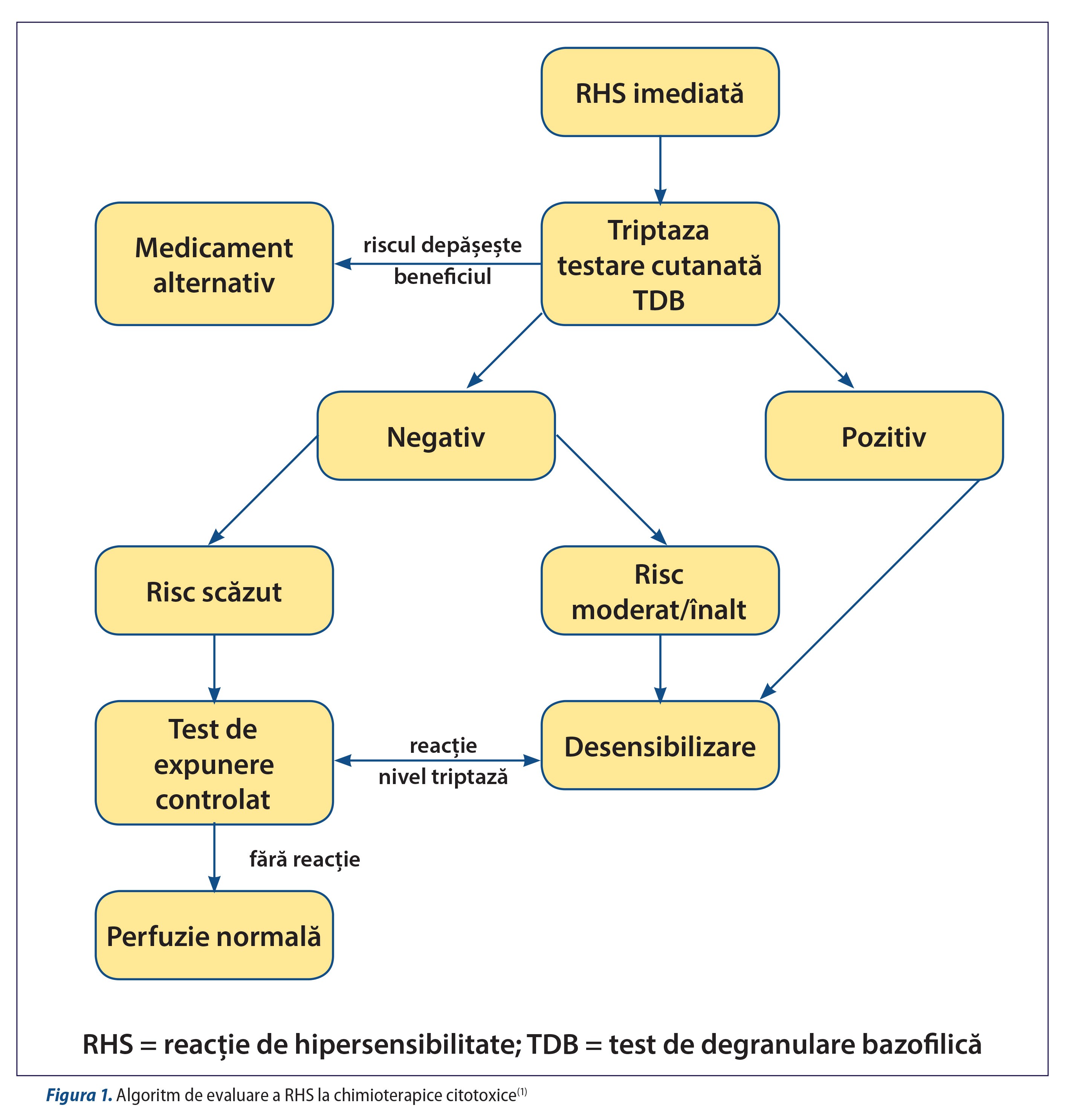
Dacă medicamentul incriminat în RHS reprezintă prima linie de tratament și nu există alternativă terapeutică, se inițiază un protocol de evaluare alergologică, cu scopul de readministrare în siguranță a terapiei incriminate (figura 1)(1). După evaluarea clinică și reluarea anamnezei, se stabilesc tipul de reacție (imediată sau tardivă) și gradul de severitate al reacției. În cazul în care reacția este considerată severă, se retrage total medicația. Pentru reacțiile imediate se poate recolta triptaza serică (în timpul reacției), se pot efectua teste in vitro (test de degranulare bazofilică) sau in vivo (teste cutanate). Rezultatele pozitive vor orienta către reintroducerea citotoxicului printr-un procedeu de desensibilizare. În cazul în care rezultatele testelor sunt negative, iar reacția inițială a fost ușoară, se recomandă testul de expunere controlată la medicația potențial ofensivă pentru confirmare. Un test de expunere controlat negativ recomandă reintroducerea medicamentului în perfuzie nemodificată, iar dacă după un test de expunere controlat reapare RHS, se poate folosi desensibilizarea. Pentru testele negative, dar la pacienți cu risc moderat/înalt sau istoric de reacții moderat-severe, se recomandă utilizarea protocolului de desensibilizare.
În cursul unei evaluări alergologice, pacienții pot fi împărțiți în două grupe: cu risc scăzut și cu risc înalt. Din ultima categorie fac parte pacienții cu reacție anterioară severă (de exemplu, istoric de intubare oro-traheală sau colaps cardiovascular), pacienții cu anumite afecțiuni care se pot ușor degrada (precum astm necontrolat sau afecțiune pulmonară cu VEMs<1 L) sau pacienții cu medicație concomitentă de tip beta-blocante care nu poate fi întreruptă, precum și gravidele.
Testele cutanate sunt considerate utile în reacțiile imediate la sărurile de platină(9), în timp ce pentru restul citotoxicelor experiența este limitată. Acestea ar trebui efectuate la cel puțin 2-6 săptămâni de la reacția anafilactică, pentru a evita un rezultat fals negativ datorat hiporeactivității mastocitare(4). În cursul testării intradermice pot apărea reacții adverse de toxicitate cutanată, din cauza activității locale citostatice. Agenții citotoxici pot fi iritanți chiar și la diluții mici(14), deși potențialul iritant al chimioterapicelor oncologice pare să fie mic, mai ales prin folosirea unei diluții de 1/10(9). Pentru sărurile de platină se recomandă folosirea nediluată pentru testarea cutanată(9) (tabelul 1).
Testarea prick se efectuează folosind concentrația maximă a medicamentului. În cazul unei reacții negative, se continuă evaluarea cu injectarea intradermică a 0,03 ml din soluția 1/10. O reacție la testarea intradermică este considerată pozitivă dacă papula este cu cel puțin 3 mm mai mare față de cea a controlului negativ(3).
Triptaza serică poate crește de 2-5 ori față de normal, în cazul unei RHS severe în cursul chimioterapiei citotoxice(15).


RHS – management
Managementul RHS la citotoxice urmează un protocol similar celorlalte RHS postmedicamentoase. După întreruperea tratamentului și în funcție de gradul de severitate, se vor administra oxigen, perfuzie de rehidratare, antihistaminice H1 și H2, adrenalină, corticosteroizi. Semnele de toxicitate cutanată pot necesita doar tratament corticosteroid topic. Uneori este utilă doar reducerea ritmului de administrare sau oprirea temporară a medicației(6). Reacțiile ușoare, de grad 1, tranzitorii (simptome cutanate – flush sau rash, febră medicamentoasă <38 grade Celsius), nu necesită terapie specifică(3) și tratamentul poate fi reluat în aceeași zi. Pacienții cu reacții ușor-moderate pot beneficia de reluarea tratamentului, cu reducerea ritmului perfuziei(4). Reacțiile severe de grad 3 (bronhospasm cu sau fără urticarie) și cele de grad 4, care pot pune viața în pericol, necesită măsuri terapeutice instituite urgent(3). Creșterea duratei de perfuzie la 3 ore a carboplatinului (față de standardul de 30 de minute), împreună cu premedicația adecvată ar putea reduce riscul de apariție a RHS (de la 21% la 3,4%, conform unui studiu(4)). Pentru paclitaxel însă, ritmul perfuziei pare să nu influențeze acest risc(4).
În urma unei RHS, se va lua în considerare inițial posibilitatea înlocuirii terapiei oncologice ofensive. Uneori cisplatinul poate substitui cu succes carboplatinul(6). A fost raportă reactivitate încrucișată între sărurile de platină (un studiu identifică un procent de reactivitate încrucișată de 25% între cisplatin și carboplatin(16)). Unele studii descriu reactivitate încrucișată între cei doi taxani la 41-90% dintre cazuri(6). În cazul reacțiilor la taxani în care vinovat ar fi vehiculul, există ca alternativă nab-paclitaxel (paclitaxel legat de albumină sub formă de nanoparticulă), care nu necesită solvent(6).
De cele mai multe ori, terapia „vinovată“ este singura utilă pentru pacient. Astfel, dacă după o atentă evaluare, beneficiul depășește riscul, se încearcă reintroducerea aceluiași citotoxic. Câștigarea toleranței la medicamentul ofensiv se efectuează prin intermediul procedeului de desensibilizare.
Premedicația
Protocoalele terapeutice oncologice folosesc în mod uzual premedicația standard cu antihistaminice H1 și corticosteroizi sistemici, cu scopul de a reduce riscul de RHS. Premedicația cu cele două clase de medicamente a scăzut rata de RHS din cursul tratamentului citotoxic, în special cu taxani(16). Tabelul 2 prezintă câteva dintre protocoalele de premedicație folosite pentru săruri de platină și taxani.
Desensibilizarea
Protocolul de desensibilizare presupune administrarea medicamentului progresiv în doze mici într-un ritm crescător, până la atingerea dozei terapeutice; procedura va fi efectuată într-un mediu controlat cu acces la un serviciu ATI. Tolerabilitatea este temporară, necesitând repetarea procedurii la următoarele cure de tratament. Prin acest procedeu se determină inhibarea mastocitului, protejând astfel pacienții de apariția unei reacții de anafilaxie(1). Beneficiază de desensibilizare atât sărurile de platină, cât și taxanii, cu următoarele condiții: reacții de tip imediat (până în 48 de ore), indicația de continuare a tratamentului cu citotoxicul incriminat anterior în RHS, pacienții aparțin grupului de risc crescut(3). Contraindicațiile absolute ale procedurii de desensibilizare sunt: eritemul polimorf, sindromul Stevens-Johnson, necroliza epidermică toxică (TEN – Toxic Epidermal Necrolysis), DRESS (Drug Reaction with Eosinophilia and Systemic Symptoms – reacție medicamentoasă cu eozinofilie și simptome sistemice), PEGA (pustuloza exantematică generalizată acută)(16).
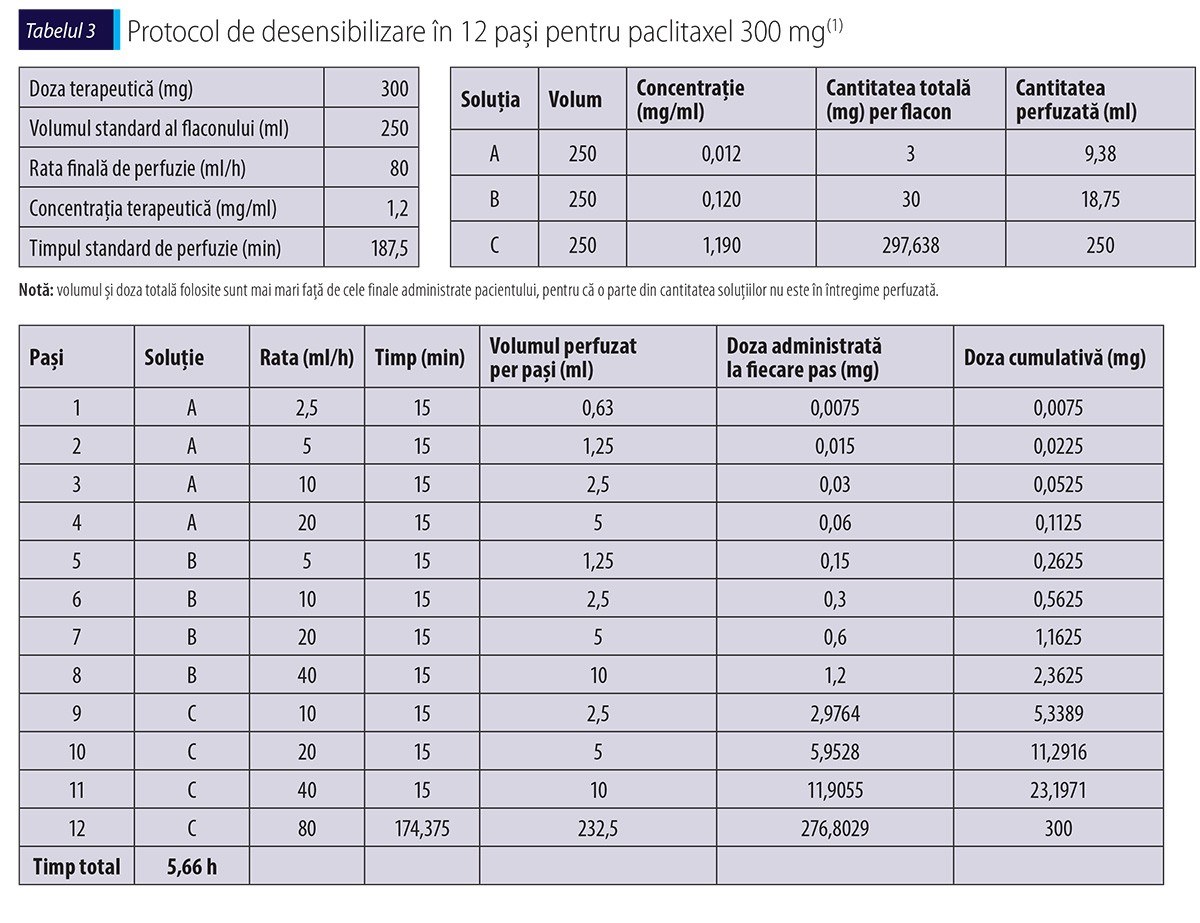
Protocolul de desensibilizare cel mai frecvent folosit recurge la 3 flacoane de soluție de concentrații progresiv crescânde (soluția A=X/100 mg, soluția B=X/10 mg, soluția C=X mg, fiecare fiind diluată în soluție salină sau dextroză 5% 250 ml, X reprezentând doza necesară a citotoxicului de administrat). Rata inițială de perfuzie a fiecărui flacon se dublează la fiecare 15 minute, primul flacon cu soluția A fiind administrat inițial cu un ritm de 2,5 ml/oră, soluția B cu 5 ml/oră, iar soluția C cu 10 ml/oră. Fiecare soluție este astfel administrată în decursul a câte patru pași. Timpul de perfuzie în cadrul ultimului pas al soluției C este suficient pentru a asigura administrarea întregii doze-țintă (tabelul 3).
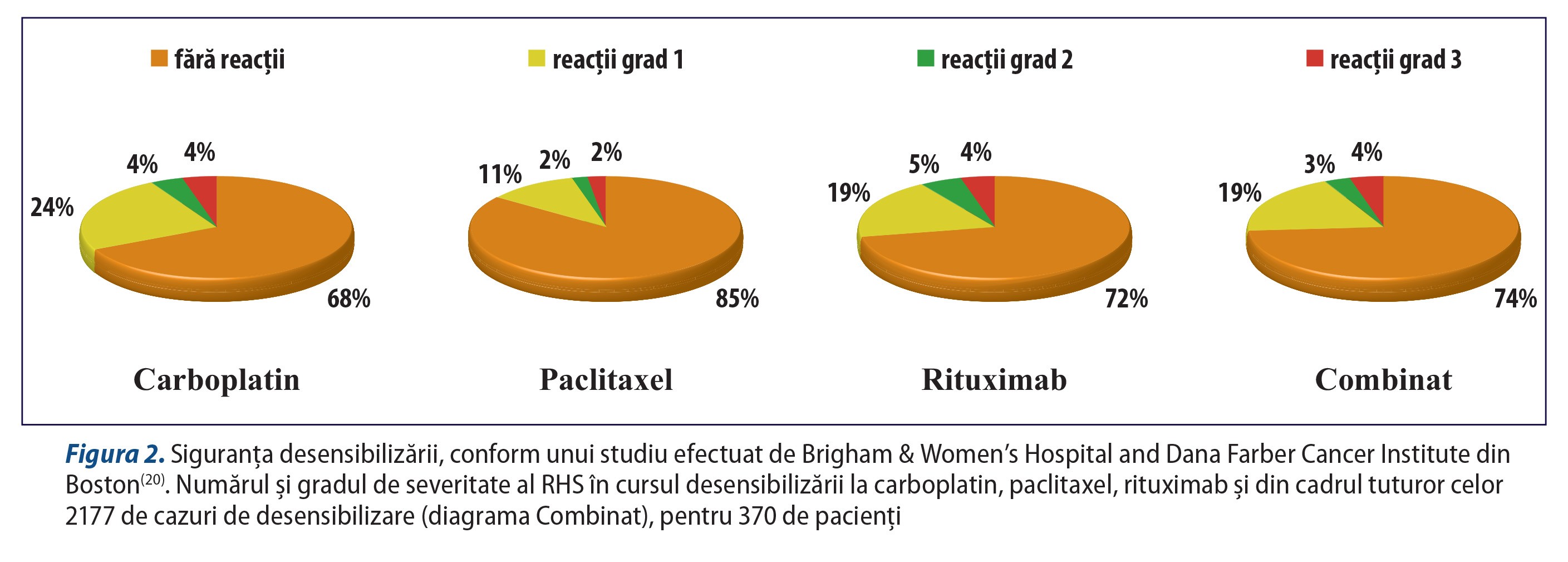
Protocoalele de desensibilizare sunt considerate sigure și eficiente, asigurând continuarea tratamentului oncologic(7). Într-un studiu care a cuprins 189 de desensibilizări rapide în cursul a 4 ore, care au implicat 23 de pacienți, 94% dintre aceștia nu au dezvoltat nicio reacție în cursul procedurii de desensibilizare, iar reacții ușoare de grad 1 au fost observate la 4%(3). Reacții moderate sau severe au dezvoltat doar 4 dintre pacienții incluși în studiu. Nu a fost înregistrată nicio reacție de grad 4 sau de grad 5 (deces). Majoritatea reacțiilor din timpul desensibilizării au apărut pe durata perfuziei cu soluția C. În cazul necesității unei noi desensibilizări pentru pacienții care au dezvoltat reacții în cursul acestei proceduri, s-a adăugat la premedicația standard acid acetilsalicilic 500 g per os și montelukast 10 mg, cu 2 ore înainte de procedură(3). Cel mai amplu studiu a fost realizat pe 370 de pacienți care au efectuat cu succes 2177 de desensibilizări(20). În cursul acestor proceduri, 93% nu au avut nicio reacție sau au asociat reacții ușoare, iar 7% au dezvoltat reacții moderate sau severe, dar care nu au împiedicat finalizarea tratamentului (figura 2).
Concluzii
RHS la chimioterapicele citotoxice pot cauza discontinuitatea unei terapii utile, contribuind astfel negativ la evoluția afecțiunilor oncologice. Deseori, alternativele disponibile nu sunt la fel de eficiente, ci sunt mai toxice și/sau mai costisitoare. Principalul factor de risc pentru sărurile de platină este reprezentat de numărul perfuziilor anterioare. Cel mai frecvent, RHS la sărurile de platină apar după cura a șasea de tratament. Premedicația s-a dovedit eficientă, în special în cazul taxanilor, putând scădea riscul de reacții acute cu până la 10%. Exceptând reacțiile severe tardive, protocolul de evaluare a RHS ar trebui să includă teste cutanate cu anumite concentrații considerate neiritante. Acestea pot prezice riscul unei reacții la reexpunere. În cazul unei testări pozitive sau al unui rezultat negativ la pacienți de risc înalt ori cu istoric de reacții moderat-severe, se poate lua în considerare reintroducerea medicației ofensive prin intermediul unui protocol de desensibilizare. Tot mai multe studii au dovedit siguranța și eficiența acestui procedeu, care permite continuarea unei terapii pentru care nu există alternative terapeutice.
Bibliografie
- Jensen-Jarolim E, Bax HJ, Bianchini R, Capron M, Corrigan C, Castells M, et al. AllergoOncology – the impact of allergy in oncology: EAACI position paper. Allergy 2017; 72: 866–887.
- Shoji T, Takatori E, Kaido Y et al. Usefulness of desensitization protocol for a carboplatin hypersensitivity reaction during docetaxel-carboplatin therapy for recurrent ovarian cancer: case report. Oncol Lett 2010; 1:1021–1023.
- Madrigal-Burgaleta R, Berges-Gimeno MP, Angel-Pereira D, Ferreiro-Monteagudo R, Guillen-Ponce C, Pueyo C, et al. Hypersensitivity and desensitization to antineoplastic agents: outcomes of 189 procedures with a new short protocol and novel diagnostic tools assessment. Allergy 2013; 68: 853–861.
- Boulanger J, Boursiquot JN, Cournoyer G et al. Management of hypersensitivity to platinum- and taxane-based chemotherapy: cepo review and clinical recommendations. Curr Oncol 2014; 21:e630–e641.
- Sibaud V, Leboeuf NR, Roche H, et al. Dermatological adverse events with taxane chemotherapy. Eur J Dermatol. 2016;26:427–443.
- Ho MY Mackey JR. Presentation and management of docetaxel-related adverse effects in patients with breast cancer. Cancer Manag Res 2014;6:253–9.
- Parel M, Ranchon F, Nosbaum A, You B, Vantard N, Schwiertz V, et al. Hypersensitivity to oxaliplatin: clinical features and risk factors. BMC Pharmacol Toxicol. 2014;15:1.
- Alvarez-Cuesta E, Madrigal-Burgaleta R, Angel-Pereira D, Urena-Tavera A, Zamora Verduga M, Lopez-Gonzalez P, Berges-Gimeno MP. Delving into cornerstones of hypersensitivity to antineoplastic and biological agents: value of diagnostic tools prior to desensitization. Allergy 2015; 70: 784–794.
- Brockow K, Garvey LH, Aberer W, Atanaskovic-Markovic M, Barbaud A, Bilo MB, et al. on behalf of the ENDA/EAACI Drug Allergy Interest Group. Skin test concentrations for systemically administered drugs – an ENDA/EAACI Drug Allergy Interest Group position paper. Allergy 2013; 68: 702–712.
- G Gastaminza, JM de la Borbolla, MJ Goikoetxea, R Escudero, J Antón, J Espinós, C Lacasa, M Fernández. A New Rapid Desensitization Protocol for Chemotherapy Agents. J Investig Allergol Clin Immunol 2011; Vol. 21(2): 108-112.
- Bergamini A, Pisano C, Di Napoli M, Arenare L, Della Pepa C, Tambaro R, et al. Cisplatin can be safely administered to ovarian cancer patients with hypersensitivity to carboplatin. Gynecol Oncol. 2017;144:72–6.
- Spicknall KE, Mutasim DF. Localized toxic erythema of chemotherapy during treatment with paclitaxel. Int J Dermatol 2014; 53: e3-5.
- Chambers CJ, Liu H, White CR, White KP, Sharon VR. Eruptive purpuric papules on the arms; a case of chemotherapy-induced inflammation of actinic keratoses and review of the literature. Dermatol Online J. 2014;20(1):21246.
- Caiado J, Venemalm L, Pereira-Santos MD, Costa L, Pereira Barbosa M, Castells M. Carboplatin-, Oxaliplatin-, and Cisplatin specific IgE: Cross-reactivity and Value in the Diagnosis of Carboplatin and Oxaliplatin Allergy. J Allergy Clin Immunol Pract. 2013;1:494-500.
- Castells Guitart MC. Rapid drug desensitization for hypersensitivity reactions to chemotherapy and monoclonal antibodies in the 21st century. J Investig Allergol Clin Immunol. 2014;24:72–9.
- Mezzano V, Giavina-Bianchi P, Picard M, Caiado J, Castells M. Drug desensitization in the management of hypersensitivity reactions to monoclonal antibodies and chemotherapy. BioDrugs. 2014;28(2):133-44.
- Castells MC, Tennant NM, Sloane DE, et al. Hypersensitivity reactions to chemotherapy: outcomes and safety of rapid desensitization in 413 cases. J Allergy Clin Immunol. 2008;122:574–80
- Feldweg AM, Lee CW, Matulonis UA, Castells M. Rapid desensitization for hypersensitivity reactions to paclitaxel and docetaxel: a new standard protocol used in 77 successful treatments. Gynecol Oncol 2005;96:824–9
- Ferrari LA. Are antineoplastic drug acute hypersensitive reactions a submerged or an emergent problem? Experience of the Medical Day Hospital of the Fondazione IRCCS Istituto Nazionale Tumori. Tumori. 2014;100(1):9–14.
- Sloane D, Govindarajulu U, Harrow-Mortelliti J, Barry W, Ida Hsu F, Hong D. Safety, Costs, and Efficacy of Rapid Drug Desensitizations to Chemotherapy and Monoclonal Antibodies. J Allergy Clin Immunol Pract. 2016 May-Jun; 4(3):497-504.
Articole din ediţiile anterioare
Managementul reacţiilor de hipersensibilitate întârziată (RHI) la interferonul alfa (IFN α)
Interferonul (IFN) α 2a şi 2b se utilizează în tratamentul hepatitei cronice cu virus C şi al melanomului. Din cauza similitudinii structurale cu I...
Reacţiile de hipersensibilitate induse de inhibitorii de pompă de protoni: strategii de diagnostic şi management
Inhibitorii de pompă de protoni (IPP) reprezintă o clasă de medicamente utilizate de elecţie în tratamentul patologiilor gastrointestinale caracter...
Hipersensibilitatea la preparatele de insulină
Hipersensibilitatea la preparatele la insulină reprezintă reacţia mediată imunologic faţă de insulină sau aditivii conţinuţi în preparat. Aceasta a...
Desensibilizarea la aspirină – când şi cum?
Aspirina (acidul acetilsalicilic) este una dintre cele mai utilizate terapii din lume. Administrată în doză mică (75-150 mg), aspirina are propriet...